زونيساميد
زونيساميد هوأحد أعضاء عائلة السلفوناميد المضادة للاختلاج المعتمدة للاستخدام كعلاج مساعد في البالغين المصابين بالنوبات ذات البداية الجزئية؛ والتشنج الصرعي، وأنواع النوبات المختلطة من متلازمة لينوكس-غاستوت، والرمع العضلي، والنوبة التوترية الرمعية.[3]
| زونيساميد | |
|---|---|
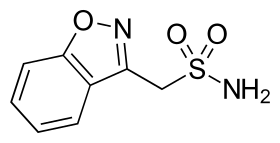 | |
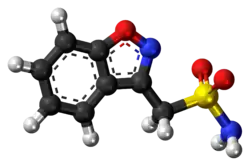 زونيساميد | |
| الاسم النظامي | |
| بنزو-إسوكسازول-3-ميثان سلفوناميد | |
| يعالج | |
| اعتبارات علاجية | |
| اسم تجاري | زونغران |
| ASHPDrugs.com | أفرودة |
| مدلاين بلس | a603008 |
| فئة السلامة أثناء الحمل | D (أستراليا) C (الولايات المتحدة) |
| طرق إعطاء الدواء | عن طريق الفم |
| بيانات دوائية | |
| توافر حيوي | ~100%[2] |
| ربط بروتيني | 40%[2] |
| استقلاب (أيض) الدواء | الكبد عن طريق سيتوكروم 3A4 |
| عمر النصف الحيوي | ساعات في الدم |
| إخراج (فسلجة) | الكلي(62%) والبراز( 3%) |
| معرّفات | |
| CAS | 68291-97-4 |
| ك ع ت | N03N03AX15 AX15 |
| بوب كيم | CID 5734 |
| IUPHAR | 7047 |
| ECHA InfoCard ID | 100.118.526 |
| درغ بنك | DB00909 |
| كيم سبايدر | 5532 |
| المكون الفريد | 459384H98V |
| كيوتو | D00538 |
| ChEBI | CHEBI:10127 |
| ChEMBL | CHEMBL750 |
| بنك بيانات البروتين ligand ID | ZON (PDBe, RCSB PDB) |
| بيانات كيميائية | |
| الصيغة الكيميائية | C8H8N2O3S |
| الكتلة الجزيئية | 212.227 غرام/مول |
| بيانات فيزيائية | |
| نقطة الانصهار | 162 °C (324 °F) |
الاستخدام الطبي
النوبات
تمت الموافقة على استخدام زونيساميد في الولايات المتحدة،[4] والمملكة المتحدة،[5] وأستراليا[6] كعلاج مساعد لللنوبات الجزئية في البالغين وفي اليابان كعلاج مساعد وأساسي للنوبات الجزئية (البسيطة والمعقدة والمعممة بشكل ثانوي) والنوبات المًعممة (التوترية، التوتري-الرمعية، والغياب غير النمطي) والنوبات المركبة.[7]
بالنسبة للصرع، استخدمت معظم الدراسات الزونيساميد عن طريق الفم في جرعات يومية تتراوح من 200 إلى 600 ملليغرام / يوم، مقسمة إلى جرعتين يوميًا، معدلة للحفاظ على مستويات المصل من 15 إلى 40 ميكروجرام / مليلتر.[8][9][10][11]
خلل الحركة المتأخر
في تجربة مُسماة مفتوحة، خفف الزونيساميد من أعراض خلل الحركة المتأخر.[12]
السمنة
كما تمت دراسة استخدام الزونيساميد في علاج السمنة[13] مع تأثيرات إيجابية كبيرة على فقدان وزن الجسم، وهناك ثلاث تجارب سريرية جارية لهذا المؤشر.[14][15][16] يُباع الزونيساميد في الأسواق كعلاج للسمنة ممزوجًا مع بوبروبيون، تحت اسم العلامة التجارية إمباتيك.
الصداع النصفي
تمت دراسة الزونيساميد كعلاج وقائي للصداع النصفي، كما أثبت فعاليته أيضًا في بعض حالات آلام الأعصاب.
الاكتئاب ثنائي القطب
كما تم استخدامه بدون تصريح من قبل الأطباء النفسيين كعلاج للاكتئاب ثنائي القطب.[17][18]
الآثار الجانبية
تشمل الآثار الجانبية المنتشرة ( حدثت في 1-10% من الحالات) ما يلي
- الكدمات
- فرط الحساسية
- التأثير على القدرة على التحمل
- القلق
- الأرق
- الاضطراب الذهاني
- تبلد الذهن
- اضطرابات التركيز
- الرأرأة (تذبذب المقلتين السريع اللإرادي)
- اضطراب الكلام
- رعشه
- وجع البطن
- الإمساك
- الإسهال
- سوء الهضم
- الغثيان
- طفح جلدي
- الحكة
- تساقط الشعر
- حصوات الكلية
- الإعياء
- أعراض تشبه الإنفلونزا
- الحمى
- الوذمة الطرفية
- خسارة الوزن
التفاعلات الدوائية
عُرف عن الزونيساميد وغيرها من مثبطات الأنهيدراز الكربوني مثل التوبيرامات، والفوروسيميد، والهيدروكلوروثيازيد أنهت تتداخل دوائيًا مع الأموباربيتال، مما يؤدي إلى تخدير غير كافٍ خلال اختبار وادا.[21] يتفاعل الزونيساميد أيضا مع مثبطات الأنهيدراز الكربوني الأخرى لزيادة إمكانية حدوث الحماض الأيضي.[2]
بالإضافة إلى ذلك، يتم تثبيط عملية التمثيل الغذائي للزونيساميد من قبل كيتوكونازول، وسيكلوسبورين، وميكونازول، وفلوكونازول وكاربامازيبين (في ترتيب تنازلي) بسبب آثارها على إنزيم سيتوكروم 3A4.[22]
ومن المعروف أن الزونيساميد يثبط انزيمات السيتوكروم بي 450 عند تناوله في تركيزات علاجية.[23]
آلية العمل
الزونيساميد هو دواء مضاد للتشنج مصنف كيميائيًا على أنه من عائلة السولفوناميد ولا علاقة له بمضادات الاختلاج الأخرى. الآلية الدقيقة لتأثير الزونيساميد المضاد للتشنجات غير معروفة، على الرغم من أنه يعتقد أنه ثثبط قنوات الصوديوم وقنوات الكالسيوم من النوع T، الأمر الذي يؤدي إلى تثبيط فرط التزامن للخلايا العصبية (وبالتالي تثبيط آلية حدوث التشنجات).[6] كما يُصنف الزونيساميد أيضًا من مثبطات الأنهيدراز الكربوني الضعيفة ( (على غرار مضاد الاختلاج أسيتازولاميد). كما يعرف عنه أيضًا التأثيرعلى الانتقال العصبي لحمض الغاما-أمينوبيوتيريك وحمض الجلوتاميك.[6][24][25][26][27]
الحركة الدوائية
الامتصاص
امتصاص الزونيساميد متغير، ولكنه ذو معدل امتصاص سريع نسبيًا إذ يصل تركيزه إلى الذروة في حوالي 2.8-3.9 ساعة. يقترب التوافر البيولوجي للزونيساميد من 100٪ ولا تؤثر المواد الغذائية على التوافر البيولوجي للزونيساميد ولكنها قد تؤثر على معدل الامتصاص.[23][28]
الأيض
يتم أيض الزونيساميد في الغالب من قبل النظير الإنزيمي سيتوكروم 3A4 ، ولكن تدخل إنزيمات CYP3A7 و CYP3A5،[29] أيضًا في تحويله إلى إلى 2- سولفامويل أستيل - فينول عن طريق الانقسام الاختزالي لحلقة 1,2 بنزيسوكسازول.[30]
التاريخ
تم اكتشاف الزونيساميد من قبل أونو وزملائه في عام 1972.[31] وبدأت شركة داينيبون سوميتومو فارما (داينيبون فارماسيوتيكال سابقًا) توزيعه في الأسواق في عام 1989 تحت مسمى إكسيغران في اليابان.[32] كما سوقته شركة إيلان في الولايات المتحدة ابتداءًا من عام 2000 تحت مسمى زونغران، قبل أن تننقل شركة إيلان حقها في تسويق الزونيساميد لشركة إيساي المحدودة في عام 2004.[33] وزعت شركة إيساي أيضًا زونغران في أسواق آسيا (الصين وتايوان، وأربعة عشر دولة أخرى)[34] وأوروبا (بدءًا من ألمانيا والمملكة المتحدة).[35]
مراجع
- معرف المصطلحات المرجعية بملف المخدرات الوطني: https://bioportal.bioontology.org/ontologies/NDFRT?p=classes&conceptid=N0000148668 — تاريخ الاطلاع: 13 ديسمبر 2016
- "Zonegran® Product Information". TGA eBusiness Services. SciGen (Australia) Pty Ltd. 4 April 2013. مؤرشف من الأصل (PDF) في 15 أكتوبر 2018. اطلع عليه بتاريخ 18 نوفمبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Comprehensive Pharmacy Review, Leon Shargel, 6th edition, p988
- Élan Pharmaceuticals Inc (22 August 2003). "NDA 20-789/S-001; Zonegran (zonisamide) Capsules 25, 50, 100 mg FDA Approvable Labeling Text" (PDF). Zonisamide Approval History. Food and Drug Administration. مؤرشف من الأصل (PDF) في 12 فبراير 2017. اطلع عليه بتاريخ 24 أغسطس 2009. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Eisai Ltd. (2005). "Zonegran Summary of Product Characteristics". electronic Medicines Compendium. Medicines.org.uk. مؤرشف من الأصل في 10 يوليو 2018. اطلع عليه بتاريخ 13 نوفمبر 2005. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Rossi, S, المحرر (2013). Australian Medicines Handbook (الطبعة 2013). Adelaide: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dainippon Pharmaceutical Co., Ltd. (2004). "EXCEGRAN Tablets 100 mg & EXCEGRAN Powder 20%" (PDF). مؤرشف من الأصل (PDF) في 28 سبتمبر 2007. اطلع عليه بتاريخ 13 مارس 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Shimizu A, Ikoma R, & Shimizu T: Effects and side effects of zonisamide during long-term medication. Curr Ther Res 1990; 47:696-706
- Iinuma K, Handa I, Fueki N, et al: Effects of zonisamide (AD-810) on refractory epilepsy in children: special reference to temporal lobe abnormalities. Curr Ther Res 1988; 43:281-282
- Sakamoto K, Kurokawa T, Tomita S, et al: Effects of zonisamide in children with epilepsy. Curr Ther Res 1988; 43:378-383
- Shimizu A, Yamamoto J, Yamada Y, et al: The antiepileptic effect of zonisamide in patients with refractory seizures. Curr Ther Res 1987; 42:147-155
- Iwata, Y; Irie, S; Uchida, H; Suzuki, T; Watanabe, K; Iwashita, S; Mimura, M (15 April 2012). "Effects of zonisamide on tardive dyskinesia: a preliminary open-label trial". Journal of the Neurological Sciences. 315 (1–2): 137–140. doi:10.1016/j.jns.2011.12.010. PMID 22285275. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gadde, Kishore M.; Franciscy, Deborah M.; Wagner, II, H. Ryan; Krishnan, K. Ranga R. (April 2003). "Zonisamide for Weight Loss in Obese Adults: A Randomized Controlled Trial". Journal of the American Medical Association. 289 (14): 1820–1825. doi:10.1001/jama.289.14.1820. PMID 12684361. الوسيط
|CitationClass=تم تجاهله (مساعدة) - University of Cincinnati (2005). "Zonegran in the Treatment of Binge Eating Disorder Associated With Obesity". ClinicalTrials.gov. مؤرشف من الأصل في 19 أغسطس 2017. اطلع عليه بتاريخ 04 مايو 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Tuscaloosa Research; Education Advancement Corporation (2005). "Zonegran for the Treatment of Weight Gain Associated With Psychotropic Medication Use: A Placebo-Controlled Trial". ClinicalTrials.gov. مؤرشف من الأصل في 19 أغسطس 2017. اطلع عليه بتاريخ 04 مايو 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة) - National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK) (2006). "Zonisamide for Weight Reduction in Obese Adults". ClinicalTrials.gov. مؤرشف من الأصل في 19 أغسطس 2017. اطلع عليه بتاريخ 04 مايو 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Brian D. Loftus (2004). "Zonegran". مؤرشف من الأصل في 21 أغسطس 2016. اطلع عليه بتاريخ 29 نوفمبر 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Hasegawa, Hisanori (May 2004). "utilization of zonisamide in patients with chronic pain or epilepsy refractory to other treatments: a retrospective, open label, uncontrolled study in a VA hospital". Curr Med Research Opinion. 20 (5): 577–580. doi:10.1185/030079904125003313. PMID 15140322. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Zonegran 25, 50, 100 mg Hard Capsules". electronic Medicines Compendium. Eisai Ltd. 8 October 2013. مؤرشف من الأصل في 16 أكتوبر 2018. اطلع عليه بتاريخ 18 نوفمبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "zonisamide (Rx) - Zonegran". Medscape Reference. WebMD. مؤرشف من الأصل في 26 يونيو 2018. اطلع عليه بتاريخ 18 نوفمبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Bookheimer, Susan; Schrader, Lara M.; Rausch, Rebecca; Sankar, Raman; Engel, Jerome Jr. (February 2005). "Reduced anesthetization during the intracarotid amobarbital (Wada) test in patients taking carbonic anhydrase-inhibiting medications". Epilepsia. 46 (2): 236–43. doi:10.1111/j.0013-9580.2005.23904.x. PMID 15679504. الوسيط
|CitationClass=تم تجاهله (مساعدة)[وصلة مكسورة] - Nakasa, H.; Nakamura H; Ono S; Tsutsui M; Kiuchi M; Ohmori S; Kitada M. (April 1998). "Prediction of drug-drug interactions of zonisamide metabolism in humans from in vitro data". European Journal of Clinical Pharmacology. 54 (2): 177–83. doi:10.1007/s002280050442. PMID 9626925. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Zonegran 25, 50, 100 mg Hard Capsules". Electronic Medicines Compendium (eMC). مؤرشف من الأصل في 14 فبراير 2019. اطلع عليه بتاريخ 12 أبريل 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Leppik, Ilo E. (December 2004). "Zonisamide: chemistry, mechanism of action, and pharmacokinetics". Seizure. 13 (Suppl 1): S5–9, discussion S10. doi:10.1016/j.seizure.2004.04.016. PMID 15511691. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Mimaki, T; Suzuki, Y; Tagawa, T; Karasawa, T; Yabuuchi, H (March 1990). "Interaction of zonisamide with benzodiazepine and GABA receptors in rat brain". Medical Journal of Osaka University. 39 (1–4): 13–7. PMID 1369646. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Mimaki, T; Suzuki, Y; Tagawa, T; Karasawa, T; Yabuuchi, H (March 1990). "[3H]zonisamide binding in rat brain". Medical Journal of Osaka University. 39 (1–4): 19–22. PMID 1369647. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ueda, Y; Doi, T; Tokumaru, J; Willmore, J (2003-08-19). "Effect of zonisamide on molecular regulation of glutamate and GABA transporter proteins during epileptogenesis in rats with hippocampal seizures". Molecular Brain Research. 116 (1–2): 1–6. doi:10.1016/S0169-328X(03)00183-9. PMID 12941455. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Zonisamide - DrugBank نسخة محفوظة 02 يوليو 2017 على موقع واي باك مشين.
- Ohmori, S.; Nakasa H; Asanome K; Kurose Y; Ishii I; Hosokawa M; Kitada M (1998-05-08). "Differential catalytic properties in metabolism of endogenous and exogenous substrates among CYP3A enzymes expressed in COS-7 cells". Biochimica et Biophysica Acta. 1380 (3): 297–304. doi:10.1016/s0304-4165(97)00156-6. PMID 9555064. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Stiff, D. D.; Robicheau JT; Zemaitis MA. (January 1992). "Reductive metabolism of the anticonvulsant agent zonisamide, a 1,2-benzisoxazole derivative". Xenobiotica. 22 (1): 1–11. doi:10.3109/00498259209053097. PMID 1615700. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Shah J, Kent Shellenberger, Daniel M. Canafax (2002-06-15) [1972]. "Zonisamide". In René H, Levy RH, Brian SM, Perrucca E (المحررون). Antiepileptic Drugs (الطبعة Fifth). Philadelphia: Lippincott Williams & Wilkins. صفحة 873. ISBN 0-7817-2321-3. اطلع عليه بتاريخ 07 نوفمبر 2007. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dainippon Sumitomo Pharma Co. Ltd. (2005). "Company History". Company Information. Dainippon Sumitomo Co., Ltd. مؤرشف من الأصل في 13 فبراير 2006. اطلع عليه بتاريخ 12 نوفمبر 2005. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dainippon Pharmaceutical Co. Ltd. (2004). "Transfer of Rights Agreement for North America and Europe Reached on Zonegran". News Releases for Dainippon Pharmaceutical in 2004. Dainippon Sumitomo Pharma Co., Ltd. مؤرشف من الأصل في 13 فبراير 2006. اطلع عليه بتاريخ 12 نوفمبر 2005. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dainippon Pharmaceutical Co. Ltd. (2005). "Dainippon Pharmaceutical and Eisai Conclude Agreement for the Development, Manufacture and Marketing of the Anti-Epileptic Agent Zonisamide in Asia". Dainippon Pharmaceutical News Releases for 2005. Dainippon Sumitomo Pharma Co., Ltd. مؤرشف من الأصل في 22 فبراير 2006. اطلع عليه بتاريخ 12 نوفمبر 2005. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Eisai Co. Ltd. (2005). "Eisai Announces Launch of Zonegran (zonisamide), Treatment For Epilepsy In the UK and Germany". Eisai 2005 News Releases. Eisai Co., Ltd. مؤرشف من الأصل في 07 فبراير 2012. اطلع عليه بتاريخ 12 نوفمبر 2005. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ أرشيف=(مساعدة)
روابط خارجية
- Official Eisai Website
- Dainippon Sumitomo Prescribing Information for Excegran[permanent dead link(ويكيبيديا:وصلات خارجية مكسورة)] (Japanese version)
- Official Dainippon Sumitomo Pharma Website (English version)
- بوابة صيدلة
- بوابة طب
