أسينابين
يُباع لأسينابين تحت الاسمين التجاريين سافريس وسيكريست وغيرهما، وهو مضاد غير نمطي للذهان يُستخدم لعلاج الفصام والهوس الحاد المرتبط بالاضطراب ثنائي القطب .
| أسينابين | |
|---|---|
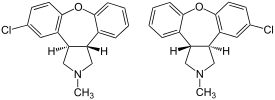 | |
 أسينابين | |
| يعالج | |
| اعتبارات علاجية | |
| اسم تجاري | Saphris, Sycrest |
| ASHPDrugs.com | أفرودة |
| مدلاين بلس | a610015 |
| الوضع القانوني | وكالة الأدوية الأوروبية:وصلة، إدارة الغذاء والدواء:وصلة |
| فئة السلامة أثناء الحمل | C (أستراليا) C (الولايات المتحدة) |
| طرق إعطاء الدواء | sublingual |
| بيانات دوائية | |
| توافر حيوي | 35% (تحت اللسان), <2% (عن طريق الفم)[2][3][4][5] |
| ربط بروتيني | 95%[2][3][4][5] |
| استقلاب (أيض) الدواء | hepatic (glucurinodation by UGT1A4 and oxidative metabolism by CYP1A2)[2][3][4][5] |
| عمر النصف الحيوي | 24 hours[2][3][4][5] |
| إخراج (فسلجة) | كلية (50%), براز (40%; ~5-16% as unchanged drug in faeces)[2][3][4][5] |
| معرّفات | |
| CAS | 65576-45-6 |
| ك ع ت | N05N05AH05 AH05 |
| بوب كيم | CID 163091 |
| IUPHAR | 22 |
| ECHA InfoCard ID | 100.059.828 |
| كيم سبايدر | 2300725 |
| المكون الفريد | JKZ19V908O |
| ChEBI | CHEBI:71253 |
| ChEMBL | CHEMBL1201756 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C17H16ClNO |
| الكتلة الجزيئية | 285.77 g/mol |
يُشتق الأسينابين كيميائيًا عن طريق تغيير التركيب الكيميائي لمضاد الاكتئاب الميانسيرين رباعي الكريات. [6]
الاستخدامات الطبية
وافقت إدارة الغذاء والدواء FDA على استخدام أسينابين للعلاج الحالات الحادة للبالغين المصابين بالفصام والحالات الحادة من نوبات الهوس أو النوبات المختلطة المرتبطة باضطراب ثنائي القطب من النوع الأول مع أو بدون أعراض ذهانية. [7] كما تمت الموافقة في أستراليا على استخدام أسينابين في علاج ما يلي: [8]
- الفصام
- حالات الهوس الحاد أو النوبات المختلطة المرتبطة بالاضطراب ثنائي القطب لمدة تصل إلى 6 أشهر
- كجرعة وقائية، أو كعلاج وحيد، لاضطراب ثنائي القطب
في الاتحاد الأوروبي والمملكة المتحدة، يتم ترخيص الآسينابين فقط للاستخدام كعلاج لهوس حاد في الاضطراب الثنائي القطب.
يُمتص الأسينابين بسهولة إذا تم تناوله تحت اللسان ، ويتم امتصاصه بشكل سيء عند البلع. [9]
الفصام
لا يوجد سوى دليل ضعيف يدعم استخدام لعلاج مرض الفصام، مما يجعل من الصعب التوصية به لهذا الاستخدام. [10]
الهوس الحاد
بالنسبة لفعاليته في علاج الهوس الحاد، أظهر التحليل التلوي مؤخرًا أنه ينتج تحسينات صغيرة نسبيًا في أعراض الهوس في المرضى الذين يعانون من الهوس الحاد والنوبات المختلطة من معظم مضادات الذهان الأخرى (باستثناء زيبراسيدون) مثل الريسبيريدون وأولانزابين. وكانت معدلات التسرب (في التجارب السريرية) مرتفعة بشكل غير عادي مع الأسينابين. [11] وفقًا للتحليل اللاحق الذي تم إجراؤه على تجربتين سريريتين لمدة 3 أسابيع، فقد يكون له بعض التأثيرات المضادة للاكتئاب في المرضى الذين يعانون من الهوس الحاد أو الحلقات المختلطة. [12]
الآثار السلبية
حالات التأثير الضار
الآثار الضارة الشائعة (> 10٪) تشمل:
الآثار الضارة الشائعة (1-10 ٪) تشمل:
- زيادة الوزن
- زيادة الشهية
- الآثار الجانبية خارج هرمية (مثل خلل التوتر، أكاثيسيا، خلل الحركة، صلابة العضلات، الشلل الرعاش)
- سكون
- دوخة
- خلل الذوق
- نقص الإحساس بالفم
- زيادة مستويات إنزيم ألانين أمينوترفراز
- إعياء
الآثار غير المألوفة (حدوث 0.1-1 ٪) تشمل ما يلي:
- ارتفاع السكر في الدم
- إغماء
- تشنج
- تلعثم
- بطء القلب الجيبي
- حزمة كتلة فرع
- إطالة فترة كيو تي. [13]
- عدم انتظام دقات القلب الجيوب الأنفية
- هبوط ضغط الدم الانتصابى
- انخفاض ضغط الدم
- تورم اللسان
- عسر البلع (صعوبة البلع)
- ألم اللسان
- مخدر الفم
الآثار السلبية النادرة (0.01-0.1٪) تشمل:
- متلازمة مضادات الذهان الخبيثة (مزيج من الحمى، وتصلب العضلات، وزيادة معدل التنفس، تعرق، وانخفاض الوعي، وتغيير مفاجئ في ضغط الدم ومعدل ضربات القلب)
- خلل الحركة المتأخر
- اضطراب الكلام
- انحلال الربيدات
- وذمة وعائية
- خلل التنسج الدموي مثل ندرة المحببات ونقص الكريات البيض وقلة العدلات
- اضطراب التكيف
- الانسداد الرئوي
- تثدي الرجل
- ثر اللبن
الآثار الضارة حدوث غير معروف
- رد فعل تحسسي
- متلازمة تململ الساقين
- غثيان
- تقرحات الفم
- فرط إفراز اللعاب
- زيداة إفراز البرولاكتين
التاريخ
طوّرت شركة شيرينغ بلاو الأسينابين لأول مرة بعد اندماجها مع شركة أورغانون الدولية في 19 نوفمبر 2007. رغم أن تجارب المرحلة الثالثة بدأت بينما كانت لا تزال شركة أورغانون جزءًا من شركة أكزو نوبل. [14] تشير البيانات الأولية إلى أنه يحتوي على الحد الأدنى من الآثار الجانبية المضادة للكولين والقلب والأوعية الدموية، فضلاً عن الحد الأدنى من زيادة الوزن. شارك أكثر من 3000 شخص في التجارب السريرية للأسينابين، ووافقت إدارة الأغذية والعقاقير على تصنيعه في أغسطس 2009. [15]
المراجع
- https://dx.doi.org/10.5281/ZENODO.1435999
- "PRODUCT INFORMATION SAPHRIS® (asenapine maleate)". TGA eBusiness Services. Merck Sharp & Dohme (Australia) Pty Limited. 14 January 2013. مؤرشف من الأصل (PDF) في 2 أبريل 2019. اطلع عليه بتاريخ 23 أكتوبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "SAPHRIS (asenapine maleate) tablet [Organon Pharmaceuticals USA]". DailyMed. Organon Pharmaceuticals USA. March 2013. مؤرشف من الأصل في 3 ديسمبر 2013. اطلع عليه بتاريخ 23 أكتوبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Sycrest 5mg and 10mg sublingual tablets - Summary of Product Characteristics (SPC)". electronic Medicines Compendium. Lundbeck Limited. 18 April 2013. مؤرشف من الأصل في 2 فبراير 2017. اطلع عليه بتاريخ 23 أكتوبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Product information 21/02/2013 Sycrest -EMEA/H/C/001177 -II/0012" (PDF). European Medicines Agency. N.V. Organon. 21 February 2013. مؤرشف من الأصل (PDF) في 28 يوليو 2017. اطلع عليه بتاريخ 23 أكتوبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Minassian, A; Young, JW (August 2010). "Evaluation of the clinical efficacy of asenapine in schizophrenia". Expert Opinion on Pharmacology. 11 (12): 2107–2115. doi:10.1517/14656566.2010.506188. PMID 20642375. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Saphris (asenapine) prescribing information" (PDF). Schering Corporation. 2009-08-01. مؤرشف من الأصل (PDF) في 22 نوفمبر 2009. اطلع عليه بتاريخ 05 سبتمبر 2009. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Rossi, S, المحرر (2013). Australian Medicines Handbook (الطبعة 2013). Adelaide: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Stoner, Steven (2012). "Asenapine: a clinical review of a second-generation antipsychotic". Clinical Therapeutics. 34 (5): 1023–40. doi:10.1016/j.clinthera.2012.03.002. PMID 22494521. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Hay, A; Byers, A; Sereno, M (2015). "Asenapine versus placebo for schizophrenia". Cochrane Database of Systematic Reviews (11): CD011458.pub2. doi:10.1002/14651858.CD011458.pub2. PMID 26599405. مؤرشف من الأصل في 17 يونيو 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Cipriani, A; Barbui, C; Salanti, G; Rendell, J; Brown, R; Stockton, S; Purgato, M; Spineli, LM; Goodwin, GM (October 2011). "Comparative efficacy and acceptability of antimanic drugs in acute mania: a multiple-treatments meta-analysis". Lancet. 378 (9799): 1306–1315. doi:10.1016/S0140-6736(11)60873-8. PMID 21851976. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Szegedi, A; Zhao, J; van Willigenburg, A; Nations, KR; Mackle, M; Panagides, J (June 2011). "Effects of asenapine on depressive symptoms in patients with bipolar I disorder experiencing acute manic or mixed episodes: a post hoc analysis of two 3-week clinical trials". BMC Psychiatry. 11: 101. doi:10.1186/1471-244X-11-101. PMID 21689438. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Washington, Nicole B. (October 2012). "Which psychotropics carry the greatest risk of QTc prolongation?". Current Psychiatry. 11 (10): 36–39. مؤرشف من الأصل في 25 يونيو 2017. اطلع عليه بتاريخ 14 أبريل 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Bipolar Disorder". Clinical Trials Update. Genetic Engineering & Biotechnology News. 2007-06-15. صفحات 52, 55. الوسيط
|CitationClass=تم تجاهله (مساعدة) - (Press release). الوسيط
|CitationClass=تم تجاهله (مساعدة); مفقود أو فارغ|title=(مساعدة)[وصلة مكسورة]
- بوابة صيدلة
- بوابة طب
