داء بطني
الداء البطني، الداء الزلاقي[بحاجة لمصدر]، السيلياك وأحيانا (مرض حساسية القمح) والأخير يعتبر وصف غير دقيق، كلها أسماء متعددة لمرض واحد هو (بالإنجليزية: Coeliac disease) ويكتب احيانا (بالإنجليزية: Celiac disease). هو مرض مناعي ذاتي مكتسب يصيب الأمعاء الدقيقة لدى الأشخاص ذوي العرضة والذين يتمتعون بقابلية جينية للإصابة به.[2] تشمل الأعراض الكلاسيكية مشاكل في الجهاز الهضمي مثل الإسهال المزمن وانتفاخ البطن وسوء الامتصاص وفقدان الشهية وبين فشل الأطفال في النمو بشكل طبيعي.[3] هذا غالبا ما يبدأ بين ستة أشهر وسنتين من العمر.[3] الأعراض غير الكلاسيكية أكثر شيوعًا، خاصة في الأشخاص الذين تزيد أعمارهم عن عامين.[4][5][6] قد تكون هناك أعراض معدية معوية أو غائبة، أو عدد كبير من الأعراض التي تنطوي على أي جزء من الجسم أو بدون أعراض واضحة.[3]
| Coeliac disease | |
|---|---|
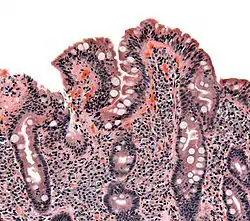 صورة لخزعة نسيجية تظهر أعراض داء بطني على الأمعاء صورة لخزعة نسيجية تظهر أعراض داء بطني على الأمعاء | |
| تسميات أخرى | celiac sprue, nontropical sprue, endemic sprue, gluten enteropathy |
| النطق | /ˈsiːli.æk/ |
| معلومات عامة | |
| الاختصاص | طب الجهاز الهضمي |
| من أنواع | مرض الجهاز الهضمي بالمناعة الذاتية ، واعتلال معوي غلوتيني |
| المظهر السريري | |
| الأعراض | إسهال [1]، والإمساك [1]، وتقيؤ [1]، وغثيان [1] |
تم وصف مرض الاضطرابات الهضمية لأول مرة في مرحلة الطفولة؛[7][4] ومع ذلك، فقد يتطور في أي عمر.[3][4] تتراوح نسبة حدوث هذا المرض لدى الأطفال ما بين 0.33 – 1.06 % أما لدى البالغين فيتراوح العدد ما بين 0.18 – 1.2 %، بعض الحالات المرضية كمتلازمة داون والسكري المعتمد على الانسولين ومتلازمة تيرنر لديهم قابلية أعلى للإصابة بداء بطني وتتراوح نسبة الإصابة لديهم بين 5 – 10 %، حدوث الداء البطني كردة فعل للتعرض لمادة الغليادين الموجودة في الحبوب وخاصة القمح، وتؤدي إلى حالة اعتلال معوي بسبب الغليادين.
العلامات والأعراض
الأعراض الكلاسيكية لمرض الاضطرابات الهضمية غير المعالجة تشمل براز شاحب، لين، دهني، وفقدان الوزن أو الفشل في زيادة الوزن. قد تكون الأعراض الشائعة الأخرى خفية أو تحدث بشكل أساسي في أعضاء أخرى غير الأمعاء نفسها.[8] من الممكن أيضًا الإصابة بمرض الاضطرابات الهضمية دون أي من الأعراض الكلاسيكية على الإطلاق.[9] تبين أن هذا يشتمل على 43٪ على الأقل من العروض التقديمية لدى الأطفال.[10] علاوة على ذلك، قد يصاب العديد من البالغين المصابين بأمراض خفية فقط بالتعب أو فقر الدم.[11] كثير من الأفراد غير المشخصين الذين يعتبرون أنفسهم غير متماثلين للأعراض هم في الواقع ليسوا كذلك، لكنهم اعتادوا على العيش في حالة صحية مزمنة. في الواقع، بعد البدء في اتباع نظام غذائي خالٍ من الغلوتين ويصبح التحسن اللاحق واضحًا، يتمكن هؤلاء الأفراد غالبًا من التذكر بأثر رجعي والتعرف على الأعراض السابقة لمرضهم غير المعالج الذي تجاهلوه عن طريق الخطأ.[12][13]
الجهاز الهضمي
الإسهال الذي يتسم بمرض الاضطرابات الهضمية هو مزمن، شاحب، ذو حجم كبير، ورائحة سيئة بشكل غير طبيعي. قد يكون هناك ألم في البطن، والتشنج ، والانتفاخ (يُعتقد أنه ناتج عن إنتاج تخمير غازات الأمعاء)، وتقرحات الفم.[14] مع زيادة تلف الأمعاء، قد تتطور درجة من عدم تحمل اللاكتوز.[9] في كثير من الأحيان، تعزى الأعراض إلى متلازمة القولون العصبي، فقط في وقت لاحق للاعتراف بمرض الاضطرابات الهضمية. في المجموعات السكانية للأشخاص الذين يعانون من أعراض القولون العصبي، يمكن إجراء تشخيص لمرض الاضطرابات الهضمية في حوالي 3.3٪ من الحالات، أو 4x أكثر أحتمالية بشكل عام.[15] يوصى المعهد القومي للصحة والتميز السريري، والجمعية البريطانية لأمراض الجهاز الهضمي والكلية الأمريكية لأمراض الجهاز الهضمي بالكشف عنها لمرض الاضطرابات الهضمية، لكنه ذو فائدة غير واضحة في أمريكا الشمالية.[15][16] يؤدي مرض الاضطرابات الهضمية إلى زيادة خطر الإصابة بسرطان الغدد اللمفاوية والأورام اللمفاوية في الأمعاء الدقيقة (سرطان الغدد الليمفاوية المرتبط بالأمراض التائية المعوية أو سرطان الغدد الليمفاوية الأخرى غير هودجكين).[17] هذا الخطر أعلى أيضًا في الأقارب من الدرجة الأولى مثل الأشقاء والآباء والأطفال. ما إذا كان اتباع نظام غذائي خالٍ من الغلوتين أو إعادته إلى هذا الأساس أمر غير واضح.[18] قد يؤدي المرض الطويل الأمد وغير المعالج إلى مضاعفات أخرى، مثل التهاب الصائم التقرحي (تشكيل قرحة الأمعاء الدقيقة) والتضيق (الضيق نتيجة للتندب مع انسداد الأمعاء).[19]
سوء الأمتصاص ذات الصلة
التغييرات في الأمعاء تجعلها أقل قدرة على امتصاص العناصر الغذائية والمعادن والفيتامينات الذائبة في الدهون A وD وE وK.[9][20]
1) عدم القدرة على امتصاص الكربوهيدرات والدهون قد يسبب فقدان الوزن أو(الفشل في النمو/ توقف النمو عند الأطفال) والتعب أو نقص الطاقة.
2) قد يتطور فقر الدم بعدة طرق: قد يؤدي سوء امتصاص الحديد إلى فقر الدم الناجم عن نقص الحديد، وقد يؤدي سوء امتصاص حمض الفوليك وفيتامين بي 12 إلى فقر الدم الضخم.
3) قد يسبب سوء امتصاص الكالسيوم وفيتامين د (وفرط نشاط الغدة الدرقية الثانوي التعويضي) هشاشة العظام (انخفاض محتوى المعادن في العظام) وضعف العظام وخطر هشاشة الكسور.
4) إن سوء امتصاص السيلينيوم في مرض الاضطرابات الهضمية، مع انخفاض نسبة السيلينيوم في العديد من الأطعمة الخالية من الغلوتين، يمثل خطرًا لنقص السيلينيوم.[21]
5) كما يرتبط نقص النحاس والزنك بمرض الاضطرابات الهضمية.[22]
6) وهناك نسبة صغيرة منها تخثر غير طبيعي بسبب نقص فيتامين K وتعرض قليلا لخطر النزيف غير الطبيعي.
الفسيولوجيا المرضية
يبدو أن مرض الاضطرابات الهضمية متعدد العوامل، حيث إن أكثر من عامل وراثي يمكن أن يتسبب في هذا المرض، وأن أكثر من عامل ضروري للمرض لكي يظهر في شخص ما. تقريبا كل الناس (95٪) يعانون من مرض الاضطرابات الهضمية لديهم إما أليل HLA-DQ2 البديل أو (الأقل شيوعًا) أليل HLA-DQ8 [11][23]ومع ذلك، فقد ورث حوالي 20-30٪ من الناس الذين يعانون من مرض الاضطرابات الهضمية أيضا أي من هذه الأليلات.[24] هذا يشير إلى أن هناك حاجة إلى عوامل إضافية لمرض الاضطرابات الهضمية لتطوير. هذا هو خطر أليل HLA المهدد، هو ضروري ولكنه غير كافٍ لتطوير مرض الاضطرابات الهضمية. علاوة على ذلك، حوالي 5٪ من أولئك الذين يصابون بمرض الاضطرابات الهضمية ليس لديهم أليلات HLA-DQ2 أو HLA-DQ8 نموذجية (انظر أدناه).[11]
عوامل جينية
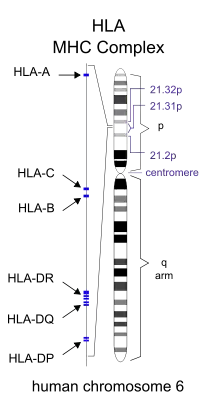
الغالبية العظمى من المرضى يحملون إحدى نوعي جينات التوافق الجيني HLA DQ2 والموجود على الذراع القصير للكروموسوم (الصبغي) السادس. التوافق الجيني HLA DQ2 له سبعة أنواع (DQ2 وDQ4 حتى DQ9) ويوجد لدى المصابين بداء بطني عادة إما نوع DQ2 أو DQ8، تزيد هذه الجينات من عدد المستقبلات التي ترتبط ببروتين الغليادين مما يزيد من قوة تنشيط الخلايا اللمفاوية خلية تائية وبالتالي تفعيل الجهاز المناعي ضد الخلايا المبطنة للأمعاء.[25][26]
برولامينات
غالبية البروتينات الموجودة في الغذاء والمسؤولة عن داء بطني هي من فئة البرولامينات، وهي بروتينات غنية بأحماض البرولين والغلوتامين الأمينية، يعتبر الغليادين من البرولامينات وهو بروتين سكري أيضاً. تتميز البرولامينات بذائبيتها في الكحول وقدرتها على مقاومة تأثير أنزيمات الببتيديز (محطم البروتين) والبروتياز المسؤولين عن تحطيم البروتينات الغذائية.
تقوم بروتينات الغليادين بالتأثير على نقاط الالتحام الموجودة بين خلايا بطانة الأمعاء الدقيقة مما يسهل دخول جزيئات أكبر إلى داخل الأنسجة المعوية ويسبب وصول البرولامينات والببتيدات المحتوية على الغليادين إلى مرمى الجهاز المناعي مسببة رد فعل مناعي.[27]
أنزيم الترانس أمينيز (ناقلات الأمين)
وجد لدى تشريح المصابين بداء بطني نسب عالية من الأجسام المضادة لأنزيم الترانس أمينيز [28]، ويشكل هذا التفاعل رواسب تظهر في عدة أمراض مناعية ولدى بعض المصابين بفقر الدم وسوء الامتصاص.
سوء الامتصاص وضمور الزغب المعوي
يؤدي رد الفعل المناعي الناتج عن مهاجمة الخلايا اللمفاوية خلية تائية لبطانة الأمعاء الدقيقة مسببة تهديم البنية الهندسية للزغب المعوي ومحدثة ترققاً في جدار الأمعاء، وهذا ما يؤدي إلى اصابة المريض بسوء الامتصاص وخاصة امتصاص فيتامينات (أ) و(د) و(هـ) و(ك)، يحدث في كثير من الحالات أيضاً سوء امتصاص سكر اللاكتوز الموجود في منتجات الحليب.
التشخيص
كثيرة هي الطرق التي يتم فيها تشخيص داء بطني، وعادة ما تلعب الأعراض السريرية دوراً هاماً في تحديد نوع الفحص المخبري أو الأشعاعي أو الإجراءات المختارة للتشخيص، من المهم الإشارة إلى أن كل التحاليل تصبح بلا قيمة في حال كان المريض بالأساس متبعاً لحمية غذائية خالية من الحبوب أو بروتين الغليادين لأن الضرر المعوي الناتج عن داء بطني قد يشفى خلال أسابيع من بدء الحمية وتنحسر تراكيز الأجسام المضادة خلال شهور قليلة.
يتم من أجل المرضى المحميين غذائياً إعادة ادخال مادة الغليادين من خلال إضافة 10 جرامات أو قطعتي خبز لحمية المريض لمدة 2-6 أسابيع وبعدها يعاد إجراء التحاليل المخبرية.
اختبار الدم

اختبارات الدم المصلية هي خط البحث الأول المطلوب لإجراء تشخيص لمرض الاضطرابات الهضمية. ترتبط حساسيتها بدرجة الآفات النسيجية. الأشخاص الذين يعانون من أضرار طفيفة في الأمعاء الدقيقة قد تكون لديهم نتائج مصلية، لذلك غالباً ما يتم تفويت مرضى الاضطرابات الهضمية. في المرضى الذين يعانون من ضمور الزغب، يمكن للأجسام المضادة المضادة للالتهاب الداخلي من نوع الغلوبولين المناعي (IgA) اكتشاف مرض الاضطرابات الهضمية بحساسية وخصوصية 90٪ و 99٪، على التوالي.[29] تم الإبلاغ في البداية أن الأمصال المضادة للأجسام المضادة للغلوتامين لديها حساسية أعلى (99٪) وخصوصية (>90٪). ومع ذلك، يُعتقد الآن أن لها خصائص مشابهة للأجسام المضادة للبطانة الداخلية.[29] تتمتع كل من الأجسام المضادة للغلوتامين وanti-endomysial بحساسية عالية لتشخيص الأشخاص الذين يعانون من أعراض كلاسيكية وضمور زغبي كامل، لكنهم لا يتواجدون إلا في 30-89٪ من الحالات المصابة بضمور زغبي جزئي وفي أقل من 50٪ من الأشخاص الذين لديهم آفات مخاطية طفيفة (كثرة الخلايا اللمفاوية الاثنا عشر) مع الزغب الطبيعي.[30][31] يعدل نسيج الغلوتين من الأنسجة الببتيد الغلوتين إلى شكل قد يحفز جهاز المناعة بشكل أكثر فعالية.[32] يتم تعديل هذه الببتيدات عن طريق tTG بطريقتين، نزع الأمين أو نقل الأمين تعتمد المقايسات الحديثة المضادة لـ tTG على بروتين مؤتلف من البشر كمولد الضد.[33] يجب إجراء اختبار tTG أولاً لأنه اختبار أسهل في الأداء. نتيجة ملتبسة على اختبار tTG يجب أن تتبعها أجسام مضادة مضادة للبطانة الداخلية.[34]
الكشف عن القابلية الجينية
كما ذكر سابقاً يوجد لدى المصابين بداء بطني عادة إما نوع DQ2 أو DQ8 من جين القابية الجينية (بالإنجليزية: HLA DQ)، تبلغ حساسية HLA DQ2 94% ودقته النوعية 74%، وبالنسبة ل HLA DQ8 تبلغ حساسيته 12% أما دقته النوعية فتبلغ 84%.
التنظير المعوي
التنظير العلوي للجهاز الهضمي مع أخذ الخزعات النسيجية هو حجر الأساس في تشخيص داء بطني، يجب الوصول إلى المعي الإثني عشري والمعي الصائم حتى يكون التنظير مجدياً، كثير من الخزعات المأخوذة من مرضى داء بطني قد تبدو سليمة ولذا يجب أخذ عدة عينات نسيجية من مناطق مختلفة حتى يكون التنظير دقيقاً ومثمراً.
تصنيف مارش
يعتمد تصنيف مارش الباثولوجي لتحديد مدى حدة تأثر الأمعاء الدقيقة بداء بطني، مراحل تصنيف مارش الخمسة هي:
- المرحلة 0: أغشية مخاطية طبيعية.
- المرحلة 1: ازدياد عدد الخلايا اللمفاوية في النسيج الطلائي للأمعاء وغالبا ما يكون العدد أكثر من 20 خلية لمفاوية لكل 100 خلية معوية.
- المرحلة 2: تزايد خبايا ليبركون في جدار الأمعاء..
- المرحلة 3: ضمور زغابي معوي جزئي أو كلي.
- المرحلة 4: نقص تنسج البنية المعوية.
تم تعديل تصنيف مارش، الذي تم تقديمه في عام 1992، في عام 1999 إلى ست مراحل، حيث تم تقسيم المرحلة السابقة 3 في ثلاث محطات فرعية.[35] أظهرت دراسات أخرى أن هذا النظام لم يكن دائمًا موثوقًا به وأن التغييرات التي لوحظت في مرض الاضطرابات الهضمية يمكن وصفها في واحدة من ثلاث مراحل: [9][36]
ويمثل تسلل الخلايا اللمفاوية مع مظهر الزغب العادي. B1 تصف ضمور الزغب الجزئي؛ و B2 تصف ضمور الزغب الكامل
التغييرات الكلاسيكية تحسن أو تعكس بعد إزالة الغلوتين من النظام الغذائي. ومع ذلك، فإن معظم الإرشادات لا توصي بتكرار الخزعة ما لم يكن هناك تحسن في الأعراض في النظام الغذائي.[19][37] في بعض الحالات، قد يتم إجراء تحدي متعمد للغلوتين، يتبعه خزعة، لتأكيد أو رفض التشخيص. تشير الخزعة الطبيعية والأمصال الطبيعية بعد التحدي إلى أن التشخيص قد يكون غير صحيح.[19] في مرض الاضطرابات الهضمية غير المعالج، يكون ضمور الزغب أكثر شيوعًا في الأطفال الذين تقل أعمارهم عن ثلاث سنوات، ولكن في الأطفال الأكبر سناً والبالغين، من الشائع العثور على آفات معوية بسيطة (لمفانيا الاثنا عشر) مع الزغابات المعوية الطبيعية.[38][39] عادة ما تتحسن الحالة خلال2-6 أسابيع من إزالة بروتين الغلوتين من الطعام وينصح بإعادة أخذ وفحص الخزعات النسيجية بعد 4-6 شهور من بداية العلاج.
فحوصات أخرى
من الفحوص الأخرى المهمة لنفي التشخيصات الأخرى وقياس مدى حدة وتأثير الأعراض الجانبية كسوء الامتصاص ما يلي:
- تعداد الدم الكامل.
- تراكيز الشوارد في الدم
- فحص وظائف الكلى
- فحص وظائف الكبد
- تركيز فيتامين (ب 12) في الدم
- تركيز حمض الفوليك في الدم
- فحص سرعة تخثر الدم
العلاج
الحمية الغذائية
المحتوي الرئيسي: نظام غذائي خال من الغلوتين
في الوقت الحاضر، فإن العلاج الفعال الوحيد هو اتباع نظام غذائي خال من الغلوتين مدى الحياة.[40] لا يوجد دواء يمنع الضرر أو يمنع الجسم من مهاجمة الأمعاء عند وجود الغلوتين. يساعد التقيد الصارم بالنظام الغذائي على شفاء الأمعاء، مما يؤدي إلى حل جميع الأعراض في معظم الحالات، واعتمادًا على الوقت الذي يبدأ فيه النظام الغذائي، يمكن أيضًا القضاء على خطر الإصابة بهشاشة العظام والسرطان المعوي وفي بعض الحالات العقم.[41] النظام الغذائي يمكن أن تكون مرهقة. عدم الامتثال للنظام الغذائي قد يسبب الانتكاس.
يُطلب بشكل عام مدخلات أخصائي التغذية للتأكد من إدراك الشخص للأطعمة التي تحتوي على الغلوتين والأطعمة الآمنة وكيفية اتباع نظام غذائي متوازن على الرغم من القيود. في العديد من البلدان، تتوفر المنتجات الخالية من الغلوتين بوصفة طبية وقد يتم تعويضها عن طريق خطط التأمين الصحي. المنتجات الخالية من الغلوتين عادة ما تكون أكثر تكلفة وأصعب من الأطعمة الشائعة التي تحتوي على الغلوتين.[42] نظرًا لأن المنتجات الجاهزة تحتوي غالبًا على آثار الغلوتين، فقد تجد بعض الألفيات أنه من الضروري الطهي من الصفر.[43]
يستخدم المصطلح "خالٍ من الغلوتين" عمومًا للإشارة إلى مستوى غير ضار مفترض من الغلوتين بدلاً من الغياب التام.[44] المستوى الدقيق الذي يكون فيه الغلوتين غير ضار غير مؤكد ومثير للجدل. خلصت مراجعة منهجية حديثة مبدئيًا إلى أن استهلاك أقل من 10 ملغ من الغلوتين يوميًا من غير المرجح أن يسبب تشوهات نسيجية، على الرغم من أنه لاحظ أنه لم يتم إجراء سوى عدد قليل من الدراسات الموثوقة.[44] تنظيم التسمية "خالية من الغلوتين" يختلف. في الاتحاد الأوروبي، أصدرت المفوضية الأوروبية لوائح في عام 2009 تقصر استخدام الملصقات "الخالية من الغلوتين" للمنتجات الغذائية على تلك التي تحتوي على أقل من 20 ملغم/كغم من الغلوتين، و "الملصقات منخفضة الغلوتين" لمن لديهم أقل من 100 ملغم/كغم. في الولايات المتحدة، أصدرت إدارة الأغذية والعقاقير لوائح في 2013 تقصر استخدام الملصقات "الخالية من الغلوتين" للمنتجات الغذائية على تلك التي تحتوي على أقل من 20 جزء في المليون من الغلوتين. [45][46][47] يسمح معيار Codex Alimentarius الدولي الحالي بـ 20 جزء في المليون من الغلوتين فيما يسمى الأطعمة "الخالية من الجلوتين".[48] العديد من المنظمات، مثل منظمة شهادة الغلوتين الحرة (GFCO)، وجمعية Celiac Sprue، والمؤسسة الوطنية للتوعية الاضطرابات الهضمية (NFCA)، تصدق أيضًا المنتجات والشركات على أنها خالية من الغلوتين.[49]
النظام الغذائي الخالي من الغلوتين يحسن نوعية الحياة المتعلقة بالرعاية الصحية، والالتزام الصارم بالنظام الغذائي يعطي فائدة أكبر من الالتزام غير الكامل. ومع ذلك، فإن اتباع نظام غذائي خالٍ من الغلوتين لا يؤدي إلى تطبيع نوعية الحياة تمامًا.[50]
علاج حراري
بين 0.3٪ و 10٪ من الناس يعانون من مرض حراري، مما يعني أن لديهم ضمور زغبي مستمر في نظام غذائي خال من الغلوتين على الرغم من عدم التعرض للجلوتين لأكثر من 12 شهرا.[51] ومع ذلك، فإن التعرض غير المقصود للغلوتين هو السبب الرئيسي لضمور الزغابات المستمر، ويجب استبعاده قبل إجراء تشخيص لمرض الحراريات.[51] غالبًا ما يعتقد الأشخاص الذين يعانون من سوء التعليم الأساسي وفهم النظام الغذائي الخالي من الغلوتين أنهم يتبعون النظام الغذائي بدقة، لكنهم يرتكبون أخطاء منتظمة. [52][51][53] أيضا، نقص الأعراض ليس مؤشرا موثوقا على الانتعاش المعوي.[51] إذا تم القضاء على أسباب بديلة لضمور الزغابات، فيمكن اعتبار المنشطات أو مثبطات المناعة (مثل الآزويثوبرين) في هذا السيناريو.[19]
لا ينبغي الخلط بين مرض الاضطرابات الهضمية الحرارية واستمرار الأعراض على الرغم من انسحاب الغلوتين[51] الناجم عن حالات عابرة ناجمة عن الضرر المعوي،[54][55][56] التي تعود أو تتحسن عمومًا بعد عدة أشهر من بدء خالية من الغلوتين الحمية الغذائية،[57][58] مثل فرط نمو البكتيريا المعوية الصغيرة، عدم تحمل اللاكتوز، الفركتوز،[59] السكروز ،[54] وسوء الامتصاص السوربيتول[55]، قصور البنكرياس الخارجي،[60][51] والتهاب القولون المجهري [51] من بين أمور أخرى.
حالات عصية
وجد لدى عدد بسيط من مرضى داء بطني أن الحالة المرضية لا تتحسن بعد اتباع الحمية الغذائية، وقد يعزى ذلك لطول استمرارية المرض الأمر الذي يجعل التضرر الحاصل في الأمعاء الدقيقة بالغاً وغير قابل للعكس والعلاج.
علاجات تجريبية
توجد مجموعة من العلاجات لداء بطني ما زالت في طور التجربة وما زلنا ننتظر نتائج الدراسات السريرية فيها، من هذه العلاجات:
- تناول الحبوب المعدلة وراثياً والخالية من الغلوتين، إلا أن مشكلة تواجه هذا النوع من الحبوب تكمن في انخفاض جودة العجين المصنع منه لغياب هذه المادة.
- إضافة بعض الأنزيمات الهاضمة للغلوتين إلى الحمية الغذائية وذلك لتسهيل هضم هذه المادة وتمكين المريض من تناول الأغذية المحتوية على الغلوتين.[61]
- تثبيط عمل بروتين الزولين الذي يزيد من نفاذية الأغشية المخاطية في الأمعاء مما يقلل من حجم الالتهاب الناتج عن عبور البرولامينات إلى داخل جدار الأمعاء وحدوث رد الفعل الالتهابي فيها.[62]
علم الأوبئة
تؤثر أمراض الاضطرابات الهضمية على مستوى العالم بين شخص واحد من بين كل 100 شخص و 1 من كل 170 شخص.[63][64] ومع ذلك، تختلف الأسعار بين مناطق مختلفة من العالم من أقل من 1 في 300 إلى ما يصل إلى 1 في 40.[63] في الولايات المتحدة، يُعتقد أنه يؤثر على ما بين 1 في 1750 (يُعرف باسم المرض السريري بما في ذلك التهاب الجلد الحلئي مع أعراض محدودة في الجهاز الهضمي) إلى 1 في 105 (يُعرف بوجود IgA TG في المتبرعين بالدم).[65] بسبب علامات وأعراض متغيرة، يعتقد أن حوالي 85٪ من الأشخاص المصابين لم يتم تشخيصهم.[66] النسبة المئوية للأشخاص المصابين بمرض مشخص سريرياً (الأعراض التي تحث على إجراء الاختبارات التشخيصية) تتراوح بين 0.05 و 0.27٪ في العديد من الدراسات. ومع ذلك، تشير الدراسات السكانية من أجزاء من أوروبا والهند وأمريكا الجنوبية وأستراليا والولايات المتحدة الأمريكية (باستخدام الأمصال والخزعة) إلى أن النسبة المئوية للأشخاص المصابين بالمرض قد تتراوح ما بين 0.33 و 1.06٪ في الأطفال (ولكن 5.66٪ في دراسة واحدة لـ أطفال الشعب الصحراوي المهيوس[67] و 0.18-1.2٪ في البالغين.[32] من بين أفراد مجتمع الرعاية الأولية الذين يبلغون عن أعراض الجهاز الهضمي، فإن معدل الإصابة بمرض الاضطرابات الهضمية هو حوالي 3٪.[29] في أستراليا، يصاب شخص واحد من كل 70 شخصًا بالمرض.[68] النسبة بين المتبرعين بالدم البالغين في إيران وإسرائيل وسوريا وتركيا هي 0.60٪، 0.64، 1.61٪ و 1.15٪، على التوالي.[18] نادراً ما يتم تشخيص الأشخاص من أصل أفريقي وياباني وصيني؛[69] وهذا يعكس انتشارًا أقل بكثير لعوامل الخطر الجيني، مثل HLA-B8.[69] يبدو أن الناس من أصل هندي لديهم مخاطر مماثلة لتلك التي من أصل غرب القوقاز.[18] تشير الدراسات السكانية أيضًا إلى أن نسبة كبيرة من الأورام الشائكة تبقى غير مشخصة؛ ويرجع ذلك، جزئيًا، إلى أن العديد من الأطباء غير مألوفين بالحالة وأيضًا بسبب حقيقة أنه قد يكون بدون أعراض.[70] يعد مرض الاضطرابات الهضمية أكثر شيوعًا عند النساء منه في الرجال.[71] كشفت دراسة كبيرة متعددة المراكز في الولايات المتحدة عن انتشار بنسبة 0.75٪ في المجموعات غير المعرضة للخطر، حيث ارتفعت إلى 1.8٪ في الأشخاص الذين يعانون من أعراض، و 2.6٪ في الأقارب من الدرجة الثانية (مثل الأجداد، العمة أو العم، الأحفاد، وما إلى ذلك) من شخص مصاب بمرض الاضطرابات الهضمية و 4.5٪ في الأقارب من الدرجة الأولى (الأشقاء أو الآباء أو الأطفال).[18] هذا الملف مشابه للانتشار في أوروبا.[18] تشمل الفئات السكانية الأخرى الأكثر عرضة لخطر الإصابة بمرض الاضطرابات الهضمية، حيث تتراوح معدلات الانتشار بين 5٪ إلى 10٪، الأفراد المصابين بمتلازمات داون وتيرنر، ومرض السكري من النوع 1، وأمراض الغدة الدرقية المناعي الذاتي، بما في ذلك كل من فرط نشاط الغدة الدرقية (فرط نشاط الغدة الدرقية) ونقص نشاط الغدة الدرقية (قصور الغدة الدرقية) .[72]
تاريخيا، كان يعتقد أن مرض الاضطرابات الهضمية أمر نادر الحدوث، مع انتشار حوالي 0.02٪.[72] سبب الزيادات الأخيرة في عدد الحالات المبلغ عنها غير واضح.[64] قد يكون ذلك جزئيًا على الأقل بسبب التغييرات في الممارسة التشخيصية.[73] يبدو أن هناك أيضًا زيادة حقيقية بمقدار 4.5 أضعاف تقريبًا والتي قد تكون بسبب التعرض الأقل للبكتيريا ومسببات الأمراض الأخرى في البيئات الغربية.[64]
انظر أيضًا
مراجع
- معرف أنطولوجية المرض: http://www.disease-ontology.org/?id=DOID:10608 — تاريخ الاطلاع: 30 نوفمبر 2020 — الرخصة: CC0
- "Celiac Disease". NIDDKD. June 2015. مؤرشف من الأصل في 16 يونيو 2016. اطلع عليه بتاريخ 17 مارس 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Fasano, Alessio (2005-04-01). "Clinical presentation of celiac disease in the pediatric population". Gastroenterology (باللغة الإنجليزية). 128 (4): S68–S73. doi:10.1053/j.gastro.2005.02.015. ISSN 0016-5085. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Husby, S.; Koletzko, S.; Korponay-Szabó, I. R.; Mearin, M. L.; Phillips, A.; Shamir, R.; Troncone, R.; Giersiepen, K.; Branski, D. (2012-1). "European Society for Pediatric Gastroenterology, Hepatology, and Nutrition Guidelines for the Diagnosis of Coeliac Disease". Journal of Pediatric Gastroenterology and Nutrition (باللغة الإنجليزية). 54 (1): 136–160. doi:10.1097/MPG.0b013e31821a23d0. ISSN 0277-2116. PMID 22197856. مؤرشف من الأصل في 27 سبتمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Newnham, Evan D. (2017). "Coeliac disease in the 21st century: paradigm shifts in the modern age". Journal of Gastroenterology and Hepatology (باللغة الإنجليزية). 32 (S1): 82–85. doi:10.1111/jgh.13704. ISSN 1440-1746. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Tonutti, Elio; Bizzaro, Nicola (2014-04-01). "Diagnosis and classification of celiac disease and gluten sensitivity". Autoimmunity Reviews. 13 (4): 472–476. doi:10.1016/j.autrev.2014.01.043. ISSN 1568-9972. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ciccocioppo, Rachele; Kruzliak, Peter; Cangemi, Giuseppina C.; Pohanka, Miroslav; Betti, Elena; Lauret, Eugenia; Rodrigo, Luis (2015-10-22). "The Spectrum of Differences between Childhood and Adulthood Celiac Disease". Nutrients. 7 (10): 8733–8751. doi:10.3390/nu7105426. ISSN 2072-6643. PMID 26506381. مؤرشف من الأصل في 10 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Schuppan, Detlef; Zimmer, Klaus-Peter (2013-12). "The Diagnosis and Treatment of Celiac Disease". Deutsches Ärzteblatt International. 110 (49): 835–846. doi:10.3238/arztebl.2013.0835. ISSN 1866-0452. PMID 24355936. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Sabatino, Antonio Di; Corazza, Gino Roberto (2009-04-25). "Coeliac disease". The Lancet (باللغة الإنجليزية). 373 (9673): 1480–1493. doi:10.1016/S0140-6736(09)60254-3. ISSN 0140-6736. PMID 19394538. مؤرشف من الأصل في 2 نوفمبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Vriezinga, Sabine L.; Schweizer, Joachim J.; Koning, Frits; Mearin, M. Luisa (2015-09). "Coeliac disease and gluten-related disorders in childhood". Nature Reviews Gastroenterology & Hepatology (باللغة الإنجليزية). 12 (9): 527–536. doi:10.1038/nrgastro.2015.98. ISSN 1759-5053. مؤرشف من الأصل في 18 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Heel, D. A. van; West, J. (2006-07-01). "Recent advances in coeliac disease". Gut (باللغة الإنجليزية). 55 (7): 1037–1046. doi:10.1136/gut.2005.075119. ISSN 0017-5749. PMID 16766754. مؤرشف من الأصل في 15 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ludvigsson, Jonas F; Card, Tim; Ciclitira, Paul J; Swift, Gillian L; Nasr, Ikram; Sanders, David S; Ciacci, Carolina (2014-12-09). "Support for patients with celiac disease: A literature review". United European Gastroenterology Journal (باللغة الإنجليزية). 3 (2): 146–159. doi:10.1177/2050640614562599. ISSN 2050-6406. PMID 25922674. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Lionetti, Elena; Gatti, Simona; Pulvirenti, Alfredo; Catassi, Carlo (2015-06-01). "Celiac disease from a global perspective". Best Practice & Research Clinical Gastroenterology. 29 (3): 365–379. doi:10.1016/j.bpg.2015.05.004. ISSN 1521-6918. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ferguson, R; Basu, M K; Asquith, P; Cooke, W T (1976-01-03). "Jejunal mucosal abnormalities in patients with recurrent aphthous ulceration". British Medical Journal. 1 (6000): 11–13. ISSN 0007-1447. PMID 1247715. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Irvine, Andrew; Chey, William; Ford, Alexander (2017-1). "Screening for Celiac Disease in Irritable Bowel Syndrome: An Updated Systematic Review and Meta-analysis". American Journal of Gastroenterology (باللغة الإنجليزية). 112 (1): 65–76. doi:10.1038/ajg.2016.466. ISSN 0002-9270. PMID 27753436. مؤرشف من الأصل في 27 سبتمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - "Overview | Irritable bowel syndrome in adults: diagnosis and management | Guidance | NICE". www.nice.org.uk. مؤرشف من الأصل في 28 يونيو 2019. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Caio, Giacomo; Volta, Umberto; Sapone, Anna; Leffler, Daniel A.; De Giorgio, Roberto; Catassi, Carlo; Fasano, Alessio (2019-07-23). "Celiac disease: a comprehensive current review". BMC Medicine. 17 (1): 142. doi:10.1186/s12916-019-1380-z. ISSN 1741-7015. PMID 31331324. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gujral, Naiyana; Freeman, Hugh J.; Thomson, Alan BR (2012-11-14). "Celiac disease: Prevalence, diagnosis, pathogenesis and treatment". World Journal of Gastroenterology (باللغة الإنجليزية). 18 (42): 6036–6059. doi:10.3748/wjg.v18.i42.6036. PMID 23155333. مؤرشف من الأصل في 30 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "American Gastroenterological Association medical position statement: Celiac sprue". Gastroenterology (باللغة الإنجليزية). 120 (6): 1522–1525. 2001-05-01. doi:10.1053/gast.2001.24055. ISSN 0016-5085. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Presutti, R. John; Cangemi, John R.; Cassidy, Harvey D.; Hill, D. Ashley (2007-12-15). "Celiac Disease". American Family Physician (باللغة الإنجليزية). 76 (12): 1795–1802. ISSN 0002-838X. مؤرشف من الأصل في 3 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Michelle Maria (2013-10-17). Clinical Gastroenterology. New York, NY: Springer New York. صفحات 137–159. ISBN 9781461485599. مؤرشف من الأصل في 17 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Michelle Maria (2014). S. Devi; Mullin, Gerard E. (المحررون). Celiac Disease. (باللغة الإنجليزية). New York, NY: Springer New York. صفحات 137–159. doi:10.1007/978-1-4614-8560-5_11. ISBN 9781461485605. مؤرشف من الأصل في 17 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Longmore, Murray; Wilkinson, Ian; Baldwin, Andrew; Wallin, Elizabeth (2014-01). "Oxford Handbook of Clinical Medicine". Oxford Medicine Online. doi:10.1093/med/9780199609628.001.0001. مؤرشف من الأصل في 27 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Hadithi, Muhammed (2007-09-04). "Accuracy of Serologic Tests and HLA-DQ Typing for Diagnosing Celiac Disease". Annals of Internal Medicine (باللغة الإنجليزية). 147 (5): 294. doi:10.7326/0003-4819-147-5-200709040-00003. ISSN 0003-4819. مؤرشف من الأصل في 27 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Jores RD, Frau F, Cucca F; et al. (2007). "HLA-DQB1*0201 homozygosis predisposes to severe intestinal damage in celiac disease". Scand. J. Gastroenterol. 42 (1): 48–53. doi:10.1080/00365520600789859. PMID 17190762. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Hadithi M, von Blomberg BM, Crusius JB; et al. (2007). "Accuracy of serologic tests and HLA-DQ typing for diagnosing celiac disease". Ann. Intern. Med. 147 (5): 294–302. PMID 17785484. مؤرشف من الأصل في 21 أغسطس 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Green PH, Cellier C (2007). "Celiac disease". N. Engl. J. Med. 357 (17): 1731–43. doi:10.1056/NEJMra071600. PMID 17960014. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dieterich W, Ehnis T, Bauer M, Donner P, Volta U, Riecken E, Schuppan D (1997). "Identification of tissue transglutaminase as the autoantigen of celiac disease". Nat Med. 3 (7): 797–801. doi:10.1038/nm0797-797. PMID 9212111. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Windt, Daniëlle A. W. M. van der; Jellema, Petra; Mulder, Chris J.; Kneepkens, C. M. Frank; Horst, Henriëtte E. van der (2010-05-05). "Diagnostic Testing for Celiac Disease Among Patients With Abdominal Symptoms: A Systematic Review". JAMA (باللغة الإنجليزية). 303 (17): 1738–1746. doi:10.1001/jama.2010.549. ISSN 0098-7484. مؤرشف من الأصل في 30 أغسطس 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Lewis, N. R.; Scott, B. B. (2006). "Systematic review: the use of serology to exclude or diagnose coeliac disease (a comparison of the endomysial and tissue transglutaminase antibody tests)". Alimentary Pharmacology & Therapeutics (باللغة الإنجليزية). 24 (1): 47–54. doi:10.1111/j.1365-2036.2006.02967.x. ISSN 1365-2036. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Rostom, Alaa; Murray, Joseph A.; Kagnoff, Martin F. (2006-12-01). "American Gastroenterological Association (AGA) Institute Technical Review on the Diagnosis and Management of Celiac Disease". Gastroenterology (باللغة الإنجليزية). 131 (6): 1981–2002. doi:10.1053/j.gastro.2006.10.004. ISSN 0016-5085. PMID 17087937. مؤرشف من الأصل في 10 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - van Heel, D A; West, J (2006-7). "Recent advances in coeliac disease". Gut. 55 (7): 1037–1046. doi:10.1136/gut.2005.075119. ISSN 0017-5749. PMID 16766754. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Sblattero, D.; Berti, I.; Trevisiol, C.; Marzari, R.; Tommasini, A.; Bradbury, A.; Fasano, A.; Ventura, A.; Not, T. (2000-05). "Human recombinant tissue transglutaminase ELISA: an innovative diagnostic assay for celiac disease". The American Journal of Gastroenterology. 95 (5): 1253–1257. doi:10.1111/j.1572-0241.2000.02018.x. ISSN 0002-9270. مؤرشف من الأصل في 27 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - "Coeliac disease: recognition and assessment | Guidance | NICE". www.nice.org.uk. مؤرشف من الأصل في 25 يونيو 2018. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Oberhuber, Georg; Granditsch, Gerhard; Vogelsang, Harald (1999-10). "The histopathology of coeliac disease: time for a standardized report scheme for pathologists". European Journal of Gastroenterology & Hepatology (باللغة الإنجليزية). 11 (10). doi:10.1097/00042737-199910000-00019. ISSN 0954-691X. PMID 10524652. مؤرشف من الأصل في 27 سبتمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Corazza, Gino Roberto; Villanacci, Vincenzo; Zambelli, Claudia; Milione, Massimo; Luinetti, Ombretta; Vindigni, Carla; Chioda, Caterina; Albarello, Luca; Bartolini, Daniela (2007-07-01). "Comparison of the Interobserver Reproducibility With Different Histologic Criteria Used in Celiac Disease". Clinical Gastroenterology and Hepatology (باللغة الإنجليزية). 5 (7): 838–843. doi:10.1016/j.cgh.2007.03.019. ISSN 1542-3565. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Hill, Ivor; Dirks, Martha; Liptak, Gregory; Colletti, Richard; Fasano, Alessio; Guandalini, Stefano; Hoffenberg, Edward; Horvath, Karoly; Murray, Joseph (2005-1). "Guideline for the Diagnosis and Treatment of Celiac Disease in Children: Recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition". Journal of Pediatric Gastroenterology and Nutrition (باللغة الإنجليزية). 40 (1): 1–19. doi:10.1097/00005176-200501000-00001. ISSN 0277-2116. PMID 15625418. مؤرشف من الأصل في 27 سبتمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Vivas, Santiago; Vaquero, Luis; Rodríguez-Martín, Laura; Caminero, Alberto (2015-11-06). "Age-related differences in celiac disease: Specific characteristics of adult presentation". World Journal of Gastrointestinal Pharmacology and Therapeutics. 6 (4): 207–212. doi:10.4292/wjgpt.v6.i4.207. ISSN 2150-5349. PMID 26558154. مؤرشف من الأصل في 10 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Molina‐Infante, J.; Santolaria, S.; Sanders, D. S.; Fernández‐Bañares, F. (2015). "Systematic review: noncoeliac gluten sensitivity". Alimentary Pharmacology & Therapeutics (باللغة الإنجليزية). 41 (9): 807–820. doi:10.1111/apt.13155. ISSN 1365-2036. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Kupper, Cynthia (2005-04-01). "Dietary guidelines and implementation for celiac disease". Gastroenterology (باللغة الإنجليزية). 128 (4): S121–S127. doi:10.1053/j.gastro.2005.02.024. ISSN 0016-5085. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Treem, William (2004-10). "Emerging concepts in celiac disease". Current Opinion in Pediatrics (باللغة الإنجليزية). 16 (5): 552–559. doi:10.1097/01.mop.0000142347.74135.73. ISSN 1040-8703. PMID 15367850. مؤرشف من الأصل في 27 سبتمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Lee, A. R.; Ng, D. L.; Zivin, J.; Green, P. H. R. (2007). "Economic burden of a gluten-free diet". Journal of Human Nutrition and Dietetics (باللغة الإنجليزية). 20 (5): 423–430. doi:10.1111/j.1365-277X.2007.00763.x. ISSN 1365-277X. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Troncone, R.; Ivarsson, A.; Szajewska, H.; Mearin, M. L. (2008). "Review article: future research on coeliac disease – a position report from the European multistakeholder platform on coeliac disease (CDEUSSA)". Alimentary Pharmacology & Therapeutics (باللغة الإنجليزية). 27 (11): 1030–1043. doi:10.1111/j.1365-2036.2008.03668.x. ISSN 1365-2036. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Akobeng, A. K.; Thomas, A. G. (2008). "Systematic review: tolerable amount of gluten for people with coeliac disease". Alimentary Pharmacology & Therapeutics (باللغة الإنجليزية). 27 (11): 1044–1052. doi:10.1111/j.1365-2036.2008.03669.x. ISSN 1365-2036. مؤرشف من الأصل في 31 يوليو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Commissioner, Office of the (2019-02-09). "'Gluten-Free' Means What It Says". FDA (باللغة الإنجليزية). مؤرشف من الأصل في 26 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "uslaw.link". uslaw.link. مؤرشف من الأصل في 20 يناير 2020. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Federal Register Citation". Federal Register. مؤرشف من الأصل في 21 يناير 2019. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Official Standards List". web.archive.org. 2011-06-04. مؤرشف من الأصل في 6 أبريل 2020. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Jane; December 01, erson Updated; 2018. "What Gluten-Free Certification Means for Consumers". Verywell Fit (باللغة الإنجليزية). مؤرشف من الأصل في 5 أغسطس 2019. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة)CS1 maint: numeric names: قائمة المؤلفون (link) - Burger, Jordy P. W.; Brouwer, Bart de; IntHout, Joanna; Wahab, Peter J.; Tummers, Marcia; Drenth, Joost P. H. (2017-04-01). "Systematic review with meta-analysis: Dietary adherence influences normalization of health-related quality of life in coeliac disease". Clinical Nutrition (باللغة الإنجليزية). 36 (2): 399–406. doi:10.1016/j.clnu.2016.04.021. ISSN 0261-5614. PMID 27179800. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Woodward, Jeremy (2016-08-03). "Improving outcomes of refractory celiac disease – current and emerging treatment strategies". Clinical and Experimental Gastroenterology. 9: 225–236. doi:10.2147/CEG.S87200. ISSN 1178-7023. PMID 27536154. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - See, Jacalyn A.; Kaukinen, Katri; Makharia, Govind K.; Gibson, Peter R.; Murray, Joseph A. (2015-10). "Practical insights into gluten-free diets". Nature Reviews Gastroenterology & Hepatology (باللغة الإنجليزية). 12 (10): 580–591. doi:10.1038/nrgastro.2015.156. ISSN 1759-5053. مؤرشف من الأصل في 10 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Mulder, Chris J. J.; Wanrooij, R. L. J. van; Bakker, S. F.; Wierdsma, N.; Bouma, G. (2013). "Gluten-Free Diet in Gluten-Related Disorders". Digestive Diseases (باللغة الإنجليزية). 31 (1): 57–62. doi:10.1159/000347180. ISSN 0257-2753. PMID 23797124. مؤرشف من الأصل في 30 يونيو 2014. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Levy, Joseph; Bernstein, Leora; Silber, Nicole (2014-12-01). "Celiac Disease: An Immune Dysregulation Syndrome". Current Problems in Pediatric and Adolescent Health Care. 44 (11): 324–327. doi:10.1016/j.cppeds.2014.10.002. ISSN 1538-5442. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Montalto, M.; Gallo, A.; Ojetti, V.; Gasbarrini, A. (2013). "Fructose, trehalose and sorbitol malabsorption". European Review for Medical and Pharmacological Sciences. 17 Suppl 2: 26–29. ISSN 2284-0729. PMID 24443064. مؤرشف من الأصل في 14 ديسمبر 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Berni Canani, Roberto; Pezzella, Vincenza; Amoroso, Antonio; Cozzolino, Tommaso; Di Scala, Carmen; Passariello, Annalisa (2016-03-10). "Diagnosing and Treating Intolerance to Carbohydrates in Children". Nutrients. 8 (3). doi:10.3390/nu8030157. ISSN 2072-6643. PMID 26978392. مؤرشف من الأصل في 3 مارس 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - García‐Manzanares, Álvaro; Lucendo, Alfredo J. (2011). "Review: Nutritional and Dietary Aspects of Celiac Disease". Nutrition in Clinical Practice (باللغة الإنجليزية). 26 (2): 163–173. doi:10.1177/0884533611399773. ISSN 1941-2452. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Green, Peter HR; Jabri, Bana (2003-08-02). "Coeliac disease". The Lancet (باللغة الإنجليزية). 362 (9381): 383–391. doi:10.1016/S0140-6736(03)14027-5. ISSN 0140-6736. PMID 12907013. مؤرشف من الأصل في 2 نوفمبر 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Castillo, Natalia E.; Theethira, Thimmaiah G.; Leffler, Daniel A. (2015-2). "The present and the future in the diagnosis and management of celiac disease". Gastroenterology Report. 3 (1): 3–11. doi:10.1093/gastro/gou065. ISSN 2052-0034. PMID 25326000. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Leffler, Daniel A.; Green, Peter H. R.; Fasano, Alessio (2015-08-11). "Extraintestinal manifestations of coeliac disease". Nature Reviews Gastroenterology & Hepatology (باللغة الإنجليزية). 12 (10): 561–571. doi:10.1038/nrgastro.2015.131. ISSN 1759-5045. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Siegel M, Bethune M, Gass J, Ehren J, Xia J, Johannsen A, Stuge T, Gray G, Lee P, Khosla C (2006). "Rational design of combination enzyme therapy for celiac sprue". Chem Biol. 13 (6): 649–58. doi:10.1016/j.chembiol.2006.04.009. PMID 16793522. مؤرشف من الأصل في 18 أكتوبر 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Fasano A, Not T, Wang W, Uzzau S, Berti I, Tommasini A, Goldblum S (2000). "Zonulin, a newly discovered modulator of intestinal permeability, and its expression in coeliac disease". Lancet. 355 (9214): 1518–9. doi:10.1016/S0140-6736(00)02169-3. PMID 10801176. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Fasano, Alessio; Catassi, Carlo (2012-12-20). "Celiac Disease". New England Journal of Medicine. 367 (25): 2419–2426. doi:10.1056/NEJMcp1113994. ISSN 0028-4793. PMID 23252527. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Lebwohl, Benjamin; Ludvigsson, Jonas F; Green, Peter H R (2015-10-05). "Celiac disease and non-celiac gluten sensitivity". The BMJ. 351. doi:10.1136/bmj.h4347. ISSN 0959-8138. PMID 26438584. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Rewers, Marian (2005-04-01). "Epidemiology of celiac disease: What are the prevalence, incidence, and progression of celiac disease?". Gastroenterology (باللغة الإنجليزية). 128 (4): S47–S51. doi:10.1053/j.gastro.2005.02.030. ISSN 0016-5085. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Guandalini, Stefano; Assiri, Asaad (2014-03-01). "Celiac Disease: A Review". JAMA Pediatrics (باللغة الإنجليزية). 168 (3): 272–278. doi:10.1001/jamapediatrics.2013.3858. ISSN 2168-6203. مؤرشف من الأصل في 27 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Catassi, Carlo; Ratsch, IIse-Maria; Gandolfi, Lenora; Pratesi, Riccardo; Fabiani, Elisabetta; Asmar, Ramzi El; Frijia, Maria; Bearzi, Italo; Vizzoni, Luciano (1999-08-21). "Why is coeliac disease endemic in the people of the Sahara?". The Lancet (باللغة الإنجليزية). 354 (9179): 647–648. doi:10.1016/S0140-6736(99)02609-4. ISSN 0140-6736. PMID 10466670. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Coeliac Disease - Coeliac Australia". www.coeliac.org.au. مؤرشف من الأصل في 9 مارس 2018. اطلع عليه بتاريخ 02 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Houlston, R. S.; Ford, D. (1996-10-01). "Genetics of coeliac disease". QJM: An International Journal of Medicine (باللغة الإنجليزية). 89 (10): 737–744. doi:10.1093/qjmed/89.10.737. ISSN 1460-2725. مؤرشف من الأصل في 1 يونيو 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Zipser, Robert D; Farid, Mary; Baisch, Donald; Patel, Bhairavi; Patel, Devika (2005-7). "BRIEF REPORT: Physician Awareness of Celiac Disease". Journal of General Internal Medicine. 20 (7): 644–646. doi:10.1111/j.1525-1497.2005.0107.x. ISSN 0884-8734. PMID 16050861. مؤرشف من الأصل في 10 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Hischenhuber, C.; Crevel, R.; Jarry, B.; Mäki, M.; Moneret‐Vautrin, D. A.; Romano, A.; Troncone, R.; Ward, R. (2006). "Review article: safe amounts of gluten for patients with wheat allergy or coeliac disease". Alimentary Pharmacology & Therapeutics (باللغة الإنجليزية). 23 (5): 559–575. doi:10.1111/j.1365-2036.2006.02768.x. ISSN 1365-2036. مؤرشف من الأصل في 23 فبراير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Barker, Jennifer M.; Liu, Edwin (2008). "Celiac Disease: Pathophysiology, Clinical Manifestations and Associated Autoimmune Conditions". Advances in pediatrics. 55: 349–365. doi:10.1016/j.yapd.2008.07.001. ISSN 0065-3101. PMID 19048738. مؤرشف من الأصل في 20 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Leeds, John S.; Hopper, Andrew D.; Sanders, David S. (2008-12-01). "Coeliac disease". British Medical Bulletin (باللغة الإنجليزية). 88 (1): 157–170. doi:10.1093/bmb/ldn044. ISSN 0007-1420. مؤرشف من الأصل في 5 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة طب
- بوابة علم الأحياء
