كشف السرطان
يهدف كشف السرطان إلى التحري عن وجود السرطان قبل ظهور الأعراض. يمكن أن يشمل ذلك فحوصات الدم والبول واختبارات الحمض النووي وغيرها، أو التصوير الطبي.[1][2] يجب الموازنة بين فوائد الكشف من ناحية الوقاية من السرطان والكشف المبكر والمعالجة اللاحقة ضد أي أضرار.
| كشف السرطان | |
|---|---|
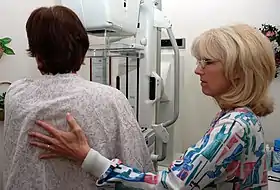 الكشف عن سرطان الثدي الكشف عن سرطان الثدي | |
| من أنواع | كشف |
يشمل الكشف الشامل، المعروف أيضًا باسم التحرّي الشامل أو كشف السكان، الكشف على كل شخص، وعادةً ما يتضمّن فئة عمرية محددة. يحدد الكشف الانتقائي أشخاص معروف أنهم أكثر عرضة للإصابة بالسرطان، مثل الأشخاص الذين لديهم سوابق عائلية للإصابة بالسرطان.[3]
يمكن أن يؤدي الكشف إلى نتائج إيجابية كاذبة وإجراءات باضعة لاحقة.[4] يمكن أن يؤدي الكشف أيضًا إلى نتائج سلبية كاذبة، إذ يُخفق في الكشف عن سرطان موجود. ينشأ الجدل عندما يكون من غير الواضح ما إذا كانت فوائد الكشف تفوق مخاطر إجراء الكشف نفسه، وأي اختبارات تشخيصية وعلاجات متابَعة.[5]
يجب أن تكون اختبارات الكشف فعالة وآمنة ومتحمّلة بشكل جيد مع معدلات منخفضة إلى حد ما من النتائج الإيجابية أو السلبية الكاذبة. إذا كُشف عن وجود علامات للسرطان، تُجرى اختبارات متابعة أكثر نوعيةً وباضعة للوصول إلى التشخيص. يمكن أن يؤدي كشف السرطان إلى الوقاية من السرطان والتشخيص المبكر. يمكن أن يؤدي التشخيص المبكر إلى معدلات أعلى للعلاج الناجح والعمر الطويل. ومع ذلك، يمكن أن يكون كشفًا زائفًا أيضًا نتيجة زيادته الوقت حتى الوفاة من خلال حدوث انحياز المهلة الزمنية أو تحيز الوقت.
المخاطر
يعد كشف السرطان أمرًا مثيرًا للجدل في الحالات التي لا يُعرف في ما إذا كان الاختبار ينقذ حياة الأشخاص بالفعل.[6] يمكن أن يؤدي الكشف إلى نتائج إيجابية كاذبة مهمة وإجراءات باضعة لاحقة.[4] ينشأ الجدل عندما لا يكون واضحًا إذا كانت فوائد الكشف تفوق مخاطر اختبارات التشخيص اللاحقة وعلاجات السرطان. لا يُستطب كشف السرطان ما لم يكن متوسط العمر المتوقع أكبر من خمس سنوات والفائدة غير مؤكدة فوق سن 70.[7]
يُنظر في العديد من العوامل لتحديد ما إذا كانت فوائد الكشف تفوق مخاطره وتكاليفه.[1] تتضمن هذه العوامل:
- الأضرار المحتملة من اختبار الكشف: تعرض بعض أنواع اختبارات الكشف، مثل صور الأشعة السينية، الجسم للإشعاع المؤيِّن الذي يحتمل أن يكون ضارًا. هناك احتمال ضئيل بتسبب الإشعاع لسرطان جديد في الشخص السليم. لا يُنصح بالماموغرافي الكشفي، المستخدم للكشف عن سرطان الثدي، للرجال أو الشابات لأنهم عرضة للضرر أكثر من الاستفادة منه. ليس للاختبارات الأخرى، مثل فحص الجلد للكشف عن سرطان الجلد، خطر أذية كبير للمريض. يُوصى بإجراء اختبار مع احتمال حدوث مخاطر عالية فقط عندما تكون الفوائد عالية أيضًا.
- احتمال أن يحدد الاختبار السرطان بشكل صحيح: إذا لم يكن الاختبار حساسًا، يمكن أن يخطئ تشخيص السرطان. إذا لم يكن الاختبار نوعيًا، يمكنه أن يشير بشكل خاطئ إلى وجود السرطان لدى شخص سليم. تنتج جميع اختبارات كشف السرطان نتائج إيجابية كاذبة وسلبية كاذبة، وتنتج معظمها نتائج إيجابية كاذبة. ينظر الخبراء في معدل الأخطاء عند تقديم توصيات حول الاختبار الذي يجب استخدامه. يمكن أن يعمل الاختبار بشكل أفضل لدى بعض السكان أكثر من غيرهم. القيمة التنبؤية الإيجابية هي حساب احتمالية أن نتيجة الاختبار الإيجابية تمثل بالفعل وجود السرطان لدى فرد معين، بناءً على نتائج الأشخاص الذين لديهم عوامل خطر مماثلة.
- احتمالية الإصابة بالسرطان: لا يفيد الكشف في حالات السرطان النادرة. نادرًا ما يُجرى للشباب، إذ أن السرطان إلى حد كبير مرض موجود لدى الأشخاص الذين تزيد أعمارهم عن 50 عامًا. غالبًا ما تركز البلدان توصياتها بشأن الكشف على الأشكال الرئيسية من السرطان القابلة للعلاج والموجودة لدى سكانها. على سبيل المثال، توصي الولايات المتحدة بإجراء كشف شامل لسرطان القولون، الإصابة به شائعة في الولايات المتحدة، دون الكشف عن سرطان المعدة، الأقل شيوعًا؛ على النقيض من ذلك، توصي اليابان بالكشف عن سرطان المعدة، دون الكشف عن سرطان القولون النادر في اليابان. تعتمد توصيات الكشف على خطر إصابة الفرد بالسرطان، إذ يتلقى الأشخاص المعرضون لخطورة عالية كشفًا مبكرًا ومتكررًا أكثر من الأشخاص ذوي خطر الإصابة المنخفض.
- الأضرار المحتملة من إجراءات المتابعة: إذا كان اختبار الكشف إيجابيًا، تُجرى المزيد من الاختبارات التشخيصية عادةً، مثل خزعة الأنسجة. إذا أسفر الاختبار عن العديد من النتائج الإيجابية الكاذبة، فسيخضع العديد من الأشخاص لإجراءات طبية لا داعٍ لها، إذ يمكن أن يكون بعضها خطيرًا.
- ما إذا كان العلاج المناسب متاحًا ومناسبًا: لا يُنصح بالكشف في حال لم يكن هناك علاج فعال متاح. عندما لا يتوفر علاج فعال ومناسب، فإن تشخيص المرض القاتل ينتج عنه أضرار نفسية وعاطفية كبيرة. على سبيل المثال، لا يكون الكشف الروتيني للسرطان عادة مناسبًا لكبار السن الضعفاء جدًا، لأن علاج أي سرطان يُكتشف يمكن أن يقتل المريض.
- ما إذا كان الكشف المبكر يحسن نتائج العلاج: حتى عندما يتوفر العلاج، فإن الكشف المبكر لا يحسن النتيجة في بعض الأحيان. إذا كانت نتيجة العلاج نفسها كما لو لم تُكتشف، فإن الأمر الوحيد الذي يقوم به برنامج الكشف هو زيادة طول الوقت الذي عاش فيه الشخص ويعلم إصابته بالسرطان. هذه الظاهرة تسمى انحياز المهلة. يقلل برنامج الكشف المفيد من عدد سنوات الحياة المحتمل أن يخسرها (حياة أطول) والسنوات الحياتية المرافقة لإعاقة (حياة صحية أطول).
- ما إذا كانت هناك ضرورة لعلاج السرطان: يسمى تشخيص السرطان لدى الشخص الذي لن يتضرر من السرطان أبدًا بالتشخيص المفرط. التشخيص المفرط أكثر شيوعًا بين كبار السن المصابين بسرطانات بطيئة النمو. المخاوف حول التشخيص المفرط شائعة لسرطانات الثدي والبروستات.
- ما إذا كان الاختبار مقبولًا للمرضى: إذا كان اختبار الكشف مرهقًا للغاية، مثل تتطلب الكثير من الوقت، أو الكثير من الألم، أو السلوكيات غير المقبولة ثقافياً، فسيرفض الناس المشاركة.[3]
- تكلفة الاختبار: تتجاهل بعض هيئات الخبراء، مثل فرقة الخدمات الوقائية الأمريكية، مسألة المال تمامًا. ومع ذلك، فإن معظم هيئات الخبراء تتضمن تحليلاً للفعالية من ناحية التكلفة، إذ أن جميع العناصر الأخرى متساوية، تفضل الاختبارات الأقل تكلفة على الاختبارات الأكثر تكلفة، وتحاول موازنة تكلفة برنامج الكشف مع فوائد استخدام هذه الأموال لبرامج صحية أخرى. عادة ما تتضمن هذه التحليلات التكلفة الإجمالية لبرنامج الكشف لنظام الرعاية الصحية، مثل طلب وإجراء الاختبار والإبلاغ عن النتائج وإجراء الخزعات للنتائج المشبوهة، ولكن ليس من العادة أن تتضمن تكاليف الفرد، مثل الوقت المستغرق بعيدًا عن العمل.
- مدى إمكانية علاج السرطان: إذا كان متوسط العمر المتوقع للشخص منخفضًا أو كان في المراحل النهائية من حالة مزمنة، يمكن أن يعيش المريض حياة أفضل من خلال تجاهل السرطان حتى لو شُخّص به. إذا لم يؤدي تشخيص السرطان إلى تغيير في الرعاية، فإن كشف السرطان لن يؤدي على الأرجح إلى نتيجة إيجابية. يحدث التشخيص المفرط في هذه الحالة، على سبيل المثال، لدى المرضى في المراحل النهائية للقصور الكلوي، وتوصي المنظمات بعدم كشف السرطان لمثل هؤلاء المرضى.[8][9]
حسب النوع
سرطان الثدي
 مقالة مفصلة: فحص سرطان الثدي
مقالة مفصلة: فحص سرطان الثدي
كشف سرطان الثدي هو الكشف الطبي للنساء اللاتي لا تظهرن أعراض الإصابة بسرطان الثدي في محاولة للتشخيص المبكر. والهدف من التشخيص المبكر اكتشاف السرطان حين يكون قابلًا للعلاج. استُخدم عدد من اختبارات الكشف، بما في ذلك الفحوصات السريرية والذاتية للثدي والماموغرافي والكشف الجيني والموجات فوق الصوتية والتصوير بالرنين المغناطيسي. استخدام الماموغرافي في الكشف الشامل لسرطان الثدي أمرٌ مثير للجدل لأنه قد لا يقلل من معدل الوفيات للأسباب ككل ويسبب ضررًا من خلال العلاجات والإجراءات الطبية غير الضرورية. توصي به العديد من المنظمات الوطنية لمعظم النساء المسنات.[10]
سرطان عنق الرحم
 مقالة مفصلة: التنظير الشعاعي لعنق الرحم
مقالة مفصلة: التنظير الشعاعي لعنق الرحم
يعد الكشف عن سرطان عنق الرحم من خلال اختبار بابانيكولاو أو طرق أخرى فعالة للغاية في الكشف عن سرطان عنق الرحم والوقاية منه، على الرغم من وجود خطر كبير من العلاج المفرط لدى الشابات حتى سن 20 عامًا أو أكثر، والمعرضات لوجود الكثير من الخلايا غير الطبيعية التي تزول تلقائيًا.[11] هناك نطاق كبير في العمر الموصى به لبدء الكشف حول العالم. وفقًا للمبادئ التوجيهية الأوروبية لعام 2010 لكشف سرطان عنق الرحم، يتراوح عمر بدء الكشف من 20 إلى 30 عامًا، «ولكن يفضل ألّا يكون قبل سن 25 أو 30 عامًا»، اعتمادًا على عبء المرض بين السكان والموارد المتاحة.[12]
في الولايات المتحدة، يبلغ معدل الإصابة بسرطان عنق الرحم 0.1٪ بين النساء دون سن 20 عامًا، لذلك توصي جمعية السرطان الأمريكية وكذلك الكلية الأمريكية لأطباء التوليد وأمراض النساء بشدة أن يبدأ الكشف في سن 21، بغض النظر عن العمر عند بدء ممارسة الجنس أو غيرها من السلوكيات التي لها علاقة بخطر الإصابة.[13][14][15] بالنسبة للنساء الأصحاء اللاتي تتراوح أعمارهن بين 21 و29 عامًا ولم يسبق عندهن اكتشاف لطاخة عنق الرحم غير طبيعية، يجب إجراء كشف سرطان عنق الرحم باستخدام علم الخلية (لطاخة بابانيكولاو) كل 3 سنوات، بغض النظر عن حالة التلقيح ضد فيروس الورم الحليمي البشري (إتش بّي ڤي). الكشف المفضل للنساء اللواتي تتراوح أعمارهن بين 30 و65 عامًا هو «الاختبار المشترك»، والذي يتضمن مزيجًا من كشف الخلايا الخلوية العنقية واختبار فيروس الورم الحليمي البشري، كل 5 سنوات. ومع ذلك، من المقبول الكشف عن السرطان ضمن هذه الفئة العمرية باستخدام مسحة عنق الرحم وحدها كل 3 سنوات. في النساء فوق سن 65 عامًا، يمكن إيقاف الكشف عن سرطان عنق الرحم في حالة عدم وجود نتائج غير طبيعية للكشف خلال السنوات العشر السابقة ودون وجود سوابق سي آي إن 2 أو أعلى.[16]
سرطان الأمعاء
كشف سرطان القولون والمستقيم، في حال أُجري مبكرًا بشكل كافٍ، هو إجراء وقائيٌ[17][18] لأن معظم سرطانات القولون والمستقيم تنشأ تقريبًا من أورام حميدة تسمى السلائل القولونية (بوليبات)، والتي يمكن تحديد موقعها وإزالتها أثناء تنظير القولون.
توصي فرقة عمل الخدمات الوقائية الأمريكية بالكشف عن سرطان القولون والمستقيم باستخدام اختبار الدم الخفي في البراز أو التنظير السيني أو تنظير القولون، لدى البالغين بدءًا من سن 50 عامًا وحتى سن 75 عامًا.[19] لا يُنصح بالكشف بالنسبة للأشخاص الذين تزيد أعمارهم عن 75 عامًا أو الأشخاص الذين يقل عمرهم عن 10 سنوات. ومن الطرق الإنزيمية الجديدة لكشف سرطان القولون والمستقيم هي اختبار إم 2 بّي كي،[20] القادر على الكشف عن النزف وسرطانات القولون والمستقيم غير النزفية.[19] في عام 2008، نفذت مجموعة كايسر بيرمانينت كولورادو برنامجًا يستخدم المكالمات الآلية ويرسل معدات اختبار كيميائية مناعية للمرضى الذين تأخروا عن كشف سرطان القولون والمستقيم. زاد البرنامج نسبة جميع الأعضاء المؤهلين الذين كُشف لديهم عن السرطان بنسبة 25 بالمئة.[21] اعتُمد اختبار الحمض النووي مع اختبار كولوغارد من قِبل إدارة الأغذية والعقاقير.[22][23]
في إنجلترا، يُكشف عن السرطان لدى البالغين كل سنتين من خلال تحرّي وجود الدم الخفي في البراز بين سن 60 و74 عامًا.[24]
مراجع
- "What Is Cancer Screening?". National Cancer Institute. 2010-01-13. مؤرشف من الأصل في 04 أبريل 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Press Announcements - FDA authorizes, with special controls, direct-to-consumer test that reports three mutations in the BRCA breast cancer genes". 2019-09-10. مؤرشف من الأصل في 23 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Wilson, JMG; Jungner, G (1968). Principles and Practice of Screening for Disease (PDF). 34. Geneva: World Health Organization. مؤرشف من الأصل (PDF) في 01 مايو 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Croswell, JM; Kramer, BS; Kreimer, AR; Prorok, PC; et al. (2009). "Cumulative incidence of false-positive results in repeated, multimodal cancer screening". Annals of Family Medicine. 7 (3): 212–22. doi:10.1370/afm.942. PMC 2682972. PMID 19433838. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Nogueira, Felipe (2019). "Screening for prostate and breast cancer: It's more complex than you may think". Skeptical Inquirer. 43 (1): 50–53. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Osório, Flávia; Lima, Manuela Polidoro; Chagas, Marcos Hortes (January 2015). "Assessment And Screening Of Panic Disorder In Cancer Patients: Performance Of The PHQ-PD". Journal of Psychosomatic Research. 78 (1): 91–94. doi:10.1016/j.jpsychores.2014.09.001. PMID 25242741. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Spalding, MC; Sebesta, SC (July 15, 2008). "Geriatric screening and preventive care". American Family Physician. 78 (2): 206–15. PMID 18697503. مؤرشف من الأصل في 15 أبريل 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - American Society of Nephrology. "Five Things Physicians and Patients Should Question" (PDF). Choosing Wisely. ABIM Foundation. مؤرشف من الأصل (PDF) في 12 أبريل 2015. اطلع عليه بتاريخ 17 أغسطس 2012. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Chertow, GM; Paltiel, AD; Owen, WF; Lazarus, JM (1996). "Cost-effectiveness of cancer screening in end-stage renal disease". Archives of Internal Medicine. 156 (12): 1345–50. doi:10.1001/archinte.1996.00440110117016. PMID 8651845. الوسيط
|CitationClass=تم تجاهله (مساعدة) - PDQ Screening and Prevention Editorial Board (2002), "Breast Cancer Screening (PDQ®): Patient Version", PDQ Cancer Information Summaries, National Cancer Institute (US), PMID 26389160, مؤرشف من الأصل في 27 مايو 2020, اطلع عليه بتاريخ 30 أبريل 2020 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)CS1 maint: ref=harv (link) - Lixin, Tao; Lili, Han; Xia, Li; Qi, Gao; Lei, Pan; Lijuan, Wu; Yanxia, Luo; Wei, Wang; Zihe, Zheng; Xiuhua, Guo (2014). "Prevalence And Risk Factors For Cervical Neoplasia: A Cervical Cancer Screening Program In Beijing". BMC Public Health. 14 (1): 1185. doi:10.1186/1471-2458-14-1185. PMC 4256817. PMID 25410572. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Arbyn, M; Anttila, A; Jordan, J; Ronco, G; Schenck, U; Segnan, N; Wiener, H; Herbert, A; von Karsa, L (Mar 2010). "European Guidelines for Quality Assurance in Cervical Cancer Screening. Second edition--summary document". Annals of Oncology. 21 (3): 448–58. doi:10.1093/annonc/mdp471. PMC 2826099. PMID 20176693. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "SEER Stat Fact Sheets: Cervix Uteri Cancer". مؤرشف من الأصل في 25 مايو 2020. اطلع عليه بتاريخ 08 أبريل 2014. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Karjane, N; Chelmow, D (June 2013). "New cervical cancer screening guidelines, again". Obstetrics and Gynecology Clinics of North America. 40 (2): 211–23. doi:10.1016/j.ogc.2013.03.001. PMID 23732026. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Cervical Cancer Screening Guidelines for Average-Risk Women" (PDF). Center for Disease Control. مؤرشف من الأصل (PDF) في 02 مايو 2020. اطلع عليه بتاريخ 17 أبريل 2014. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Committee on Practice, Bulletins—Gynecology (Nov 2012). "ACOG Practice Bulletin Number 131: Screening for cervical cancer". Obstetrics and Gynecology. 120 (5): 1222–38. doi:10.1097/AOG.0b013e318277c92a. PMID 23090560. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "What Can I Do to Reduce My Risk of Colorectal Cancer?". Centers for Disease Control and Prevention. April 2, 2014. مؤرشف من الأصل في 13 مايو 2020. اطلع عليه بتاريخ March 5, 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة); Cite journal requires|journal=(مساعدة) - "Colon cancer". MedlinePlus. March 2, 2015. مؤرشف من الأصل في 05 يوليو 2016. اطلع عليه بتاريخ March 5, 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Screening for Colorectal Cancer". United States Preventive Services Task Force. October 2008. مؤرشف من الأصل في 06 يوليو 2014. اطلع عليه بتاريخ 29 يونيو 2014. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Tonus, C; Sellinger, M; Koss, K; Neupert, G (August 2012). "Faecal pyruvate kinase isoenzyme type M2 for colorectal cancer screening: A meta-analysis". World Journal of Gastroenterology. 18 (30): 4004–11. doi:10.3748/wjg.v18.i30.4004. PMC 3419997. PMID 22912551. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Automated Calls Followed by Mailed Kits Significantly Increase Colorectal Cancer Screening Rate in Those Overdue for Testing". Agency for Healthcare Research and Quality. 2013-02-13. مؤرشف من الأصل في 13 مارس 2020. اطلع عليه بتاريخ 13 مايو 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "FDA approves first non-invasive DNA screening test for colorectal cancer". 2014-08-11. مؤرشف من الأصل في 10 فبراير 2017. اطلع عليه بتاريخ 19 يناير 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Tepus, Melanie; Yau, Tung On (20 May 2020). "Non-Invasive Colorectal Cancer Screening: An Overview". Gastrointestinal Tumors (باللغة الإنجليزية): 1–12. doi:10.1159/000507701. ISSN 2296-3774. مؤرشف من الأصل في 27 مايو 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Population screening programmes: NHS bowel cancer screening (BCSP) programme - GOV.UK". مؤرشف من الأصل في 22 سبتمبر 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة)
 صور وملفات صوتية من كومنز
صور وملفات صوتية من كومنز
- بوابة طب
