جهد لينارد-جونز
جهد لينارد-جونز (الذي يُطلق عليه أيضًا جهد ل- ج، أو جهد 6-12، أو جهد 12- 6) هو نموذج بسيط رياضيًا يقرب التفاعل بين زوج من الذرات أو الجزيئات المتعادلة. قدم جون لينارد-جونز[1] للاقتراح صيغة لهذا الجهد بين الذري أول مرة في عام 1924. أكثر التعبيرات شيوعًا عن جهد ل- ج هي:
| فيزياء حاسوبية | ||||||||

| ||||||||
| تحليل عددي · محاكاة ديناميكا حرارية حاسوبية · كهرومغناطيسية حاسوبية · ميكانيكا حاسوبية
| ||||||||
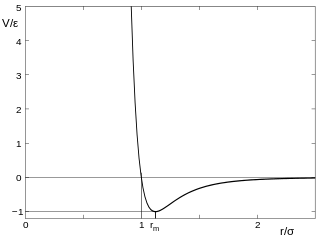
حيث ε هو عمق البئر الجهدي، وσ هي المسافة النهائية التي يكون عندها الجهد بين الجسيمات يساوي الصفر، وr هي المسافة بين الجسيمات، وrm هي المسافة التي تكون عندها قيمة الجهد أقل ما يمكن. وتكون قيمة دالة الجهد تساوي –ε عند rm. وترتبط المسافات ببعضها حيث rm = 21/6σ ≈ 1.122σ. يمكن لهذه البارامترات أن تُعدل حتى تنتج البيانات التجريبية أو حسابات دقيقة للكيمياء الكمية. يُستخدم جهد لينارد- جونز بشدة في المحاكات الحاسوبية نظرًا لبساطتها الحوسبية، بالرغم من وجود معادلات أكثر دقة لوصف الجهد.
التفسير
يصف الحد r12، وهو حد طارد، تنافر باولي في نطاقات قصيرة بسبب تداخل مدارات الإلكترونات، والحد r6، وهو الحد الجاذب على نطاق واسع يصف التجاذب في نطاقات كبيرة (قوى فان دير فالس أو قوى التشتت).
يعطي اشتقاق جهد ل- ج فيما يتعلق بـ r انطباعًا عن صافي القوة بين الجزيئية الموجودة بين الجزيئين. وقد تكون هذه القوة بين الجزيئية جاذبة أو طاردة، وفقًا لقيمة r. عندما تكون قيمة r صغيرة جدًا، تتنافر الجزيئات عن بعضها.
بينما يوجد تبرير فيزيائي واضح لصيغة الدالة عن الحد الجاذب، لا يوجد للحد الطارد أي تبرير نظري. فهو يُستخدم لأنه يقرب تنافر باولي جيدًا ولأنه ملائم أكثر بسبب كفاءة الحوسبة النسبية في حساب r12 كمربع r6.
يُعد جهد ل-ج تقريبًا جيدًا نسبيًا. نظرًا لبساطته، غالبًا ما يُستخدم لوصف خصائص الغازات وفي وضع نماذج للتشتت ويدمج التفاعلات في النماذج الجزيئية. وهو دقيق خصوصًا فيما يتعلق بذرات الغازات النبيلة وهو تقريب جيد على المسافات الطويلة والقصيرة للذرات والجزيئات المتعادلة.
الترتيب الأقل طاقة لأعداد الذرات اللانهائية التي يصفها جهد لينارد-جونز هو التعبئة المتراصة السداسية. عند رفع درجة الحرارة، يصبح الترتيب ذو الطاقة الحرة الأقل التعبئةَ المتراصة المكعبة، ثم السائلة. تحت الضغط، يتحول التركيب الأقل طاقة بين التعبئة المتراصة السداسية والمكعبة.[2] من المواد الحقيقية أيضًا الهياكل المكعبة المتمركزة حول الجسم.[3]
تحسن جهد ليناردو-جونز (12,6) بعد معادلة جهد باكنغهام التي اقترحها ريتشاد باكنغهام فيما بعد، والتي تتضمن بارامترًا إضافيًا وتحل فيها دالة أُسية محل الجزء الطارد:[4]
هناك طرق أحدث تصف تفاعل الجزيئات بدقة أكبر مثل جهد ستوكماير. يمكن لطرق الكيمياء الكمية أو نظرية اضطراب مولر- بليسيه أو طريقة العنقود المتقارن أو تفاعل التكوين الكامل أن تعطي نتائج في غاية الدقة لكنها تتطلب تكلفة حوسبية عالية.
تعبيرات بديلة
هناك عدة طرق مختلفة لصياغة جهد لينارد- جونز. بعض الصيغ الشائعة:
صيغة AB
هي صيغة بسيطة تستخدمها بعض برمجيات المحاكاة:
حيث و. والعكس، و. هذه الصيغة التي كتب بها لينارد- جونز جهد 12-6.[5]
وهناك صيغة حسابية عامة أكثر من ذلك تحتوي على متغير إضافي n.
حيث هي الطاقة الرابطة للجزيء (الطاقة اللازمة لفصل الذرات). يمكن أن يكون الأس n مرتبطًا بثابت الانطلاق k. (في ، حيث ) حيث:
ومنها يمكن حساب n إذا عُرف k. عادةً ما تكون الحالات المتناسقة معروفة، حيث يمكن أن يكون n مرتبطًا أيضًا بسرعة المجموعة في بلورة،
حيث a هي المسافة الشبكية وm كتلة الذرة.
انظر أيضًا
مراجع
- Lennard-Jones, J. E. (1924), "On the Determination of Molecular Fields", Proc. R. Soc. Lond. A, 106, صفحات 463–477, Bibcode:1924RSPSA.106..463J, doi:10.1098/rspa.1924.0082 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)CS1 maint: ref=harv (link) - Barron, T. H. K.; Domb, C. (1955), "On the Cubic and Hexagonal Close-Packed Lattices", Proceedings of the Royal Society of London. Series A, Mathematical and Physical Sciences, 227, صفحات 447–465, Bibcode:1955RSPSA.227..447B, doi:10.1098/rspa.1955.0023 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)CS1 maint: ref=harv (link) - Zhen, Shu; Davies, G. J. (16 August 1983). "Calculation of the Lennard-Jones n–m potential energy parameters for metals". Physica Status Solidi A. 78 (2): 595–605. Bibcode:1983PSSAR..78..595Z. doi:10.1002/pssa.2210780226. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Peter Atkins and Julio de Paula, "Atkins' Physical Chemistry" (8th edn, W. H. Freeman), p. 637.
- Lennard-Jones, J. E. (1931). "Cohesion". Proceedings of the Physical Society. 43 (5): 461–482. Bibcode:1931PPS....43..461L. doi:10.1088/0959-5309/43/5/301. الوسيط
|CitationClass=تم تجاهله (مساعدة)
وصلات خارجية
- بوابة الفيزياء
- بوابة الكيمياء
- بوابة تقنية المعلومات