تيوغوانين
تيوغوانين يعرف أيضا بالثيوغوانين أو 6 ثيوغوانين .وهو دواء يستخدم في علاج سرطان الدم النقياني الحاد (AML) ، وسرطان الدم الليمفاوي الحاد (ALL) وأيضا سرطان الدم النقياني المزمن (CML).[2] لا ينصح باستخدامه لفترات طويله.[2] ويعطى من خلال الفم.[2]
| تيوغوانين | |
|---|---|
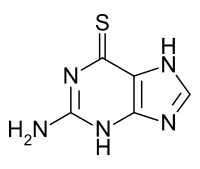 | |
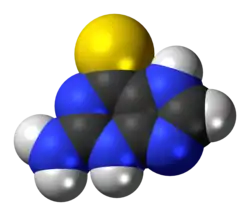 تيوغوانين | |
| الاسم النظامي | |
| 2-amino-1H-purine-6(7H)-thione | |
| يعالج | |
| اعتبارات علاجية | |
| اسم تجاري | Lanvis, Tabloid, others |
| ASHPDrugs.com | أسماء الدواء الدولية |
| مدلاين بلس | a682099 |
| طرق إعطاء الدواء | by mouth |
| بيانات دوائية | |
| توافر حيوي | 30% (range 14% to 46%) |
| استقلاب (أيض) الدواء | Intracellular |
| عمر النصف الحيوي | 80 minutes (range 25–240 minutes) |
| معرّفات | |
| CAS | 154-42-7 |
| ك ع ت | L01L01BB03 BB03 |
| بوب كيم | CID 2723601 |
| IUPHAR | 6845 |
| ECHA InfoCard ID | 100.005.299 |
| درغ بنك | DB00352 |
| كيم سبايدر | 2005804 |
| المكون الفريد | WIX31ZPX66 |
| كيوتو | D08603 |
| ChEBI | CHEBI:9555 |
| ChEMBL | CHEMBL727 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C5H5N5S |
| الكتلة الجزيئية | 167.193 g/mol |
أشهر الآثار الجانبيه لاستخدام هذا الدواء تتضمن : كبت النخاع العظمي ، امراض بالكبد ، التهاب مخاطية الفم.[2][3] حيث يوصى بعمل فحص لانزيمات الكبد بشكل اسبوعي خلال فترة العلاج [2]، ويزداد خطر تعرض المريض للآثار الجانبيه للدواء إذا كان من الأشخاص اللذين لديهم نقص في انزيم الثيوبيورين ميثل ترانسفيراز.[3] كذلك يجب تجنب الحمل إذا كان الرجل أو المرأة يخضع للعلاج بهذا الدواء.[2]
تيوغوانين يعد من ضمن الأدوية المضاده للايض .[4] ومن ناحية تركيبه الكيميائي فهو مضاهئ بيورين في الغوانين ويعمل التيوغوانين على تدمير ال DNA و ال RNA.[5]
تم تطوير تيوغوانين بين عامي 1949 و 1951.[6][7] و هو على قائمة الأدوية الأساسية لمنظمة الصحة العالمية، الأدوية الأكثر فعالية وأمانا المطلوبة في النظام الصحي.[8] سعر الجملة في العالم النامي يبلغ حوالي 7.07 دولار أمريكي لكل 40 ملغ من الحبوب بحلول عام 2014.[9] في المملكة المتحدة يكلف هذا المبلغ NHS حوالي 4.14 جنيه.[10]
الاستخدامات الطبية
- سرطان الدم الحاد عند الأطفال والبالغين
- سرطان الدم النقياني المزمن
- مرض الأمعاء الالتهابي ، خاصة التهاب القولون التقرحي
- الصدفيه [11]
الآثار الجانبيه
- قلة الكريات البيض و قلة الخلايا المتعادلة
- نقص الصفيحات
- فقر الدم
- فقدان الشهية
- غثيان وتقيء
- تسمم الكبد و هذا يتجلى على النحو التالي:
مرض الكبد انسداد فينيو
كان مصدر القلق الرئيسي الذي أعاق استخدام ثيوغوانين هو مرض انسداد الأوعية الدموية (VOD) . و تم الإبلاغ عن حدوث NRH مع ثيوغوانين بين 33-76 ٪.[12] إن خطورة ظهور الفيديو حسب الطلب أمر خطير وغير قابل للإعادة بشكل دائم لذا كان هذا التأثير الجانبي مصدر قلق كبير. ومع ذلك، أظهرت الأدلة الحديثة باستخدام نموذج حيواني للـ NRH / VOD الناجم عن مادة تيوغينين أنه، خلافاً للافتراضات السابقة، يعتمد NRH / VOD على الجرعة وقد تم إثبات آلية ذلك.[12] وقد تأكد هذا في التجارب على البشر، حيث ثبت أن ثيوجوانين آمن لكنه فعال لمرض الاضطرابات الهضمية عند استخدامه بجرعات أقل من تلك الموصوفة عادة.[13] وقد أدى هذا إلى إحياء الاهتمام في ثيوغوان بسبب فعاليته العالية وأسرع من العمل مقارنة بالثيوبيورين ومثبطات المناعة الأخرى مثل الميكوفينيلات.[14]
موانع الاستعمال
التفاعلات
الامراض السرطانية التي لا تستجيب للعلاج بالميركابتوبيورين لن تستجيب للتيوغوانين . ومن ناحيه أخرى، بعض حالات مرض الامعاء الالتهابي التي لا تستجيب للميركابتوبيورين (أو الدواء الاولي له آزاثيوبرين ) من الممكن ان تستجيب للتيوغوانين.
علم الوراثة الدوائي
يعد إنزيم الثيوبيورين ميثل ترانسفيراز هو المسؤول عن التثبيط المباشر لثيوغوان إلى قاعدة ميثيليثوغوانين - وهذا الميثيون يمنع ثيوغوانين من تحويل إضافي إلى نواتج نوكليوتيد نوكليوتيد نشطة [16][17][18] يمكن أن تؤدي بعض التغيرات الجينية داخل الجين TPMT إلى انخفاض أو عدم وجود نشاط إنزيم TPMT ، والأفراد الذين هم متماثلات اللواقح أو متغاير الزيجوت لهذه الأنواع من الاختلافات الجينية قد يكون لديهم مستويات متزايدة من نواتج TGN وزيادة خطر الإصابة بإخماد نخاع العظم الشديد (كبت نقي العظم) تلقي ثيوغوانين [16] في العديد من الأعراق، تحدث تعدد الأشكال TPMT التي تؤدي إلى انخفاض أو غياب نشاط TPMT مع تردد حوالي 5 ٪، وهذا يعني أن حوالي 0.25 ٪ من المرضى متماثلون لهذه المتغيرات.[16][19] ومع ذلك، يمكن لمقايسة نشاط TPMT في خلايا الدم الحمراء أو اختبار وراثي TPMT تحديد المرضى الذين يعانون من نشاط TPMT مخفض، مما يسمح بتعديل جرعة ثيوبورين أو تجنب الدواء بالكامل.[16][20] وصف الدواء الذي وافقت عليه إدارة الأغذية والعقاقير لمذكرات الثيوغوان أن المرضى الذين يعانون من نقص TPMT قد يكونون عرضة لتطوير كبت نقي العظم وأن المختبرات تقدم اختبار لنقص TPMT.[21]] في الواقع، يعد اختبار نشاط TPMT حاليًا أحد الأمثلة القليلة على علم الوراثة الدوائي الذي يتم ترجمته إلى الرعاية السريرية الروتينية.[22]
الأيض وحركية الدواء
جرعة واحده عن طريق الفم لا تتعرض بأكملها لعمليات الايض والامتصاص وهذا يختلف من شخص لآخر. التوافر الحيوي للثيوغوانين يبلغ بالمتوسط 30% (بمدى يتراوح بين 14-46 % ) . اعلى تركيز من هذا الدواء في البلازما بعد جرعة واحدة عن طريق الفم يظهر بعد 8 ساعات .
الثيوغوانين، مثل الثيوبيورينات الأخرى، سام للخلايا البيضاء ؛ ونتيجة لذلك فأن جرعات قليله منه تثبط المناعة والجرعات العالية منه تعطي تأثير مضاد لسرطان الدم اومضاد للورم . الثيوغوانين يندمج في خلايا نخاع العظم في الانسان، لكن لاتستطيع العبور من خلال حاجز الدم الدماغي . كما لا يمكن اثبات ان الثيوغوانين موجود في السائل الدماغي الشوكي .
عمر النصف للثيوغوانين في البلازما قصير، بسبب امتصاصه السريع من قبل الكبد وخلايا الدم وتحويله إلى 6 ثيوغوانين نيوكليوتيد . يتم طرح الثيوغوانين خارج الجسم من خلال الكليتين في البول، لكن بشكل رئيسي كناتج ايض ( 2-امينو6-ميثل ثيوبيورين ).
الثيوغوانين يتعرض للايض الهدمي بطريقتين [23]، أول طريقة تتمثل بحدوث عملية نزع الأمين من خلال انزيم نازعة أمين الغوانين لينتج المركب 6 ثيوزانثين، الذي له فاعلية قليلة كمضاد للاورام، ثم يحدث له اكسدة من خلال انزيم أوكسيداز الزانثين وينتج حمض التيوريك . الطريقة الثانية تتمثل بحدوث عملية نزع مجموعة ميثل من الثيوغوانين وينتج المركب 2-امين 6-ميثل ثيوبيورين، له فاعلية قليلة كمضاد للاورام ويعد اقل سميه من الثيوغوانين .
آلية التفاعل
6-ثيوغوانين يستخدم انزيم هيبوكزانتين-غوانين فوسفوريبوزيل-ترانسفيراز ليتحول للمركب 6-ثيوغوانوزين مونوفوسفات، تركيز عالي من هذا المركب من الممكن ان يؤدي إلى تراكمه داخل الخلايا وعرقلة تصنيع الغوانين نيوكليوتيد عن طريق انزيم ديهيدروجيناز إينوزين مونوفوسفات .(IMP dehydrogenase).[24]
ثم يتعرض المركب 6-ثيوغوانوزين مونوفوسفات لعملية فسفرة وينتج المركبين، ثيوغوانوزين ثنائي الفوسفات وثيوغوانوزين ثلاثي الفوسفات . 6-ثيوغوانوزين مونوفوسفات ثيوغوانوزين ثنائي الفوسفات وثيوغوانوزين ثلاثي الفوسفات، هذه الثلاث مركبات مجتمعة تسمى 6-ثيوغوانين نيوكليوتيد .
6-ثيوغوانين نيوكليوتيد سام للخلايا من خلال :
- اندماجه مع DNA في فترة حدوث الطور التركيب من دورة الخلية
- يثبط الجي بروتين مما يؤدي إلى تثبيط Rac1 ، الذي ينظم المسار المسمى ب Rac/Vav [25]
من الممكن ان يرتبط ال 6-ثيوغوتنين بال RNA ، مما يؤدي إلى تعديل في شريط ال RNA لا يمكن قرأته من قبل الريبوسوم .
الكيمياء
لونه أصفر باهت، ليس له رائحة، على شكل مسحوق بلوري.
الاسماء
تيوغوانين (INN، BAN) أو ثيوغوانين (AAN، USAN).
يدار ثيوغوانين عن طريق الفم (كأقراص تدعى لانفس - "Lanvis").
المصادر
- https://drugs.ncats.io/drug/WIX31ZPX66 — تاريخ الاطلاع: 2 نوفمبر 2018 — المخترع: معاهد الصحة الوطنية الأمريكية
- BNF 69 : British national formulary. ISBN 9780857111562. OCLC 906247142. مؤرشف من الأصل في 15 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Taylor, April (2016-12-21). "Ocean Shipping Container Availability Report, December 21, 2016" (PDF). مؤرشف من الأصل (PDF) في 19 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); Cite journal requires|journal=(مساعدة) - "Tioguanine 40 mg Tablets – Summary of Product Characteristics (SPC) – (eMC)". www.medicines.org.uk. مؤرشف من الأصل في 21 ديسمبر 2016. اطلع عليه بتاريخ 21 ديسمبر 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Principles of pharmacology : the pathophysiologic basis of drug therapy (الطبعة 3rd ed). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2012. ISBN 9781608312702. OCLC 705260923. مؤرشف من الأصل في 15 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: نص إضافي (link) - Sigel, Astrid; Sigel, Helmut (1996). Metal Ions in Biological Systems: Volume 32: Interactions of Metal Ions with Nucleotides: Nucleic Acids, and Their Constituents (باللغة الإنجليزية). CRC Press. صفحة 302. ISBN 9780824795498. مؤرشف من الأصل في 21 ديسمبر 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Landau, Ralph; Achilladelis, Basil; Scriabine, Alexander (1999). Pharmaceutical Innovation: Revolutionizing Human Health (باللغة الإنجليزية). Chemical Heritage Foundation. صفحة 342. ISBN 9780941901215. مؤرشف من الأصل في 21 ديسمبر 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "WHO Model List of Essential Medicines (19th List)" (PDF). World Health Organization. April 2015. مؤرشف من الأصل (PDF) في 13 ديسمبر 2016. اطلع عليه بتاريخ 08 ديسمبر 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Tioguanine". International Drug Price Indicator Guide. مؤرشف من الأصل في 11 أكتوبر 2018. اطلع عليه بتاريخ 28 نوفمبر 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - British national formulary : BNF 69 (الطبعة 69). British Medical Association. 2015. صفحات 588, 592. ISBN 9780857111562. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Mason C, Krueger GG (January 2001). "Thioguanine for refractory psoriasis: a 4-year experience". J. Am. Acad. Dermatol. 44 (1): 67–72. doi:10.1067/mjd.2001.109296. PMID 11148479. مؤرشف من الأصل في 10 يناير 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dubinsky MC, Vasiliauskas EA, Singh H, et al. (2003). "6-thioguanine can cause serious liver injury in inflammatory bowel disease patients". Gastroenterology. 125 (2): 298–303. doi:10.1016/S0016-5085(03)00938-7. PMID 12891528. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Tack GJ, van Asseldonk DP, van Wanrooij RL, et al. (August 2012). "Tioguanine in the treatment of refractory coeliac disease – a single centre experience". Aliment Pharmacol Ther. 36 (3): 274–81. doi:10.1111/j.1365-2036.2012.05154.x. PMID 22646133. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Van Asseldonk DP, Oancea I, Jharap B, et al. (March 2012). "Is thioguanine-associated sinusoidal obstruction syndrome avoidable? Lessons learned from 6-thioguanine treatment of inflammatory bowel disease and a mouse model". Rev Assoc Med Bras. 58 (Suppl.1): S8–13. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gardiner SJ, Gearry RB, Roberts RL, et al. (2006). "Exposure to thiopurine drugs through breast milk is low based on metabolite concentrations in mother-infant pairs". Br J Clin Pharmacol. 62 (4): 453–6. doi:10.1111/j.1365-2125.2006.02639.x. PMC 1885151. PMID 16995866. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Relling MV, Gardner EE, Sandborn WJ, Schmiegelow K, Pui CH, Yee SW, Stein CM, Carrillo M, Evans WE, Klein TE; Clinical Pharmacogenetics Implementation Consortium (March 2011). "Clinical Pharmacogenetics Implementation Consortium guidelines for thiopurine methyltransferase genotype and thiopurine dosing". Clin Pharmacol Ther. 89 (3): 387–91. doi:10.1038/clpt.2010.320. PMC 3098761. PMID 21270794. الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|pmc=و|PMC=تكرر أكثر من مرة (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Zaza G, Cheok M, Krynetskaia N, Thorn C, Stocco G, Hebert JM, McLeod H, Weinshilboum RM, Relling MV, Evans WE, Klein TE, Altman RB (September 2010). "Thiopurine pathway". Pharmcogenet Genomics. 20 (9): 573–4. doi:10.1097/FPC.0b013e328334338f. PMC 3098750. PMID 19952870. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Fujita K, Sasaki Y (August 2007). "Pharmacogenomics in drug-metabolizing enzymes catalyzing anticancer drugs for personalized cancer chemotherapy". Curr. Drug Metab. 8 (6): 554–62. doi:10.2174/138920007781368890. PMID 17691917. مؤرشف من الأصل في 12 يناير 2013. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Mutschler, Ernst; Schäfer-Korting, Monika (2001). Arzneimittelwirkungen (باللغة الألمانية) (الطبعة 8). Stuttgart: Wissenschaftliche Verlagsgesellschaft. صفحات 107, 936. ISBN 3-8047-1763-2. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Payne, K.; Newman, W.; Fargher, E.; Tricker, K.; Bruce, I. N.; Ollier, W. E. R. (2007). "TPMT testing in rheumatology: Any better than routine monitoring?". Rheumatology. 46 (5): 727–729. doi:10.1093/rheumatology/kel427. PMID 17255139. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "TABLOID- thioguanine tablet". http://dailymed.nlm.nih.gov/dailymed/drugInfo.cfm?setid=4490128b-e73f-4849-9d6e-e8591639d771. الوسيط
|CitationClass=تم تجاهله (مساعدة); روابط خارجية في|موقع=(مساعدة); مفقود أو فارغ|url=(مساعدة);|access-date=بحاجة لـ|url=(مساعدة) - Wang L, Pelleymounter L, Weinshilboum R, Johnson JA, Hebert JM, Altman RB, Klein TE (June 2010). "Very important pharmacogene summary: thiopurine S-methyltransferase". Pharmacogenet Genomics. 20 (6): 401–5. doi:10.1097/FPC.0b013e3283352860. PMC 3086840. PMID 20154640. الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|pmc=و|PMC=تكرر أكثر من مرة (مساعدة) - Oncea I; Duley J. (2008). "Chapter 38. Pharmacogenetics of Thiopurines.". In Brunton, L. L.; Lazo, J. S.; Parker, K. (المحررون). Goodman & Gilman's The Pharmacological Basis of Therapeutics (الطبعة 11th). McGraw-Hill's Access Medicine (on-line). الوسيط
|CitationClass=تم تجاهله (مساعدة) - Evans WE. (2004). "Pharmacogenetics of thiopurine S-methyltransferase and thiopurine therapy". Ther Drug Monit. 26 (2): 186–91. doi:10.1097/00007691-200404000-00018. PMID 15228163. الوسيط
|CitationClass=تم تجاهله (مساعدة) - de Boer NK, van Bodegraven AA, Jharap B, et al. (Dec 2007). "Drug Insight: pharmacology and toxicity of thiopurine therapy in patients with IBD". Nat Clin Pract Gastroenterol Hepatol. 4 (12): 686–94. doi:10.1038/ncpgasthep1000. PMID 18043678. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء
- بوابة صيدلة
- بوابة طب
 صور وملفات صوتية من كومنز
صور وملفات صوتية من كومنز
