هيدروكسيد الصوديوم
هيدروكسيد الصوديوم مركب كيميائي قوي له الصيغة الكيميائية (NaOH). يعرف أيضاً بالصودا الكاوية(يعرف في بعض الدول العربية بالأطرونة) ،[4][5] ويستخدم في العديد من الصناعات درجة ذوبانه في الماء عالية جداً وتصل المحاليل المائية إلى تركيزات كبيرة ،ويعتبر هيدروكسيد الصوديوم المصدر الأساسي في صناعة ملح الطعام (كلوريد الصوديوم).
| هيدروكسيد الصوديوم | |
|---|---|
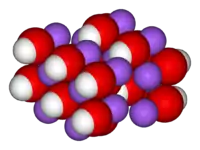 هيدروكسيد الصوديوم | |
 هيدروكسيد الصوديوم | |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Sodium hydroxide[1] | |
| تسمية الاتحاد الدولي للكيمياء | |
Sodium oxidanide[2] | |
| المعرفات | |
| رقم CAS | 1310-73-2 |
| بوب كيم (PubChem) | 14798 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| الصيغة الجزيئية | NaOH |
| الكتلة المولية | 39.9971 g mol−1 |
| المظهر | White, waxy, opaque crystals |
| الرائحة | odorless |
| الكثافة | 2.13 g/cm3 |
| نقطة الانصهار | 318 °س، 591 °ك، 604 °ف |
| نقطة الغليان | 1388 °س، 1661 °ك، 2530 °ف |
| الذوبانية في الماء | 41.8 g/100 mL (0 °C) 111 g/100 mL (20 °C) 337 g/100 mL (100 °C) |
| الذوبانية | soluble in غليسرول negligible in أمونياك insoluble in إيثر |
| الذوبانية في methanol | 23.8 g/100 mL |
| الذوبانية في ethanol | <<13.9 g/100 mL |
| ضغط البخار | <2.4 kPa (at 20 °C) |
| حموضة (pKa) | 13 |
| معامل الانكسار (nD) | 1.3576 |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
−427 kJ·mol−1[3] |
| إنتروبيا مولية قياسية S |
64 J·mol−1·K−1[3] |
| الحرارة النوعية، C | 59.66 J/mol K |
| المخاطر | |
| صحيفة بيانات سلامة المادة | External MSDS |
| رمز الخطر وفق GHS |  |
| فهرس المفوضية الأوروبية | 011-002-00-6 |
| ترميز المخاطر |  C C |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
0
3
1
ALK |
| مركبات متعلقة | |
| أنيونات أخرى | بيكبريتيد الصوديوم |
| كتيونات أخرى | هيدروكسيد السيزيوم هيدروكسيد الليثيوم |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
خواصه
- مركب صلب أبيض متميع
- له ملمس صابونى وتأثيره كاو على الجلد
- يذوب في الماء بسهولة ويكون محلول قلوي
- يتفاعل مع الأحماض المخففة مكونا ملح الصوديوم للحمض والماء
التحضير
قديما كان يحضر من معالجة رماد الصودا الناتج من طريقة لوبلان بهيدروكسيد الكالسيوم
وذلك اعتمادا على أن كربونات الكالسيوم غير منحلة في محلول الصودا الكاوية. إلا أن هذه الطريقة لم تعد تستخدم منذ عام 1962. الطريقة المعتمدة حاليا للإنتاج تتم من خلال التحليل الكهربائي لمحلول مركز من كلوريد الصوديوم في الماء حيث يتشكل غاز الكلور على الأنود (المصعد) في حين يتشكل كل من غاز الهيدروجين وهيدروكسيد الصوديوم على الكاثود (المهبط). المعادلة الإجمالية للتفاعل:
يجب الفصل بين الكلور وهيدروكسيد الصوديوم الناتجين من عملية التحليل الكهربائي للحصول على كل منهما، ويتم ذلك باستخدام إحدى أنواع خلايا التحليل التالية
- خلية الزئبق
وهي أقدم الخلايا المستخدمة ويكون الأنود فيها إما من الغرافيت أو من التيتانيوم، في حين يكون الكاثود عبارة عن حوض من الزئبق. يعطي التحليل الكهربائي ملغمة زئبق-صوديوم التي لا تتفكك بوجود المحلول الملحي المركز، في حين يتم تفكيكها بحوض مائي آخر منفصل حسب المعادلة
إلا أنه ما يؤخذ على هذه الطريقة استعمالها للزئبق السام، مما أدى إلى تراجعها مقارنة مع غيرها.
- الخلية الحجابية
يستخدم في هذا النوع من الخلايا حجاب (diaphragm) من الأسبيستوس يفصل بين الأنود والكاثود، مما يسمح بالهجرة الكهربائية للشوارد (الأيونات) لكنه يقلل من انتشار النواتج. يكون الأنود من الغرافيت أما الكاثود من حديد الصب. يجب أن تتم عملية استبدال مستمر للحجب بشكل منتظم.
- الخلية الغشائية
ويستخدم فيها غشاء نصف نفوذ يفصل بين الأنود والكاثود. يتم التحكم بالهجرة المعاكسة للأيونات من خلال معدل تدفق السائل خلال الغشاء، والذي يتم من خلال تحكم دقيق لمستوى السائل في الحجرات. الأغشية المستخدمة عبارة عن بوليمرات مثل النافيون.
التفاعلات
إذا أرسلنا غاز الكلور في دورق يحوي محلول الصود الكاوي لمدة كافية حصلنا على مزيج من ملحين هما كلوريد الصوديوم وتحت كلوريت الصوديوم NaOCl وفق المعادلتين :
- HCl + NaOH = NaCl +H2O
- HOCL +NaOH = NaOCl +H2O
الاستخدامات
هيدروكسيد الصوديوم قاعدة رئيسية قوية تستخدم في الصناعات الكيميائية
- صناعة الورق
هيدروكسيد الصوديوم كان يستخدم على نطاق واسع في صناعة الورق مع كبريتيد الصوديوم يستخدم لفصل مادة (السيلولوز) المستخدم في صناعة الورق عن المواد غير السيلولوزية
- الكشف عن الشقوق القاعدية (الكاتيونات)
وذلك بإضافة محلول هيدروكسيد الصوديوم إلى محلول الملح فيتكون راسب ملون
(الكشف عن كاتيون النحاس +2)
محلول الملح + محلول هيدروكسيد الصوديوم = راسب أزرق من هيدروكسيد النحاس II يسود بالتسخين
CuSo4 + 2NaOH ---> Cu(OH)2 + Na2So4
Cu(OH)2 ---> CuO + H2O
(الكشف عن كاتيون الألومنيوم +3)
محلول الملح + محلول هيدروكسيد الصوديوم = راسب أبيض من هيدروكسيد الألومنيوم يذوب في وفرة من هيدروكسيد الصوديوم لتكون ميتاألومنيات الصوديوم الذي يذوب في الماء
AlCl3 + 3NaOH ---> Al(OH)3 + 3NaCl
Al(OH)3 + NaOH ---> NaAlO2 + 2H2O
- صناعة الصابون
بإضافة هيدروكسيد الصوديوم إلى زيت نباتي
- صناعة الحرير الصناعي
- تنقية البترول من الشوائب الحامضية
- إنتاج الألومينا
- الحفر بحثاً عن النفط
- إنتاج الوقود
- الديزل الحيوي
- عامل تنظيف
- ترميم نوافذ الزجاج المرصص
- مقشر الدهانات
- الاستخدام في التحليل الكيميائي
المصادر
- "Sodium Hydroxide - Compound Summary". مؤرشف من الأصل في 8 أغسطس 2014. اطلع عليه بتاريخ 12 يونيو 2012. الوسيط
|CitationClass=تم تجاهله (مساعدة) - 1310-73-2|Sodium hydroxide solution|Sigma Aldrich|sodium oxidanide نسخة محفوظة 27 يناير 2018 على موقع واي باك مشين.
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. صفحة A23. ISBN 0-618-94690-X. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Material Safety Datasheet" (PDF). مؤرشف من الأصل (PDF) في 13 أكتوبر 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Material Safety Datasheet 2" (PDF). مؤرشف من الأصل (PDF) في 3 مارس 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة)

