انتشار
الانتشار هي عملية توزيع جزيئات أو ذرات أو حبيبات بشكل متساوٍ في فراغ أو في حيّز متاح أو تخللها خلال حاجز غشائي.[1][2][3] ويتم الانتشار بانتقال الجزيئات أو الذرات من منطقة ذات تركيز عالي إلى منطقة ذات تركيز أقل حتى يتساوى تركيز الجزيئات في المنطقتين.
.png.webp)
تنشأ ظاهرة الانتشار بسبب الحركة الحرارية العشوائية لجزيئات المادة التي تصطدم مع بعضها البعض وتتباعد لتشغل جميع الحيز المتاح لها.
توضيح عملية الانتشار

لتوضيح عملية الانتشار يمكن مشاهدة عملية تلوين سايل شفاف بصبغة ومراقبة عملية انتشار اللون في السائل الشفاف كما هو واضح في الصورة.
في هذا المثل فإن الصبغة يتم إضافتها للسائل، وتُترك لتنتشر في السائل دون أي تحريك لا للسائل ولا أي تحريك للمائدة التي يقف عليها. فتوزيع اللون في السائل الشفاف تتم ذاتياً بسبب خاصية الانتشار. في هذه الحالة هناك أيضاً عوامل أخرى مؤثرة في توزيع اللون في السائل مثل الكثافة فرق درجة الحرارة بين السائلين.
آلية الانتشار
يعتمد الانتشار على حركة الجزيئات البراونية، وهي الحركة العشوائية للجزيئات في الحيز، والتي تسبب تصادم الجزئيات مع بعضها البعض وابتعادها عن بعضها لملء أي حيّز متاح. تعتمد هذه الحركة على الطاقة الحرارية المخزونة في المادة. هذه الحركة هي من خواص المادة ولا تحتاج إلى طاقة خارجية، وهي من مميزات كل مادة درجة حرارتها فوق الصفر المطلق.
تتسبب نزعة المادة لملء كامل الحيز المُتاح لها بحركة المادة من المنطقة ذات التركيز العالي إلى الجهة ذات التركيز المنخفض ولحركة بالاتجاه المعاكس من المنطقة ذات التركيز المنخفض إلى المنطقة ذات التركيز العالي، وذلك لكون الحركة عشوائية، إلا أن كثرة الجزيئات في جهة التركيز العالي تتسبب بتحرك عدد أكبر من الجزيئات تجاه جهة التركيز المنخفض، أي أن محصلة حركة الجزيئات يكون من المنطقة ذات التركيز العالي إلى منطقة التركيز المنخفض حتى يتساوى التركيزان فيحصل التوازن، مما يعني تساوي الحركة في الاتجاهين. لهذا فإن الانتشار يمكن أن يُنظر إليه على أنه القوة التي تؤدي إلى انتقال المادة من أ إلى ب.
العوامل المؤثرة في الانتشار
| الحالة | المسافة المقطوعة |
|---|---|
| الغازات | 100 مم في دقيقة |
| السوائل | 0,5 مم في دقيقة |
| الأجسام الصلبة | 0,0001 مم في دقيقة |
هناك عدة عوامل تؤثر في سرعة الانتشار وتشمل:
- درجة الحرارة والتناسب معها طردي، فبارتفاع درجة الحرارة ترتفع الطاقة الحركية لجزيئات المادة، وتزيد عدد اصتداماتها في الثانية الواحدة، وبالتالي ضغط الانتشار.
- حجم الجزيئات وتناسبه عكسي.
- فرق التركيز في المحلول والتناسب طردي.
- حالة المادة فالانتشار في الغازات أسرع منه في السوائل، وهو أبطأ مايكون في الأجسام الصلبة. وذلك لضعف ارتباط الجزيئات مع بعضها البعض في الحالة الغازية، ولحركتها العشوائية، والتي تقل في السوائل وتكون شبه منعدمة في الحالة الصلبة.
ويمكن ربط العوامل المؤثرة في تدفق الانتشار عن طريق قانون فيك للانتشار.
حالات خاصة
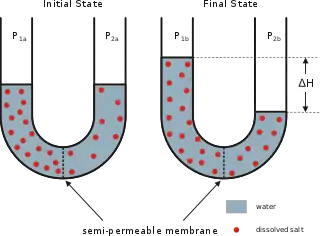
من الحالات الخاصة للانتشار الانتشار من خلال غشاء منفذ (نفوذ) (بالإنجليزية: permeable)، في هذه الحالة يكون هناك غشاء يفصل بين حيّزين، ولكنه منفذ للسائل وللمادة المُذابة فيه. في هذه الحالة فإن محصلة انتقال جزيئات المادة المُذابة يكون باتجاه الجانب ذي التركيز الأقل كما هو موضح في الصورة. من شروط الانتشار أن يكون "الحاجز" الفاصل منفذاً للمادة المذابة. أما إذا ما كان الغشاء الفاصل نصف منفذ (نصف نفوذ) (بالإنجليزية: semipermeable) فإن جزيئات المادة المُذابة تكون غير قادرة على الانتقال إلى الجانب الآخر، وهنا ينشأ ضغط يسمى بالضغط التناضحي.
تطبيقات الانتشار
من خلال تحليل سرعات الانتشار (انظر الجدول) نلاحظ أن عملية الانتشار تلعب دوراً أكبر في الحالة الغازية، وأقل في السوائل، بينما تعتبر من القوى المهملة في المواد الصلبة.
ففي الحالة الغازية نلاحظ أن تسريب غاز ما في مكان مغلق يؤدي - حتى مع انعدام التيارات الهوائية - لتوزع الغاز في كامل الحيز المغلق مثل الغرف والمكاتب، في نفس الوقت يُساهم فتح النافذة بغرض التهوية إلى تجدد الهواء حتى ولو انعدم تيار الهواء، أو لم تُزود الغرفة بالمراوح، وذلك لأن الهواء والروائح في الغرفة تتحرك تجاه الخارج، حيث يكون تركيزها بالخارج أقل منه في الغرفة.
أما في السوائل فإن انتشار المواد يكون ببطء أكثر، فلو تمت إذابة مكعب من السكر في كأس ماء، فإن الوقت الذي يحتاجه السكر للذوبان والتوزع في الكأس يكون طويلاً نسبياً، لذا يُستعان بأساليب لتسريع العملية من خلال تحريك الكأس أو خضها. أما في طهو الطعام، فإن الوقت يكون كافياً، مما يجعل عملية الانتشار تكون مفيدة في حالات يصعب بها التحريك والخلط، كما أن الملح الذي يُرَش على سطح اللحم، ينتقل مع مرور الوقت ليصل إلى الطبقات الداخلية لقطعة اللحم، ويتم انتقال الملح هنا عن طريق الانتشار خلال عُصارة اللحم.
الانتشار عبر مسافات قصيرة يكون فعالاً، فلو نظرنا إلى المسافات التي لابد أن تقطعها المواد في الخلايا فإننا سنجدها تجسر مسافات بالميكرومترات، فعلى مستوى الأوالي أو الكائنات وحيدة الخلية فإن حصول هذه الكائنات على الغذاء وعمليات الإفراز تتم بطريق الانتشار البسيط عبر الغشاء الخلوي. في الكائنات متعددة الخلايا كالإنسان مثلاً فإن الدورة الدموية تقوم بتجسير المسافات الطويلة عن طريق حركة الدم في الأوعية الدموية. أما على مستوى الأنسجة الحيوية فإن التبادل الحيوي وعمليات نقل الغذاء والإفرازات يعتمد على خواص مثل الانتشار والتناضح والنقل الحيوي.
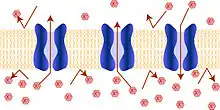
أهمية هذه الحالة يكون في الخلايا الحية، حيث يكون الجدار الخلوي منفذاً لمواد، وغير منفذ أو نصف منفذ لأخرى، وذلك يعتمد على نوع الخلية، ونوع المادة. كما يمكن للخلايا أن تقوم بفتح قنوات خاصة مثل القنوات الأيونية لفترات محدودة، للسماح بدخول أو خروج بعض المواد. انتقال المواد هنا يكون بشل تلقائي عن طريق الانتشار دون صرف أي طاقة أو نقل نشط يستهلك الطاقة.
هناك أيضا أساليب أخرى لانتقال الجزيئات والسوائل ما بين الخلايا والسائل البيني، فإلى جانب الانتشار هناك التناضح والنقل النشط وكلاهما يستهلك الطاقة تحقيق النقل.
 طالع أيضًا: تناضح
طالع أيضًا: تناضح- قانون فيك للانتشار
- نقل نشط
تخصيب اليورانيوم
تستغل ظاهرة انتشار الغازات في عملية تخصيب اليورانيوم وهي عملية تركيز اليورانيوم-235 في اليورانيوم-238. فالنسبة الطبيعية لليورانيوم-235 في اليورانيوم هي 0.7% والباقي يورانيوم-238. واليورانيوم المستخدم لتشغيل المفاعل النووي يجب أن يحتوي عل نسبة 3.5% من اليورانيوم-235 لكي يستعمل الماء كمهدئ للنيوترونات. وتتم رفع نسبة اليورانيوم 235 في اليورانيوم من 0.7% إلى 3.5% عن طريق انتشار ذرات اليورانيوم -235 واليورانيوم-238 عبر حائل مستمي ينتقلان خلاله من غرفة 1 إلى غرفة 2. يكون اليورانيوم في هيئة سادس فلوريد اليورانيوم الذي يسهل تسخينه فيتحول إلى بخاره. في البدء يكون غاز سادس فلوريد اليورانيوم في الغرفة 1 ثم ينتشر النوعان : سادس فلوريد اليورانيوم-235 وسادس فلوريد اليورانيوم-238 خلال الحائل المسامي وينتقلان إلى الغرفة 2 (الفارغة). ونظرا لأن سرعة عبور جزيئات سادس فلوريد اليورانيوم-235 تكون أسرع من سرعة انتشار سادس فلوريد اليورانيوم-238 (الأول أخف من الثاني) فنجد أن نسبة سادس فلوريد اليورانيوم-235 تكون في المخلوط أعلى من نسبته في المخلوط في الغرفة 1.
تـُكرر العملية مرارا حتى نحصل على التركيز المرغوب وهو 3.5% لليورانيوم-235. وطريقة الانتشار هي إحدى طرق تخصيب اليورانيوم، وتوجد طرق أخرى مثل طريقة المركزية الطاردة التي تستعملها إيران لتخصيب اليورانيوم.
اقرأ أيضا
مراجع
- Flow equations and frames of reference for isothermal diffusion in liquids. The Journal of Chemical Physics 33(5):1505–13. نسخة محفوظة 26 يناير 2020 على موقع واي باك مشين.
- Weiss, G. (1994). Aspects and Applications of the Random Walk. North-Holland. ISBN 0444816062. الوسيط
|CitationClass=تم تجاهله (مساعدة) - A. Einstein (1905). "Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen" (PDF). Ann. Phys. 17 (8): 549–60. Bibcode:1905AnP...322..549E. doi:10.1002/andp.19053220806. مؤرشف من الأصل (PDF) في 22 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة)
روابط خارجية
- فيديو تعليمي. (بالإنجليزية)
- شرح الانتشار نقلاً عن صفحة زاوية الأحياء (Biology corner.com). (بالإنجليزية)
- شرح خاصية الانتشار عن صفحة جامعة القدس.
- بوابة علم الأحياء
- بوابة الكيمياء
- بوابة الفيزياء
- بوابة كيمياء فيزيائية
