نزع الكبريت المهدرج
نزع الكبريت المهدرج (اختصاراً HDS من Hydrodesulfurization) هي عملية كيميائية حفزية من أجل نزع وإزالة الكبريت من المنتجات والمشتقات النفطية عن طريق الهدرجة، والتي تطبق على الغاز الطبيعي وعلى منتجات النفط المكررة مثل البنزين والكيروسين ووقود الديزل وزيت الوقود (الفيول).[1][2] يجري في العملية تحويل الكبريت الموجود في المشتقات النفطية إلى غاز كبريتيد الهيدروجين H2S (نزع مهدرج)، والذي يحول بدوره إلى عنصر الكبريت الصلب (زهر الكبريت)، أو إلى حمض الكبريتيك. تنتج كميات كبيرة من الكبريت خلال هذه العملية، ففي عام 2005 أنتج حوالي 64 مليون طن متري على نطاق العالم من الكبريت كناتج ثانوي من وحدات نزع الكبريت المهدرج في مصافي النفط.[3][4]
الهدف من نزع الكبريت هو التخفيض من انبعاثات غاز ثنائي أكسيد الكبريت (SO2) الناتجة من حرق الوقود إلى الغلاف الجوي، حيث يعد غاز SO2 من مكونات المطر الحمضي. من الأسباب المهمة الموجبة لنزع الكبريت من النفط في وحدات التكرير هو تسببه في تسمم حفازات الفلزات النبيلة مثل البلاتين أو الرينيوم في وحدات الإصلاح الحفزي التي تهدف إلى رفع رقم الأوكتان في قطفات النافثا. يقصد بتسمم الحفاز هنا ارتباط الكبريت مع الحفاز بشكل يمنعه من أداء وظيفته كما ينبغي، مما يتطلب إجراء عمليات تنشيط للحفاز وهي عمليات مكلفة.
التاريخ
على الرغم من أن التفاعلات الكيميائية المتضمنة للهدرجة الحفزية للمركبات العضوية كانت معروفة قبل عام 1897، فإن هذا الاكتشاف يعزى إلى الكيميائي الفرنسي بول ساباتييه، والذي قام بإجراء تفاعلات تثبيت للهيدروجين على الهيدروكربونات (مثل الإيثيلين والبنزين) باستخدام مسحوق ناعم من النيكل.[5][6] عن طريق ذلك تمكن ساباتييه من تحويل الهيدروكربونات غير المشبعة في الطور الغازي إلى هيدروكربونات مشبعة باستخدام غاز الهيدروجين وبوجود حفاز فلزي. تعد هذه الخطوة أساساً لعمليات الهدرجة الحفزية في الوقت الراهن.
بعد ذلك بوقت قصير، تمكن الكيميائي الألماني فيلهلم نورمان من تحويل الححموض الدهنية غير المشبعة أو الغليسريدات إلى مركبات مشبعة، وقام بعمل براءة اختراع لذلك في ألمانيا عام 1902 [7] وفي بريطانيا عام 1903.[8] مما مهد لانتشار العمليات الحفزية بشكل أوسع على نطاق العالم. جرى طرح العديد من وحدات الإصلاح الحفزي في خمسينيات القرن العشرين على مستوى تجاري وكان من ضمنها العديد من وحدات نزع الكبريت المهدرج، والتي أصبحت جزءا لا يتجزأ من مصافي النفط.
الكيمياء
تتضمن عملية نزع الكبريت المهدرج حدوث عملية تحلل هيدروجيني Hydrogenolysis، وهي نوع من تفاعلات الهدرجة التي يتم فيها تفاعل الهيدروكربونات الحاوية على ذرة غير متجانسة X مع غاز الهيدروجين يرافقه حدوث انفصام للرابطة الكيميائية C-X. بالتالي فإن ناتج التحلل الهيدروجيني تشكل الروابط C-H وH-X، أي ناتج عملية نزع الكبريت المهدرج هو غاز كبريتيد الهيدروجين. على سبيل المثال، تحدث عملية نزع الكبريت المهدرج على مركب إيثانثيول، وهو مركب كبريتي يوجد في المشتقات النفطية، فيتحول إلى الإيثان حسب المعادلة:
- C2H5SH + H2 → C2H6 + H2S
الحفازات
أغلب الحفازات المستخدمة في عملية نزع الكبريت المهدرج عبارة عن مركبات من الفلزات الانتقالية. هناك إمكانية لاستخدام حفاز وحيد مثل ثنائي كبريتيد الروثينيوم RuS2، أو مزيج ثنائي من أملاح الكوبالت والموليبدنوم، [9] مثل مركب ثنائي كبريتيد الموليبدنوم MoS2 الذي يستخدم بكميات ضئيلة.[10] يمكن استخدام حفازات أخرى من النيكل والتنغستن ويعتمد ذلك حسب طبيعة المادة المعالجة؛ كما اقترح استخدام ثنائي كبريتيد الإريديوم لهذه العملية.[11]
تضاف مواد داعمة للحفازات تتميز بأن لها مساحة سطح فعالة مرتفعة مثل الألومينا، مما يتيح من إجراء عملية توزيع لجسيمات الحفاز على كامل السطح، بالتالي نحصل على مردود حفزي أكبر.
آلية التحفيز
أظهرت الأبحاث أنه باستخدام مركب ثنائي كبريتيد الموليبدنوم كحفاز في عملية نزع الكبريت المهدرج فإن المنطقة الفعالة في التحفيز هي أطراف وجوانب سلسلة الحفاز، [12] في حين أن الدور الذي يقوم به جسم الحفاز هو كمركز لتثبيت المواقع غير المشبعة تساندياً coordinatively unsaturated site (CUS)، والتي تعرف أيضاً باسم الشاغر الأنيوني anion vacancy. فعلى سبيل المثال فإن مركبات مثل الثيوفين ترتبط إلى تلك المراكز عن طريق سلسلة من التفاعلات تفضي إلى انفصام الرابطة C-S وحدوث هدرجة للرابطة C=C. بالتالي فإن الهيدروجين هنا يقوم بأدوار عدة، فهو يولد شاغر أنيوني بإزالة الكبريتيد من الحفاز، ويقوم بهدرجة الروابط المضاعفة.
.png.webp)
وصف العملية
تجري التفاعلات الكيميائية في وحدة نزع الكبريت المهدرج على النطاق الصناعي، في مصفاة نفط مثلاً، في مفاعل كيميائي ذي سرير ثابت fixed-bed reactor عند درجات حرارة مرتفعة تتراوح بين 300 - 400°س، وعند ضغوط مرتفعة تتراوح من 30 إلى 130 جو، وبوجود حفاز من الكوبالت والموليبدنوم متموضع على قاعدة من الألومينا.
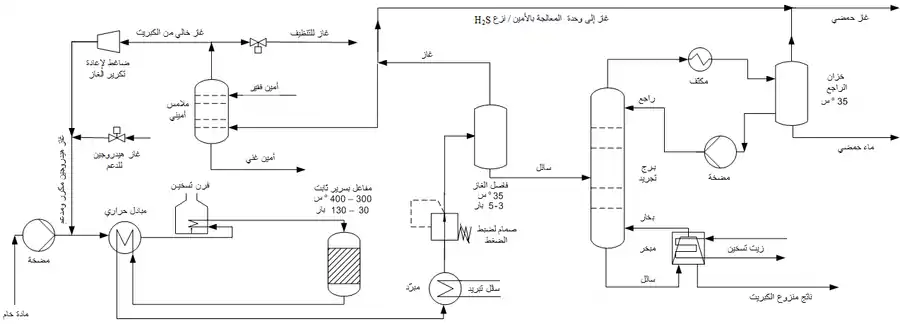
يظهر المخطط أدناه إحدى عمليات نزع الكبريت المهدرج المطبقة على المستوى الصناعي:
تدخل المادة الخام السائلة إلى الوحدة بضغط محدد عبر مضخة، وتمزج مع غاز الهيدروجين القادم من وحدة التكرير. يعمد إلى رفع درجة حرارة المزيج الناتج من السائل والغاز بالتمرير عبر مبادل حراري، وذلك قبل أن يدخل المزيج إلى فرن تسخين والذي تصل درجة الحرارة المزيج فيه من 300 إلى 400°س، مما يؤدي إلى تبخر المركبات قبل الدخول إلى المفاعل. يكون الحفاز غير متحرك ومدعم بالألومينا في المفاعل (سرير ثابت)، وهو يشكل نواة المفاعل الذي تجري فيه التفاعلات الكيميائية لنزع الكبريت المهدرج.
تبرد منتجات التفاعل جزئياً بالتمرير عبر المبادل الحراري، بعد ذلك تمرر على مبرّد إلى أن تصل إلى صمام لضبط الضغط، حيث يخفف الضغط إلى حدود 3 - 5 بار. تدخل المنتجات إلى مرحلة فصل الغاز، والتي تجري في وعاء ضغط تكون درجة الحرارة فيه 35°س. تجري عملية إعادة تكرير لغاز الهيدروجين الناتج من وحدة الفصل وذلك بتمريره على وحدة معالجة الغاز بالأمين (ملامس أميني) من أجل فصل الغازات الحمضية مثل غاز كبريتيد الهيدروجين H2S وغاز ثنائي أكسيد الكربون CO2 عن غاز الهيدروجين، نظراً للخواص القاعدية التي تملكها الأمينات. يدخل الأمين إلى الملامس الأميني وقاعديته مرتفعة، ويسمى حسب الاصطلاحات التقنية أمين فقير، ويخرج بقاعدية منخفضة (أمين غني)، والذي تجري عملية إعادة تكريره وتجديده في وحدة معالجة الغاز بالأمين الرئيسية. يدعّم غاز الهيدروجين الخالي من الكبريت والمكرر بغاز نقي قبل مزجه مجدداً مع المادة الخام.
أما بالنسبة للناتج السائل من الفاصل فإنه يدخل إلى برج تجريد stripper distillation tower ، وهو برج تقطير تعاد فيه تقطير المنتجات، بحيث تجرد من أي غاز يمكن أن يكون قد تكثف خلال العملية، ونضمن بذلك أن الناتج من أسفل هذه الوحدة يكون خالياً من الكبريت وهو الناتج النهائي. أما الغازات الناتجة من وحدة التجريد فهي غازات حمضية تحوي بالإضافة إلى الهيدروجين وكبريتيد الهيدروجين غازات الميثان والإيثان والبروبان، وبعض المكونات الأثقل، يضاف إليها غاز الهيدروجين الفائض من وحدة الفصل في الخطوة السابقة. تكثف هذه الغازات وتخزن قبل أن تنقل إلى وحدة معالجة الغاز بالأمين الرئيسية في المنشأة النفطية. في وحدة معالجة الغاز بالأمين يمرر الغاز الحمضي بسلسلة من أبراج التقطير لفصل الغازات المرافقة (هيدروجين، ميثان، إيثان) والتي تستعمل كوقود، أما كبريتيد الهيدروجين فيحول إلى كبريت فلزي عن طريق عملية كلاوس أو بتحويله إلى حمض الكبريتيك من خلال طريقة حمض الكبريتيك الرطب Wet sulfuric acid process أو بطريقة التماس.
طالع أيضاً
مراجع
- Gary, J.H. and Handwerk, G.E. (1984). Petroleum Refining Technology and Economics (الطبعة 2nd Edition). Marcel Dekker, Inc. ISBN 0-8247-7150-8. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) صيانة CS1: نص إضافي (link) - Hydrodesulfurization Technologies and CostsNancy Yamaguchi, Trans Energy Associates, William and Flora Hewlett Foundation Sulfur Workshop, Mexico City, May 29-30, 2003 [وصلة مكسورة] نسخة محفوظة 27 مايو 2008 على موقع واي باك مشين.
- Sulfur production report by the United States Geological Survey نسخة محفوظة 19 سبتمبر 2009 على موقع واي باك مشين.
- Discussion of recovered byproduct sulfur نسخة محفوظة 12 يونيو 2018 على موقع واي باك مشين.
- C.R.Acad.Sci. 1897, 132, 210
- C.R.Acad.Sci. 1901, 132, 210
- DE Patent DE141029 (Espacenet, record not available) نسخة محفوظة 11 مايو 2008 على موقع واي باك مشين.
- UK Patent GB190301515 GB190301515 (Espacenet) نسخة محفوظة 11 مايو 2008 على موقع واي باك مشين.
- Chianelli, R. R.; Berhault, G.; Raybaud, P.; Kasztelan, S.; Hafner, J. and Toulhoat, H., "Periodic trends in hydrodesulfurization: in support of the Sabatier principle", Applied Catalysis, A, 2002, volume 227, pages 83-96
- Topsøe, H.; Clausen, B. S.; Massoth, F. E., Hydrotreating Catalysis, Science and Technology, Springer-Verlag: Berlin, 1996.
-
Chianelli, R. R.; Berhault, G.; Raybaud, P.; Kasztelan, S.; Hafner, J.; Toulhoat, H. (8 March 2002). "Periodic trends in hydrodesulfurization: in support of the Sabatier principle". Applied Catalysis A: General. 227 (1–2): 83–96. doi:10.1016/S0926-860X(01)00924-3. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Daage, M.; Chianelli, R. R., "Structure-Function Relations in Molybdenum Sulfide Catalysts - the Rim-Edge Model", J. of Catalysis, 1994, 149, 414-427.
- بوابة طاقة
- بوابة الكيمياء