محرك الجينات
محرك الجينات (بالإنجليزية: Gene drive) أو أيضا الإجبار الجيني، هو تقنية في الهندسة الوراثية تسمح بنقل جين معين بطريقة فعالة على نحو تفضيلي إلى الجيل الموالي من خلال عملية التكاثر الجنسي، حتى في حالة كان الأمر يتعارض مع قوانين مندل. ظهرت هذه التقنية أول مرة في بداية القرن ال 21، وتستخدم أساسا تقنية كريسبر/CAS9. حيث أنها تساعد على تعزيز فرصة انتقال جين معين وزيادة انتشاره في ساكنة معينة.[1]
يمكن تطبيق هذه التقنية في العديد من المجالات المختلفة، من بينها منع انتشار الحشرات التي تنقل الأمراض (خاصة حشرات البعوض التي تنقل الملاريا، حمى الضنك أو فيروس زيكا)، السيطرة على الأنواع الغازية الدخيلة أو للقضاء على الأنواع المقاومة لمبيدات الأعشاب.[1][2][3] يمكن استخدام هذه التقنية أيضا لإضافة، تعطيل أو تعديل جينات ساكنة بأكملها بغرض إحداث انخفاض جذري في عدد السكان عن طريق الحد من قدرتها الإنجابية.[4] تكون تقنية محرك الجبنات فعالة فقط بالنسبة للأنواع ذات التكاثر الجنسي النشط، إذ يستحيل إستعمالها في تعديل جينات الساكنات الفيروسية أو البكتيرية. يمكن أن يحدث محرك الجينات بشكل طبيعي خلال تطور مجموعة سكانية معينة، وقد تساهم في ذلك العديد من العوامل الطبيعية التي قد تؤدي إلى تحرير المحتوى الجيني لهذه الساكنة.
الإجبار الجيني بواسطة النوكلياز هو الآلية الصناعية الأكثر شهرة والمعروفة على نحو واسع في التطوير خلال سنة 2017. ولأن هذا الإجبار الجيني يعد أهم وسيلة لتغيير وراثة بعض الجينات بشكل اصطناعي، فإن هذه التقنية تعتبر خطوة أساسية في مجال التكنولوجيا الحيوية.
هناك العديد من التحديات التي من شأنها مواجهة هذه التقنية، لاسيما تاثيرها الجيني المحتمل في حالة إطلاقها في الطبيعة، هذا الأخير الذي يثير مخاوف بيولوجية وأخلاقية كبيرة حول تطورها وكيفية إدارتها فيما بعد.
تاريخ
انطلاقا من سنة 2003، كان أوستن بيرت، عالم الوراثة التطورية في كلية لندن الإمبراطورية أول من اقترح إمكانية بناء محركات للجينات تعتمد أساسا على الجينات الطبيعية "الأنانية" (إيثار الصفات الوراثية المثالية نتيجة للانتقاء الطبيعي) التي تستخدم النوكلياز الداخلي.[4] في وقت لاحق أظهر الباحثون بالفعل أن هذه الجينات "الأنانية" يمكن أن تنتشر بسرعة عبر الأجيال المتعاقبة. أشار بيرت إلى أن هذا التأثير الجيني يمكن أن يستخدم لمنع سكان البعوض من نقل الطفيلي المسبب للملاريا أو حتى القضاء التام على عدد معين من هذا البعوض. أجريت أولى محاولات تطبيق تقنية الإجبار الجيني على أساس النوكلياز الداخلي في المختبر مع مجموعات محولة وراثيا من البعوض [5] وذباب الخل.[6][7]
بحلول أغسطس 2016، أعلنت إدارة الغذاء والدواء الأمريكية أنه "لا يوجد تأثير كبير" لخطة شركة التكنولوجيا الحيوية أوكسيتيك، الهادفة لتحريرها للزاعجة المصرية (بعوضة) المعدلة وراثيا في ولاية فلوريدا.[8] تهدف هذه الخطة إلى منع انتشار الأمراض المنقولة عن طريق البعوض، بما في ذلك فيروس زيكا. مبدأ عمل هذا التعديل الجيني يقوم على إضافة جين يعمل على قتل ذرية البعوض قبل وصولها سن التكاثر.
الإمكانيات الواعدة لهذه التقنية دفعت مؤسسة بيل وميليندا غيتس الخيرية إلى استثمار ما يعادل 75 مليون دولار في مجال محركات الجينات. حيث قدرت المؤسسة أن هذه التكنولوجيا ستكون جاهزة للاستخدام الميداني الأول بحلول عام 2029 في أفريقيا. بالرغم من ذلك قامت مؤسسة غيتس بحلول سنة 2016 بتعديل تقديراتها، حيث تخطط حاليا لإستخدامها أول مرة على مدى العامين المقبلين.[9]
بالموازات مع ذلك استثمرت "صناديق تاتا"، التي هي مؤسسة خيرية يقع مقرها بومباي، عدة ملايين من الدولارات في مشاريع محركات الجينات؛ في أفق مكافحة الملاريا بصفة خاصة.[10]
في ديسمبر 2016، رفضت حكومات العالم الدعوة إلى الوقف الاختياري العالمي لتقنيات التأثير الجيني، أثناء انعقاد اجتماع الأمم المتحدة للتنوع البيولوجي.[11]
في 19 يوليو 2017، أعلنت وكالة مشاريع البحوث المتطورة الدفاعية (داربا) عن استثمارات مالية ضخمة بقيمة 65 مليون دولار أمريكي موجهة لتطوير تقنيات تعديل الجينات، معظم هذه الأموال ستكون موجهة لتقنيات التأثير الجيني. لتصبح بذلك الوكالة أكبر مانح لبحوث الإجبار الجيني في العالم.[10] الغرض من هذه الاستثمارات هو استحداث أدوات جديدة لمكافحة انتشار السيطرة القسرية على الجينات. يمكن أن تشمل هذه التقنيات مواد كيميائية تعمل على منع تعديل الجينات أو القراء المضادة للجينات التي يمكن أن تعكس التعديل الجيني أو حتى تحصين الكائنات البرية غير المتغيرة جينيا لتكون مقاومة للإجبار الجيني.[10]
الآلية
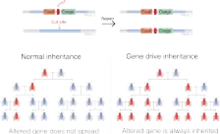
عند الأنواع التي تتكاثر جنسيا، توجد معظم الجينات في نسخ مكررة (على شكل أحاليل مختلفة)، إحداهما من تأتي من الأب والأخرى من الأم، فيكون لكل من هذه النسخ فرصة 50% لتكون موروثة(تنتقل من جيل إلى جيل). ولكي ينتشر حليل معين بين عدد كبير من السكان، يجب أن يتوفر على ميزة تطورية تزيد من فرص الأفراد لإستنساخ ونقل تلك النسخة من الجين إلى الأجيال القادمة. لذلك فإن فإن مبدأ عمل هذه التقنية يتمثل في تطويرها لآليات تعمل على رفع فرصة انتقال هذه الأحاليل لتتجاوز نسبة 50% الملاحظة عادة، ما يسمح بانتشار الجينات بين أفراد الساكنة، حتى في حالة عدم توفرها على ميزات متطورة أو أيضا في حالة تقليلها من قدره كل كائن على التكاثر. من خلال تغيير وراثة بعض الجينات على نحو مماثل، يمكن استخدام تقنية الإجبار الجيني الاصطناعي لنشر التغيرات عبر السكان.
حالياً يمكن للعلماء اختيار جين ذي خصائص معينة، كجين العقم الذكري على سبيل المثال، ونقله عبر أفراد معيّنة من الجماعة ليتم توارثه من طرف الأبناء، هذا الأمر الذي يكون مستبعدا ونادر الحدوث (أي انتقال الصفات غير المرغوبة) في الظروف الطبيعية؛ بوجود ظاهرة الانتقاء الطبيعي.
الآليات الجزيئية
على المستوى الجزيئي، يعمل الإجبار الجيني عن طريق الأنوكلياز الداخلي على قطع الصبغيات وإجبار الخلية على إصلاح الأضرار الناجمة عن نسخ تسلسل الجينات الإجبارية على الشريط المتضرر الذي ينتج نسختين متطابقتين على شريطي الصبغي. هذه التقنية هي مشتقة من تقنيات تعديل الجينوم، حيث تستخدم حقيقة أن الفواصل المزدوجة للشريطين يتم إصلاحها في كثير من الأحيان عن طريق التأشيب المتماثل إذا كان الجين متواجدا على كلا الشريطين. في حالات نادرة يتم الإصلاح بواسطة نهاية الروابك الغير متماثلة، في هذه الحالة بالذات الإجبار لا يعمل. لتحقيق هذا الهدف، يجب أن تتكون وحدات جين النوكلياز الداخلي من عنصرين مترابطين: سواء نوكلياز داخلي مؤلف أو نوكلياز داخلي موجهة بواسطة الحمض النووي الريبي (كمثال : Cas9 أو Cpf1). للحصول على وظيفة الانتشار التلقائي للجين، يجب أن يحتوي تسلسل الإصلاح هذا على تسلسل نوكلياز داخلي على الأقل. يتسبل استهداف الجينات المعبر عنها، بإجبارها على الانطفاء (الإسكات الجيني). بذلك يمكن إدخال تسلسلات إضافية في الجين الذي تم إجباره لترميز وظائف جديدة.
بالتالي، يؤدي إدخال "الجينات المجبرة" في الجينوم إلى انتشارها التلقائي في ذرية الأفراد. كل فرد يرث نسخة من الجين ذي النوع "البري" و"الإجباري" لن ينقل لذريته سوى "الجين الإجباري". إذا كان الجين موجودا بالفعل في البويضة (على سبيل المثال عندما يتم اكتسابه من أحد الوالدين)، فإن جميع أمشاج الفرد تحمل الجين (بدلا من 50% في حالة الجين العادي).
تطبيقات خارج المختبر
مشروع بريداتور فري 2050
في يوليو 2016، قدم رئيس وزراء نيوزيلندا مشروع بريداتور فري 2050، الذي هو برنامج حكومي يسعى بحلول سنة 2050 للقضاء على ثمانية أنواع من الحيوانات الغازية المفترسة للثديات (الفئران، قصيرة الذنب والأبوسوم) في نيوزيلندا.[12][13] بحلول يناير 2017، أعلن أن تكنولوجيا محرك الجينات ستستخدم في هذا المشروع.[13]
افريقيا
يأمل فريق من الباحثين يتخذ من المملكة المتحدة مقرا له، أن يبدأ انطلاقا من سنة 2024 إجراء اختبارات ميدانية للتقنية ضد بعض أنواع البعوض التي تعرف على أنها ناقلات للملاريا، بصفة خاصة أنوع الأنوفيلز الغامبية، التي تعد الناقل الرئيسي للملاريا في أفريقيا.[10]
انظر أيضًا
مراجع
- (بالإنجليزية) « U.S. researchers call for greater oversight of powerful genetic technology », في Science | AAAS, 2014-07-17 [النص الكامل (pages consultées le 2017-11-22)]
- (بالإنجليزية) Kevin M. Esvelt, Andrea L. Smidler, Flaminia Catteruccia et George M. Church, « Concerning RNA-guided gene drives for the alteration of wild populations », في eLife, vol. 3, 2014-07-17, ص. e03401 ISSN 2050-084X [النص الكامل, lien PMID, lien PMCID, lien DOI (pages consultées le 2017-11-22)]
- M. Benedict, P. D'Abbs, S. Dobson et M. Gottlieb, « Guidance for Contained Field Trials of Vector Mosquitoes Engineered to Contain a Gene Drive System: Recommendations of a Scientific Working Group », في Vector-Borne and Zoonotic Diseases, vol. 8, no 2, 2008-04-01, ص. 127–166 ISSN 1530-3667 [النص الكامل, lien DOI (pages consultées le 2017-11-22)]
- (بالإنجليزية) Austin Burt, « Site-specific selfish genes as tools for the control and genetic engineering of natural populations », في Proceedings of the Royal Society of London B: Biological Sciences, vol. 270, no 1518, 2003-05-07, ص. 921–928 ISSN 0962-8452 [النص الكامل, lien PMID, lien PMCID, lien DOI (pages consultées le 2017-11-22)]
- (بالإنجليزية) Nikolai Windbichler, Miriam Menichelli, Philippos Aris Papathanos et Summer B. Thyme, « A synthetic homing endonuclease-based gene drive system in the human malaria mosquito », في Nature, vol. 473, no 7346, 2011, ص. 212–215 [النص الكامل, lien PMID, lien PMCID, lien DOI].
- (بالإنجليزية) Yuk-Sang Chan, Daniel A. Naujoks, David S. Huen et Steven Russell, « Insect Population Control by Homing Endonuclease-Based Gene Drive: An Evaluation in Drosophila melanogaster », في Genetics, vol. 188, no 1, 2011-05-01, ص. 33–44 ISSN 0016-6731 [النص الكامل, lien PMID, lien PMCID, lien DOI (pages consultées le 2017-11-22)].
- Yuk-Sang Chan, David S. Huen, Ruth Glauert et Eleanor Whiteway, « Optimising Homing Endonuclease Gene Drive Performance in a Semi-Refractory Species: The Drosophila melanogaster Experience », في PLOS ONE, vol. 8, no 1, 2013-01-18, ص. e54130 ISSN 1932-6203 [النص الكامل, lien PMID, lien PMCID, lien DOI (pages consultées le 2017-11-23)].
- (بالإنجليزية) « FDA Approves Genetically Modified Mosquitoes For Release In Florida », في Popular Science, 5 août 2016 [النص الكامل (pages consultées le 2017-11-23)].
- (بالإنجليزية) Antonio Regalado, « Bill Gates doubles his bet on wiping out mosquitoes with gene editing », في MIT Technology Review, 2016 [النص الكامل (pages consultées le 2017-11-23)].
- (بالإنجليزية) « US defence agencies grapple with gene drives », في Nature, juillet 2017 [النص الكامل (pages consultées le 2017-11-23)].
- (بالإنجليزية) Ewen Callaway, « ‘Gene drive’ moratorium shot down at UN biodiversity meeting », في Nature, décembre 2016 [النص الكامل, lien DOI (pages consultées le 2017-11-23)].
- Stockton, Nick (July 27, 2016). "How New Zealand Plans to Kill Its (Non-Human) Invasive Mammals". WIRED. مؤرشف من الأصل في 10 يوليو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Predator Free NZ - Expert Q&A". Scoop. 17 January 2017. مؤرشف من الأصل في 08 يوليو 2018. اطلع عليه بتاريخ 20 نوفمبر 2016. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ الوصول=, |تاريخ أرشيف=(مساعدة)
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي
