كلوريد الفضة
كلوريد الفضة هو مركب كيميائي له الصيغة الكيميائية AgCl؛ ويوجد في الشروط القياسية على شكل صلب بلوري أبيض اللون. يوجد المركب على شكل معدن في الطبيعة اسمه كلورارجيريت.
| كلوريد الفضة | |
|---|---|
 كلوريد الفضة | |
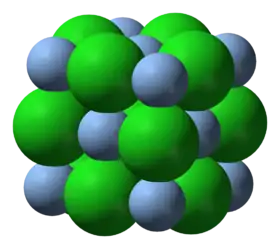 كلوريد الفضة | |
| الاسم النظامي (IUPAC) | |
Silver(I) chloride | |
| المعرفات | |
| رقم CAS | 7783-90-6 |
| بوب كيم (PubChem) | 24561 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | AgCl |
| كتلة مولية | 143.32 غ.مول−1 |
| المظهر | White Solid |
| الكثافة | 5.56 g cm−3 |
| نقطة الانصهار | 455 °س، 728 °ك، 851 °ف |
| نقطة الغليان | 1547 °س، 1820 °ك، 2817 °ف |
| الذوبانية في الماء | 520 μg/100 g at 50 °C |
| الذوبانية | soluble in أمونياك, conc. حمض الهيدروكلوريك, conc. حمض الكبريتيك, alkali سيانيد, كربونات الأمونيوم, KBr, ثيوكبريتات الصوديوم; insoluble in كحول, dilute حمضs. |
| معامل الانكسار (nD) | 2.071 |
| البنية | |
| البنية البلورية | كلوريد الصوديوم |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
−127 kJ·mol−1[1] |
| إنتروبيا مولية قياسية S |
96 J·mol−1·K−1[1] |
| المخاطر | |
| صحيفة بيانات سلامة المادة | Salt Lake Metals |
| NFPA 704 |
0
2
0
|
| مركبات متعلقة | |
| أنيونات أخرى | فلوريد الفضة الأحادي, بروميد الفضة, يوديد الفضة |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التحضير
ويتم تصنيع كلوريد الفضة بسهولة عن طريق المزج بين المحاليل المائية من نترات الفضة وكلوريد الصوديوم.
الخواص
يوجد المركب في الشروط القياسية على شكل بلورات بيضاء اللون؛ ولا ينحل المركب عملياً في الماء.
ينحل راسب كلوريد الفضة عند إضافة محاليل حاوية على ربيطات مثل الكلوريد أو السيانيد أو ثلاثي فينيل الفوسفين أو ثيوكبريتات أو ثيوسيانات أو الأمونيا.
لكلوريد الفضة حساسية للضوء؛ إذ يسود لونه ويتفكك عند التعرض للضوء.
الاستخدمات
يعد قطب كلوريد الفضة من الأقطاب المعيارية في الكيمياء الكهربائية.
المراجع
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. صفحة A23. ISBN 0-618-94690-X. الوسيط
|CitationClass=تم تجاهله (مساعدة)
في كومنز صور وملفات عن: كلوريد الفضة
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.

