غلاف تكافؤ
غلاف التكافؤ أو حزمة التكافؤ هو الغلاف الأخير في الذرة، والذي يحتوى على الإلكترونات التي تساهم في أي تفاعل تدخل فيه الذرة، والتفاعلات التي تحدث بين الروابط بين الذرات.[1][2][3] تسمى الإلكترونات التي توجد في غلاف التكافؤ بإلكترونات التكافؤ. وقد كان الكيميائي جيلبرت نيوتن لويس هو أول من حاول تطوير النظرية التي تفسر مشاركة إلكترونات غلاف التكافؤ في الروابط الكيميائية. وقد قام لينوس باولينج بتعميم وتمديد النظرية بعد ظهور ميكانيكا الكم. ولاكن تميل الغازات النبيلة لأن يكون بها 8 إلكترونات في الغلاف الخارجي (فيما عدا الهيليوم، والذي يملأ غلافه الخارجى 2 إلكترون). وهذا يتماشى مع نظرية الثمانيات (تسمى أيضا ثمانيات نيولاندز) والتي يمكن أن تطبق على عناصر الدورة الثالثة والرابعة. ومن منطلق المدارات الذرية فإن الإلكترونات الثمانية الموجودة في غلاف التكافؤ موزعة في كلآتى 2 في المدار s، و2 في كل من مدارات p الثلاثة.
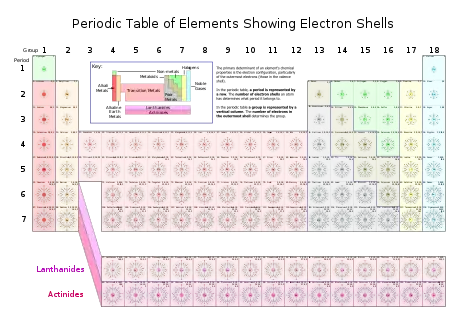
المركبات العضوية المعدنية التي تضم الفلزات الانتقالية، يتكون غلاف التكافؤ من إلكترونات المدار s، p، والتي تبلغ 8 إلكترونات، كما أن لها 10 إلكترونات موزعة 2 في كل من المدارات d الخمسة والتي تصبح 18 إلكترون والتي تكون غلاف مكتمل لهذه العناصر. والتي ترجع لنظرية الثمانية عشر.
أمثلة
في ذرة الهيدروجين يوجد إلكترون واحد فقط في المدار الأول (1) وهذا المدار يكتمل بوجود إلكترونين، لذا يُعتبر في تلك الحالة الإلكترون الوحيد ذاك هو إلكترون التكافؤ.
في ذرة الليثيوم ، يوجد إلكترونان في المدار الأول، وهو بذلك يعد مداراً مكتملاً، وبالمدار الثاني الذي يسع 8 إلكترونات، يوجد إلكترون واحد فقط وبذلك يكوّن هو حزمة التكافؤ.
في ذرة الكاربون، يوجد إلكترونين في المدار الأول، وأربعة إلكترونات في المدار الثاني الذي يسع 8 إلكترونات وبذلك تكون تلك الأربعة حزمة التكافؤ.
في ذرة الألومنيوم، يوجد إلكترونين في المدار الأول، وثمانية في المدار الثاني وبذلك يكون المدار الثاني مكتملاً أيضاً، وفي المدار الثالث (3) الذي يسع 8 إلكترونات توجد ثلاثة إلكترونات، وبذلك تكون تلك الثلاث حزمة التكافؤ. (المدار الثالث يسع عشرة إلكترونات فوق الثمانية التي ذكرناها ولكنها تمتلئ بعد وجود إلكترونين في المدار الرابع وتلك خصيصة للمدارات يمكنك مطالعتها في مقالة التوزيع الإلكتروني)
حزمة التكافؤ هي المسؤولة عن التفاعلات الكيمائية المختلفة. ففي ذرة الملح، أو كلوريد الصوديوم، تتفاعل ذرة من الصوديوم مع ذرة من الكلورين كالآتي:
تحمل ذرة الصوديوم إحدى عشر إلكتروناً، اثنان في المدار 1 وثمانية في المدار 2 وواحداً في المدار 3، والأخير ذلك يمثل حزمة التكافؤ. تحمل ذرة الكلورين سبعة عشر إلكتروناً، اثنان في المدار 1 وثمانية في المدار 2 وسبع في المدار الثالث الذي يسع ثمانية، وبالتالي تكون هذه الإلكترونات السبعة هي حزمة التكافؤ.
كما يبدو فإن الصوديوم إذا تخلص من الإلكترون الموجود في حزمة التكافؤ ستصبح مداراته كلها مكتملة أو فارغة، وعلى العكس منه الكلورين، فإذا حصل على إلكتروناً واحدً سيملأ حزمة التكافؤ ليصبح مداراً متكتملاً.
يتم التفاعل إذن عبر حصول ذرة الكلورين على إلكترون من ذرة الصوديوم ليكوّنا بذلك كلوريد الصوديوم وهو ملح الطعام الذي نتناوله كل يوم.
الغلاف المفتوح
الغلاف المفتوح هو غلاف التكافؤ غير الممتلئ إلكترونيا أي أن هناك نقصا في الإلكترونات به أو أنه لم يشارك بكامل إلكتروناته التكافؤية في تشكيل الروابط الكيميائية مع ذرات أو جزيئات أخرى
اقرأ أيضا
مراجع
- Barkla, Charles G. (1911). "XXXIX.The spectra of the fluorescent Röntgen radiations". Philosophical Magazine. 22 (129): 396. doi:10.1080/14786440908637137.
Previously denoted by letters B and A (...). The letters K and L are, however, preferable, as it is highly probable that series of radiations both more absorbable and more penetrating exist.
الوسيط|CitationClass=تم تجاهله (مساعدة) - Jue, T. (2009). "Quantum Mechanic Basic to Biophysical Methods". Fundamental Concepts in Biophysics. Berlin: Springer. صفحة 33. ISBN 1-58829-973-2. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Re: Why do electron shells have set limits ?madsci.org, 17 March 1999, Dan Berger, Faculty Chemistry/Science, Bluffton College نسخة محفوظة 05 يونيو 2017 على موقع واي باك مشين.
وصلات خارجية
- بوابة ميكانيكا الكم
- بوابة الكيمياء
- بوابة كيمياء فيزيائية
- بوابة الفيزياء
