خلية جذعية مستحثة
الخلايا الجذعية المستحثة[1] (بالإنجليزية: Induced Stem Cells) وتُدعى اختصاراً iSC، هي نوع من الخلايا الجذعية، يتم اشتقاقه اصطناعيًا من خلايا غير وافرة القدرة، عادة من خلايا جسدية بالغة، عن طريق إجبارها على تعبير جينات خاصة.
تشبه الخلايا الجذعية المستحثة وافرة القدرة الخلايا الجذعية وافرة القدرة في العديد من الجوانب، مثل الخلايا الجذعية الجنينية، مثل تعبير جينات وبروتينات خاصة بالخلايا الجذعية، زمن التضاعف، تشكيل أجسام مضغية الشكل وتشكيل الأورام المسخية.
تم إنتاج الخلايا الجذعية المستحثة وافرة القدرة للمرة الأولى عام 2006 من خلايا فأرية وعام 2007 من خلايا بشرية خلال سلسلة تجارب قام بها طاقم شينيا ياماناكا في جامعة كيوتو، اليابان، وطاقم جيمس تومسون في جامعة ويسكونسين-ماديسون. إثر بحثها في مجال الخلايا الجذعية المستحثة وافرة القدرة، حازت د. نانسي باخمان، من أونيونتا، نيويورك على جائزة وولف في الطب لعام 2012 (مع جون ب. غوردون).[2][3][4] بسبب اكتشافه الخلايا الجذعية المستحثة وافرة القدرة (ولأنه انتج أول خط خلايا جذعية جنينية)، حاز جيمس تومسون على جائزة المركز الطبي ألباني للبحوث البيوطبية لعام 2011، و جائزة الملك فيصل الدولية لعام 2011، والتي شاركها مع ياماناكا. في عام 2012، حاز ياماناكا وباحث الخلايا الجذعية جون غوردون على جائزة نوبل في الفيزيولوجيا أو الطب "على الاكتشاف أن الخلابا البالغة يمكن إعادة برمجتها لتكون وافرة القدرة".[5]
يشكل ابتكار الخلايا الجذعية المستحثة وافرة القدرة خطوة هامة في بحث الخلايا الجذعية، حيث أنها يمكن أن تمنح الباحثين الفرصة للحصول على خلايا جذعية وافرة القدرة، نوع خلايا مهم للأبحاث ويحامل أن يكون له دور علاجي، دون استخدام الأجنة المثير للجدل.
إنتاج الخلايا الجذعية المستحثة وافرة القدرة
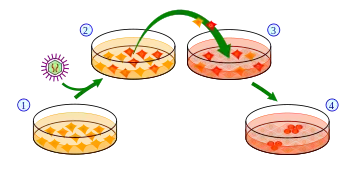
عادة ما يتم الحصول على الخلايا الجذعية المستحثة وافرة القدرة عن طريق تعداء بعض الجينات المتعلقة بالخلايا الجذعية إلى خلايا غير وافرة القدرة، مثل الخلايا الجلدية البالغة.
الجيل الأول
تم إنتاج الخلايا الجذعية المستحثة وافرة القدرة لأول مرة على يد طاقم شينيا ياماناكا في جامعة كيوتو، في اليابان عام 2006. اختار ياماناكا 24 جينًا تم تشخيصهم كجينات مهمة في الخلاية الجذعية الجنينية وفي الحفاظ على صفة تعدد القدرة لدى الخلايا، واستعمل فيروسات قهقرية لتنبيغ خلايا جلدية فأرية مع مجموعة من هذه الجينات. في كل مرة، تم إزالة جين معين وتم فحص المستعمرات الخلوية لرؤية هل منظرها يشبه شكل الخلايا الجذعية. تم تشخيص 10 جينات مهمة والتي دون إدخالها تفشل الطريقة. بالنهاية وجدوا أن هناك 4 جينات ضرورية للحصول على خلايا جذعية وافرة القدرة; Oct-3/4، SOX2، c-Myc، وKlf4.
إنتاج من خلايا جلدية إنسانية
في نوفمبر 2007، تم تحقيق خطوة عملاقة وهي إنتاج خلايا جذعية مستحثة وافرة القدرة من خلايا إنسانية بالغة; نشرت دراستان مستقلتان من مجوعتي بحث مختلفتين نتائجهما - الأولى في مجلة ساينس من قبل جيمس تومسون من جامعة ويسكونسين-ماديسون[6] والأخرى في مجلة سيل من قبل شيتيا ياماناكا وزملائه في جامعة كيوتو، اليابان.[7]
أبحاث طبية
ما زالت مهمة إنتاج الخلايا الجذعية تشكّل تحدّيًا بسبب المشاكل الستّ المذكورة أعلاه. الإشكال الأساسي الذي يجب التغلب عليه هو التضارب بين الحاجة لنجاعة الإنتاج وبين الدمج الجيني. فإن معظم الطرق التي لا تعتمد على اندماج الجينات المنقولة هي طرق غير ناجعة، بينما تلك الطرق التي تعتمد على اندماج الجينات المنقولة فتواجه مشاكل إعادة البرمجة غير الكاملة ونشوء الورم.
نمذجة الأمراض وتطوير الأدوية
إحدى الميزات الجذّابة للخلايا الجذعية المستحثة وافرة القدرة البشرية هي القدرة على استخراجها من مرضى بالغين لدراسة الأسس الخليوية للأمراض البشرية الموروثة. لأن الخلايا الجذعية المستحثة وافرة القدرة هي خلايا وافرة القدرة وتتجدد تلقائيًا، فهي تشكّل نظريًا مصدرًا غير محدود لخلايا مشتقة من المريض والتي يمكن تحويلها إلى أي نوع خلايا في الجسم. هذه ميزة مهمة لأن أنواعاً عديدة من الخلايا البشرية المشتقة من البشر تتوقف عن النمو بعد بضع من الزراعات الثانوية في المختبر. وقد أُنتجت خلايا جذعية مستحثة وافرة القدرة لمجموعة واسعة من الأمراض الوراثية البشرية مثل متلازمة داون، داء الكلية متعددة الكيسات، ومتلازمات اضطراب نظم القلب الوراثية.[8][9][10] في عديد من الحالات، تظهر الخلايا الجذعية المستحثة وافرة القدرة المشتقة من المريض عيوباً خليوية غير موجودة في الخلايا الجذعية المستحثة وافرة القدرة المشتقة من الأصحاء، وتوفّر فكرة عن الفيزيولوجيا المرضية للمرض.[11] في سنة 2012 أُقيم مشروع تعاون دولي، ستيم بانك (StemBANCC)، لبناء مجموعة من خطوط الخلايا الجذعية المستحثة وافرة القدرة لفحص أدوية لمجموعة متنوعة من الأمراض.
المراجع
- Baker, Monya (2007-12-06). "Adult cells reprogrammed to pluripotency, without tumors". Nature Reports Stem Cells. doi:10.1038/stemcells.2007.124. مؤرشف من الأصل في 07 يناير 2017. اطلع عليه بتاريخ 11 ديسمبر 2007. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Whitehead Member Rudolf Jaenisch honored for groundbreaking stem cell research". mit. مؤرشف من الأصل في 10 أبريل 2012. اطلع عليه بتاريخ 01 يناير 2012. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "THE 2011 WOLF FOUNDATION PRIZE IN MEDICINE". مؤرشف من الأصل في 11 فبراير 2012. اطلع عليه بتاريخ أكتوبر 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - "Nobel Prize in Medicine 2012 Press release". Nobel Foundation. مؤرشف من الأصل في 13 أغسطس 2018. اطلع عليه بتاريخ 08 أكتوبر 2012. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "The Nobel Prize in Physiology or Medicine – 2012 Press Release". Nobel Media AB. 8 October 2012. مؤرشف من الأصل في 13 أغسطس 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Yu J, Vodyanik MA; et al. (2007). "Induced Pluripotent Stem Cell Lines Derived from Human Somatic Cells". ساينس. 318 (5858): 1917–1920. doi:10.1126/science.1151526. PMID 18029452. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة) - Takahashi K; et al. (2007). "Induction of Pluripotent Stem Cells from Adult Human Fibroblasts by Defined Factors". Cell. 131 (5): 861–872. doi:10.1016/j.cell.2007.11.019. PMID 18035408. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة) - Park, IH; Arora, N; Huo, H; Maherali, N; Ahfeldt, T; Shimamura, A; Lensch, MW; Cowan, C; Hochedlinger, K; Daley, GQ (Sep 5, 2008). "Disease-specific induced pluripotent stem cells". Cell. 134 (5): 877–86. doi:10.1016/j.cell.2008.07.041. PMC 2633781. PMID 18691744. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Freedman, BS; Lam, AQ; Sundsbak, JL; Iatrino, R; Su, X; Koon, SJ; Wu, M; Daheron, L; Harris, PC; Zhou, J; Bonventre, JV (October 2013). "Reduced ciliary polycystin-2 in induced pluripotent stem cells from polycystic kidney disease patients with PKD1 mutations". Journal of the American Society of Nephrology : JASN. 24 (10): 1571–86. doi:10.1681/ASN.2012111089. PMID 24009235. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Shinnawi, Rami; Gepstein, Lior (2014-07-31). "iPCS Cell Modeling of Inherited Cardiac Arrhythmias". Current Treatment Options in Cardiovascular Medicine (باللغة الإنجليزية). 16 (9): 331. doi:10.1007/s11936-014-0331-4. ISSN 1092-8464. مؤرشف من الأصل في 16 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Grskovic, M; Javaherian, A; Strulovici, B; Daley, GQ (Nov 11, 2011). "Induced pluripotent stem cells--opportunities for disease modelling and drug discovery". Nature reviews. Drug discovery. 10 (12): 915–29. doi:10.1038/nrd3577. PMID 22076509. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة علم الأحياء
- بوابة تقانة
- بوابة تقانة حيوية
- بوابة طب
- بوابة علم الأحياء الخلوي والجزيئي
