خلية جذعية جنينية
الخلايا الجذعية الجنينية (بالإنجليزية: Embryonic stem cell أو ES) هي الخلايا الجذعية المحفزة المستمدة من الكتلة الخلوية الداخلية من الكيسة الأريمية، وهي الجنين في مراحله المبكرة.[1] الأجنة البشرية تصل إلى مرحلة الكيسة الأريمية بفترة 4 إلى 5 أيام بعد التخصيب، وتتكون في هذا الوقت من 50 إلى 150 خلية. عزل الأرومة المضغية أو الكتلة الخلوية الداخلية (ICM) يقود إلى اتلاف الأجنة البشرية المخصبة، مما يثير قضايا أخلاقية.
| خلية جذعية جنينية | |
|---|---|
| تفاصيل | |
| المكتشف | مارتن إيفانز ، وماثيو كوفمان ، وغيل ر. مارتن |
| نوع من | خط خلية ، وخط الخلايا الجذعية |
| معرفات | |
| ترمينولوجيا هستولوجيكا | H1.00.01.0.00030 |
| FMA | 82841 |
| ن.ف.م.ط. | A11.872.700.250 |
| ن.ف.م.ط. | D053595 |
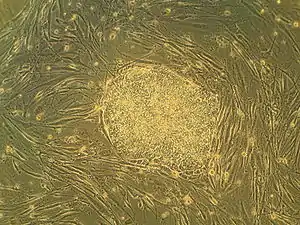
الخصائص
يتم تمييز الخلايا الجذعية الجنينية عن طريق اثنين من الخصائص المتميزة :
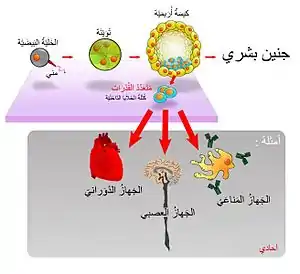
ان الخلايا الجذعية الجنينية المحفزة قادرة على التمايز في جميع المشتقات من طبقات التبرعم الثلاثة الأساسية : الأديم الظاهر, الأديم الباطن، والأديم المتوسط. وهذه تشمل كل أنواع الخلايا في الجسم البالغ التي يبلغ عددها أكثر من 220 نوع. تعدد القدرات يميز الخلايا الجذعية الجنينية من الخلايا الجذعية البالغة الموجودة في البالغين، في حين أن الخلايا الجذعية الجنينية يمكن أن تولد كل أنواع الخلايا في الجسم، فان الخلايا الجذعية البالغة هي متعددة الامكانات ويمكن ان تنتج عدد محدود من أنواع الخلايا فقط.
بالإضافة إلى ذلك، وفي ظل ظروف محددة، فإن الخلايا الجذعية الجنينية قادرة على التكاثر بنفسها إلى ما لا نهاية. هذا يسمح بتوظيف الخلايا الجذعية الجنينية كأدوات مفيدة لكل من الأبحاث والطب التجديدي، لأنها يمكن ان تنتج أعدادا لا حدود لها من نفسها لمواصلة البحث أو للاستخدام السريري.
بسبب مرونتها وقدرتها غير المحدودة لاحتمال التجديد الذاتي، تم اقتراح العلاج بالخلايا الجذعية الجنينية للطب التجديدي واستبدال الأنسجة بعد الإصابة أو المرض. الأمراض التي يحتمل أن تعالج بواسطة الخلايا الجذعية المحفزة تشمل عددا من أمراض الدم والجهاز المناعي المرتبطة بالوراثة، والسرطان، والاضطرابات؛ مثل مرض السكري للأطفال؛ وباركنسون؛ والعمى واصابات الحبل الشوكي. بالإضافة إلى المخاوف الأخلاقية من العلاج بالخلايا الجذعية (انظر الخلاف حول الخلية الجذعية)، هناك مشكلة تقنية في مرض الطعم ضد المضيف المرتبط بزرع الخلايا الجذعية الخيفية. ومع ذلك، قد يكون حل هذه المشاكل المرتبطة بالتوافق النسيجي باستخدام الخلايا الجذعية البالغة ذاتية المنح، والاستنساخ العلاجي، وبنوك الخلايا الجذعية ومؤخرا عن طريق إعادة برمجة الخلايا الجسدية مع عوامل محددة (مثل الخلايا المحفزة المستحثة). الاستخدامات المحتملة الأخرى للخلايا الجذعية الجنينية تشمل التحقيق في التنمية البشرية المبكرة، ودراسة الامراض الوراثية وكما هو الحال في النظم المختبرية لاختبار علم السموم.
البحوث التاريخية والتطورات
في عام 1964، عزل الباحثون نوع وحيد من الخلية من سرطانة مسخية, وقد عرف الآن ان هذا الورم مستمد من الخلية العروسية. هذه الخلايا المفصولة عن السرطانة المسخية تكاثرت ونمت في زرع الخلايا باعتبارها خلية جذعية والتي تعرف الآن باسم خلايا سرطانة جنينية.[3] على الرغم من أن التشابه في التشكل والتمايز المحتمل (تعدد القدرات) أدى إلى استخدام الخلايا الجذعية الجنينية كما في النموذج المختبري لأغراض تنمية فأر مبكرا،[4] إلا أن الخلايا الجذعية الجنينية تخفي الطفرات الوراثية وفي كثير من الأحيان الكروموسومات غير الطبيعية التي تراكمت خلال تطور السرطانة المسخية. هذه الانحرافات الوراثية أكدت كذلك ضرورة القدرة على زرع الخلايا متعددة القدرات مباشرة من الكتلة الخلوية الداخلية.
في عام 1981, كانت الخلايا الجذعية الجنينية (خلايا ES) وبشكل مستقل مستمدة اولا من أجنة الفئران بواسطة مجموعتين. نشر مارتن إيفانز وماثيو كوفمان من قسم علم الوراثة، في جامعة كامبريدج لأول مرة في يوليو، وكشفا عن تقنية جديدة لزراعة أجنة الفئران في الرحم للسماح بزيادة عدد الخلايا، مما يسمح باستمداد الخلايا الجذعية الجنينية من هذه الأجنة.[5] نشرت غيل ر. مارتن، من قسم التشريح في جامعة كاليفورنيا، سان فرانسيسكو، ورقة عملها في ديسمبر والتي صاغت فيها مصطلح "الخلايا الجذعية الجنينية".[6] وأظهرت فيها أن الأجنة يمكن زراعتها في المختبر ويمكن للخلايا الجذعية الجنينية أن تستمد من هذه الأجنة. في عام 1998، حدث تقدم جديد في المعرفة عندما اجرى الباحثون برئاسة جيمس تومسون من جامعة ويسكونسن ماديسون، ولأول مرة تقنية لعزل وزراعة الخلايا الجذعية الجنينية البشرية في مستنبت خلايا.[7]
تقنيات وظروف الخلية الجنينية الجذعية المستمدة والمستنبتة
يتم استمداد الخلايا الجذعية الجنينية من كتلة الخلايا الداخلية للجنين المبكر، والمكتسبة من الحيوان الأم (المصدر) المانحة. وذكر مارتن إيفانز وماثيو كوفمان التقنية التي تؤخر زرع الجنين وتسمح للكتلة الخلية الداخلية بالزيادة. وتشمل هذه العملية إزالة مبايض الأم المانحة ومداواتها بجرعات مع البروجستيرون، مغيرا بذلك بيئة الهرمون، مما يتسبب ببقاء الأجنة حرة في الرحم. بعد 4 إلى 6 أيام من هذه الزراعة داخل الرحم، يتم حصاد الأجنة وتزرع في مستنبت المختبر حتى تشكل كتلة الخلية الداخلية "هياكل البويضة مثل الأسطوانة ", التي تنفصل إلى خلايا منفردة، وتطلى على الخلايا الليفية المعالجة مع ميتومسين سي (لمنع الانقسام الفتيلي في الخلايا الليفية). يتم إنشاء خطوط الخلايا المستنسخة بواسطة انماء خلية واحدة. وأظهر ايفانز وكوفمان أن الخلايا التي نمت انطلاقا من هذه الزراعات يمكن أن تشكل ورم مسخي واجسام مضغية الشكل، وتتمايز في المختبر، وتشير كلها إلى الخلايا متعددة القدرات.[5]
استمدت غيل مارتن الخلايا الجذعية الجنينية وزرعتها بشكل مختلف. قامت بإزالة الأجنة من الام المانحة في حوالي 76 ساعة بعد التزاوج وزرعتها خلال الليل في الوسائط التي تحتوي على المصل. في اليوم التالي، قالت انها أزالت كتلة الخلية الداخلية من أواخر الكيسة الأريمية باستخدام الجراحة المجهرية. الكتلة الخلوية الداخلية المستخرجة والتي تمت زراعتها في الخلايا الليفية تعالج مع ميتوميسين سي في الوسائط التي تحتوي على المصل وكانت مشروطة من قبل الخلايا الجذعية الجنينية. بعد أسبوع تقريبا، نمت مستعمرات الخلايا. نمت هذه الخلايا في مزرعة الخلايا وأظهرت خصائص متعددة الإمكانات، كما يدل على ذلك القدرة على تكوين ورم مسخي، والتمايز في المختبر، وتشكيل اجسام مضغية الشكل. وأشار مارتن إلى هذه الخلايا كخلايا جذعية جنينية.[6]
ومن المعروف الآن أن الخلايا المغذية توفر عامل مثبط لأبيضاض الدم (LIF) ويوفر المصل بروتينات تخلق العظام (BMPs) الضرورية لمنع الخلايا الجذعية الجنينية من التمايز.[8][9] وهذه العوامل في غاية الأهمية لكفاءة الخلايا الجذعية الجنينية المستمدة. وعلاوة على ذلك، فقد تبين أن سلالات الفئران المختلفة لها كفاءات مختلفة لعزل الخلايا الجذعية الجنينية.[10] الاستخدامات الحالية للخلايا الجذعية الجنينية من الفئران تتضمن توليد فئران معدلة وراثيا، بما في ذلك الفئران المضروبة بقوة. هناك حاجة لخلايا محددة متعددة القدرات للمريض لعلاج الإنسان. تكاثر الخلايا الجذعية الجنينية البشرية أكثر صعوبة ويواجه قضايا أخلاقية. لذلك، بالإضافة إلى أبحاث الخلايا الجذعية الجنينية البشرية، تركز مجموعات كثيرة على توليد الخلايا الجذعية متعددة القدرات المستحثة (خلايا iPS).[11]
التلوث بواسطة الكواشف الكيميائية المستخدمة في زرع الخلايا
نشرت مجلة طب الطبيعة في طبعتها على الإنترنت دراسة في 24 يناير 2005 التي جاء فيها أن الخلايا الجذعية الجنينية البشرية المتاحة للبحوث الممولة فيدراليا ملوثة بجزيئات غير بشرية من وسط الزراعة المستخدم لنمو الخلايا.[12] وهو أسلوب شائع لاستخدام خلايا الفئران والخلايا الحيوانية الأخرى للحفاظ على تعدد القدرات للخلايا الجذعية المقسمة بنشاط. واكتشفت المشكلة عندما عثر على الحامض اللعابي غير البشري في وسائط النمو للتوصل إلى الاستخدامات الممكنة للخلايا الجذعية الجنينية في البشر، وفقا للعلماء في جامعة كاليفورنيا في سان دييغو.[13]
ومع ذلك، فإن الدراسة التي نشرت في طبعة الإنترنت من مجلة لانسيت الطبية في 8 مارس 2005 احتوت معلومات مفصلة حول خط الخلايا الجذعية الجديدة التي كانت مستمدة من الأجنة البشرية في ظل ظروف الخلايا والخلايا الخالية من المصل تماما. بعد أكثر من 6 أشهر من التكاثر غير المتمايز، أظهرت هذه الخلايا القدرة على تشكيل مشتقات جميع الطبقات الجرثومية الجنينية الثلاثة على حد سواء في التجارب المختبرية وفي الورم المسخي. وأيضا الحفاظ على هذه الخصائص بنجاح (أكثر من 30 قناة) مع خطوط الخلايا الجذعية المنشأة.[14]
الحد من رفض الجهات المانحة والمضيفة
وهناك أيضا البحوث الجارية للحد من احتمالات رفض الخلايا المتمايزة المستمدة من الخلايا الجذعية الجنينية بمجرد ان الباحثين قادرين على خلق العلاج الموافق عليه من أبحاث الخلايا الجذعية الجنينية. احدى الإمكانيات لمنع الرفض عن طريق إنشاء خلايا جذعية جنينية متطابقة وراثيا للمريض عن طريق الاستنساخ العلاجي.
حل بديل لرفض المريض للعلاجات المستمدة من الخلايا الجذعية الجنينية غير المستنسخة هو استمداد العديد من خطوط الخلايا الجذعية الجنينية التي تتميز جيدا من خلفيات وراثية مختلفة، واستخدام خط الخلايا الأكثر تجانسا مع المريض، ويمكن للعلاج بعد ذلك أن يكون متكيفا مع المريض، مقللا بذلك من خطر الرفض.
السلامة: الحد من مخاطر الورم المسخي وأنواع أخرى من السرطان باعتبارها تأثيرات جانبية
- مصدر القلق الرئيسي من الزراعة الممكنة للخلايا الجذعية الجنينية في المرضى كعلاجات هو قدرتها على تشكيل أورام بما في ذلك الورم المسخي.[15] قضايا السلامة دفعت إدارة الاغذية والعقاقير لوضع إجراء على أول تجربة سريرية على الخلايا الجذعية الجنينية (أنظر أدناه)، ومع ذلك لم تلاحظ أي أورام.
- الاستراتيجية الرئيسية لتعزيز سلامة الخلايا الجذعية الجنينية للاستخدام السريري المحتمل هي تمايز الخلايا الجذعية الجنينية إلى أنواع معينة من الخلايا (على سبيل المثال الخلايا العصبية والعضلات وخلايا الكبد) التي خفضت أو قضت على إمكانية التسبب بأورام. وعقب التمايز، تخضع الخلايا للتصنيف بواسطة قياس التدفق الخلوي من أجل تنقية أخرى. في حين أن المتوقع من الخلايا الجذعية الجنينية أن تكون أكثر أمنا من الخلايا الجذعية المستحثة متعددة القدرات لأنها ليست معدلة وراثيا مع مورثات من قبيل c-Myc التي لها علاقة بالسرطان. على الرغم من أن الخلايا الجذعية الجنينية عبَرت عن مستويات عالية جدا من الخلايا الجذعية متعددة القدرات المستحثة للمورثات وهذه المورثات بما في ذلك Myc ضرورية للتجديد الذاتي في الخلايا الجذعية الجنينية وتعدد القدرات،[16] أما الاستراتيجيات الممكنة لتحسين السلامة من خلال القضاء على تعبير Myc مستبعدة للحفاظ على خلايا "stemness".
أول تجربة سريرية
في 23 يناير 2009، فإن المرحلة الأولى من التجارب السريرية لزراعة اوليغوديندروستس (نوع من الخلايا في الدماغ والحبل الشوكي) المستمدة من الخلايا الجذعية الجنينية البشرية في النخاع الشوكي المصاب في الأفراد المصابين وقد تمت الموافقة عليها من هيئة الغذاء والدواء الأمريكية (FDA)، وتأشيرها بانها أول تجربة في الخلايا الجذعية الجنينية البشرية في العالم.[17] وأجريت الدراسة المؤدية إلى هذا التقدم العلمي بواسطة هانز كيرستيد وزملاؤه في جامعة كاليفورنيا في إرفاين وبدعم من شركة غيرون من مينلو بارك، كاليفورنيا. وقد أظهر تحسن في تجربة سابقة في استرداد حركة النخاع الشوكي المصاب في الفئران بعد تأخر الزراعة لمدة 7 أيام من الخلايا الجذعية الجنينية البشرية التي دفعت إلى سلالة اوليغوديندروستس.[18] في المرحلة الأولى من الدراسة السريرية المقترحة، فإن حوالي ثمانية إلى عشرة من المرضى المصابين بشلل نصفي والذين إصاباتهم ليست أطول من أسبوعين قبل بدء التجربة سيتم اختيارهم، بحيث أن الخلايا المحقونة قادرة على التشكل قبل النسيج الندبي. ومع ذلك، يؤكد الباحثون أنه من غير المتوقع أن يعمل الحقن على علاج المرضى بشكل كامل واستعادة كل الحركة. استنادا إلى نتائج التجارب على القوارض، يقول الباحثون انه من المحتمل استعادة تغطية النخاعين، وزيادة القدرة على الحركة. هذه التجربة هي أساسا اختبار لسلامة هذه الإجراءات وإذا كان كل شيء على ما يرام، فإنها يمكن أن تؤدي إلى دراسات مستقبلية تتضمن اشخاصا ذوي إعاقات أكثر شدة.[19] علق اجراء هذه التجربة في أغسطس 2009 بسبب المخاوف التي بذلتها الهيئة الأميركية للأغذية والدواء فيما يتعلق بعدد صغير من الكيسات المجهرية الموجودة في عدة نماذج من الجرذان المعالجة ولكن تم تنشيط الإجراء بتاريخ 30 يوليو 2010.[20][21][22]
في أكتوبر 2010، فإن الباحثين المسجلين والذين يعملون على إدارة العلاج بالخلايا الجذعية الجنينية لأول مريض في مركز الراعي في اتلانتا.[23] واضعي العلاج بالخلايا الجذعية، من شركة غيرون، يقدرون أن الأمر سيستغرق عدة أشهر للخلايا الجذعية للنسخ المتماثل ولعلاج GRNOPC1 ليتم تقييم النجاح أو الفشل.
الطرق المحتملة لاستمداد خط الخلايا الجديد
في 23 أغسطس 2006، نشرت مجلة نيتشر العلمية في طبعة الإنترنت رسالة بواسطة الدكتور روبرت لانزا (المدير الطبي لادفانسد سيل تكنولوجي في ورسستر، ماساتشوسيتس) تفيد بأن فريقه قد وجد طريقة لاستخراج الخلايا الجذعية الجنينية دون تدمير الأجنة الحقيقية.[24] ومن المحتمل ان يمكن هذا الإنجاز التقني العلماء للعمل على خطوط جديدة للخلايا الجذعية الجنينية المستمدة باستخدام التمويل العام في الولايات المتحدة، حيث أن التمويل الفيدرالي كان مقتصرا في ذلك الوقت على البحث باستخدام الخلايا الجذعية الجنينية المستمدة قبل أغسطس 2001. في آذار / مارس 2009، تم رفع القيد.[25]
مؤخرا، تبينت إمكانية توليد الخلايا الجذعية متعددة الامكانات والمماثلة جدا للخلايا الجذعية الجنينية عن طريق تسليم ثلاثة مورثات (Oct4، Sox2، Klf4) إلى الخلايا المتمايزة.[26] تسليم هذه المورثات "يعيد برمجة" الخلايا المتمايزة إلى الخلايا الجذعية متعددة الإمكانات، والسماح بتوليد الخلايا الجذعية متعددة الإمكانات من دون الجنين.بسبب المخاوف الأخلاقية فيما يتعلق بالخلايا الجذعية الجنينية والتي عادة ما تكون حول استمدادها من الأجنة المنتهية، يعتقد أن إعادة برمجتها إلى "الخلايا الجذعية المستحثة متعددة المكانات" (خلايا iPS) قد يكون أقل إثارة للجدل. ويمكن إعادة برمجة خلايا الإنسان والحيوان على حد سواء بواسطة هذه المنهجية، وبالتالي توليد الخلايا الجذعية متعددة الإمكانات البشرية والحيوانية على حد سواء من دون جنين.[27]
هذا قد يجعل من الممكن توليد سلالة الخلايا الجذعية الجنينية من المرضى لاستخدامها في علاج استبدال الخلايا. وبالإضافة إلى ذلك، سيسمح هذا بتوليد سلالة الخلايا الجذعية الجنينية من المرضى الذين يعانون من مجموعة متنوعة من الأمراض الوراثية، وسوف تقدم نماذج لا تقدر بثمن لدراسة تلك الأمراض.
ومع ذلك، كأول إشارة إلى أن تقنية الخلايا الجذعية المستحثة متعددة القدرات (iPS) يمكن وبتعاقب سريع ان تؤدي إلى علاجات جديدة، وكانت تستخدم بواسطة فريق بحثي برئاسة رودولف جينسش من معهد وايتهيد للأبحاث الطبية الحيوية في كامبريدج، ماساشوستس، لشفاء الفئران من فقر الدم المنجلي، كما ذكرت طبعة الإنترنت من مجلة العلوم في 6 ديسمبر 2007.[28]
في 16 يناير 2008، أعلنت شركة مقرها كاليفورنيا، ستيماغان، أنها أنشأت أول أجنة بشرية مستنسخة ناضجة من خلايا الجلد المنفردة المأخوذة من البالغين. يمكن حصاد هذه الأجنة من اجل مطابقة الخلايا الجذعية الجنينية للمريض.[29]
استخدام الخلايا الجذعية الجنينية البشرية كنماذج للاضطرابات الوراثية البشرية
بدأت دراسات جديدة عديدة لمعالجة هذه المسألة. وقد تم ذلك إما عن طريق التلاعب وراثيا في الخلايا، أو أكثر مؤخرا عن طريق استمداد سلالة الخلايا المريضة التي حددها التشخيص الوراثي قبل الولادة (PGD). وهذا النهج سيكون جيد جدا ولا تقدر بثمن في دراسة اضطرابات من قبيل متلازمة هشاشة X والتليف الكيسي والعلل الوراثية الأخرى التي لا يوجد لها نظام نموذجي يمكن الاعتماد عليه.
يوري فيرلنسكي (1 سبتمبر 1943—16 يوليو 2009)، وهو باحث طبي روسي أمريكي متخصص في الأجنة وعلم الوراثة الخلوية (علم الأحياء الخلوي الوراثي)، قام بتطوير أساليب اختبارات التشخيص قبل الولادة لتحديد الاضطرابات الوراثية والكروموسومية في وقت سابق قبل شهر ونصف من بزل السائل الامنيوسي القياسي. التقنيات تستخدم الآن من قبل العديد من النساء الحوامل والآباء المستقبليين، وخاصة أولئك الأزواج الذين لديهم تاريخ من التشوهات الوراثية أو التي فيها المرأة فوق سن ال 35، حيث يكون خطر الاضطرابات المرتبطة وراثيا أعلى. وبالإضافة إلى ذلك، فانه عن طريق السماح للآباء باختيار الأجنة من دون اضطرابات وراثية، لدى هذه التقنيات إمكانية إنقاذ حياة الأشقاء الذين سبق لديهم اضطرابات مماثلة وأمراض باستخدام الخلايا من سلالة خالية من المرض.[30]
انظر أيضاً
المراجع
- Thomson; Itskovitz-Eldor, J; Shapiro, SS; Waknitz, MA; Swiergiel, JJ; Marshall, VS; Jones, JM; et al. (1998). "Blastocysts Embryonic Stem Cell Lines Derived from Human". Science. 282 (1145): 1145–1147. doi:10.1126/science.282.5391.1145. PMID 9804556. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة) - Ying; Nichols, J; Chambers, I; Smith, A; et al. (2003). "BMP Induction of Id Proteins Suppresses Differentiation and Sustains Embryonic Stem Cell Self-Renewal in Collaboration with STAT3". Cell. 115 (3): 281–292. doi:10.1016/S0092-8674(03)00847-X. PMID 14636556. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة) - Andrews P, Matin M, Bahrami A, Damjanov I, Gokhale P, Draper J (2005). "Embryonic stem (ES) cells and embryonal carcinoma (EC) cells: opposite sides of the same coin". Biochem Soc Trans. 33 (Pt 6): 1526–30. doi:10.1042/BST20051526. PMID 16246161. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Martin GR (1980). "Teratocarcinomas and mammalian embryogenesis". Science. 209 (4458): 768–76. doi:10.1126/science.6250214. PMID 6250214. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Evans M, Kaufman M (1981). "Establishment in culture of pluripotent cells from mouse embryos". Nature. 292 (5819): 154–6. doi:10.1038/292154a0. PMID 7242681. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Martin G (1981). "Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells". Proc Natl Acad Sci USA. 78 (12): 7634–8. doi:10.1073/pnas.78.12.7634. PMC 349323. PMID 6950406. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Thomson J, Itskovitz-Eldor J, Shapiro S, Waknitz M, Swiergiel J, Marshall V, Jones J (1998). "Embryonic stem cell lines derived from human blastocysts". Science. 282 (5391): 1145–7. doi:10.1126/science.282.5391.1145. PMID 9804556. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Smith AG, Heath JK, Donaldson DD, Wong GG, Moreau J, Stahl M, Rogers D (1988). "Inhibition of pluripotential embryonic stem cell differentiation by purified polypeptides". Nature. 336 (6200): 688–690. doi:10.1038/336688a0. PMID 3143917. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Williams RL, Hilton DJ, Pease S, Willson TA, Stewart CL, Gearing DP, Wagner EF, Metcalf D, Nicola NA, Gough NM (1988). "Myeloid leukaemia inhibitory factor maintains the developmental potential of embryonic stem cells". Nature. 336 (6200): 684–687. doi:10.1038/336684a0. PMID 3143916. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Ledermann B, Bürki K (1991). "Establishment of a germ-line competent C57BL/6 embryonic stem cell line". Exp Cell Res. 197 (2): 254–258. doi:10.1016/0014-4827(91)90430-3. PMID 1959560. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Takahashi K, Tanabe K, Ohnuki M, Narita M, Ichisaka T, Tomoda K, Yamanaka S. (2007). "Induction of pluripotent stem cells from adult human fibroblasts by defined factors". Cell. 131 (5): 861–872. doi:10.1016/j.cell.2007.11.019. PMID 18035408. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Ebert, Jessica (24 January 2005). "Human stem cells trigger immune attack". News from "Nature". London: Nature Publishing Group. doi:10.1038/news050124-1. مؤرشف من الأصل في 07 يوليو 2011. اطلع عليه بتاريخ 27 فبراير 2009. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Martin MJ, Muotri A, Gage F, Varki A (2005). "Human embryonic stem cells express an immunogenic nonhuman sialic acid". Nat. Med. 11 (2): 228–32. doi:10.1038/nm1181. PMID 15685172. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Klimanskaya I, Chung Y, Meisner L, Johnson J, West MD, Lanza R (2005). "Human embryonic stem cells derived without feeder cells". Lancet. 365 (9471): 1636–41. doi:10.1016/S0140-6736(05)66473-2. PMID 15885296. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Paul S. Knoepfler. Deconstructing stem cell tumorigenicity: a roadmap to safe regenerative medicine Stem Cells doi:10.1002/stem.37
- Varlakhanova, et al. myc maintains embryonic stem cell pluripotency and self-renewal Differentiation doi:10.1016/j.diff.2010.05.001
- "FDA approves human embryonic stem cell study - CNN.com". January 23, 2009. مؤرشف من الأصل في 4 ديسمبر 2017. اطلع عليه بتاريخ May 1, 2010. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Keirstead HS, Nistor G, Bernal G; et al. (2005). "Human embryonic stem cell-derived oligodendrocyte progenitor cell transplants remyelinate and restore locomotion after spinal cord injury". J. Neurosci. 25 (19): 4694–705. doi:10.1523/JNEUROSCI.0311-05.2005. PMID 15888645. الوسيط
|CitationClass=تم تجاهله (مساعدة); Explicit use of et al. in:|مؤلف=(مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Steven Reinberg FDA OKs 1st Embryonic Stem Cell Trial نسخة محفوظة 25 أكتوبر 2017 على موقع واي باك مشين.
- Geron comments on FDA hold on spinal cord injury trial http://www.geron.com/media/pressview.aspx?id=1188 نسخة محفوظة 12 فبراير 2011 على موقع واي باك مشين.
- Geron comments on FDA hold on spinal cord injury trial
- Geron to Proceed with First Human Clinical Trial of Embryonic Stem Cell-Based Therapy http://www.geron.com/media/pressview.aspx?id=1188 نسخة محفوظة 12 فبراير 2011 على موقع واي باك مشين.
- Vergano, Dan (11 October 2010). "Embryonic stem cells used on patient for first time". يو إس إيه توداي. مؤرشف من الأصل في 28 يونيو 2011. اطلع عليه بتاريخ 12 أكتوبر 2010. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Klimanskaya I, Chung Y, Becker S, Lu SJ, Lanza R. (2006). "Human embryonic stem cell lines derived from single blastomeres". Nature. 444 (7118): 481–5. doi:10.1038/nature05142. PMID 16929302. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - US scientists relieved as Obama lifts ban on stem cell research, الغارديان, 10 March 2009 نسخة محفوظة 26 يوليو 2013 على موقع واي باك مشين.
- "Human stem cells may be produced without embryos 'within months'". Zangani. 2007-07-17. مؤرشف من الأصل في 3 أبريل 2012. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Embryonic stem cells made without embryos". رويترز. 2007-11-21. مؤرشف من الأصل في 1 أبريل 2009. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Rick Weiss (2007-12-07). "Scientists Cure Mice Of Sickle Cell Using Stem Cell Technique: New Approach Is From Skin, Not Embryos". واشنطن بوست. صفحات A02. مؤرشف من الأصل في 25 ديسمبر 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Helen Briggs (2008-01-17). "US team makes embryo clone of men". بي بي سي. صفحات A01. مؤرشف من الأصل في 22 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Dr. Yury Verlinsky, 1943-2009: Expert in reproductive technology" Chicago Tribune, July 20, 2009
وصلات خارجية
- فهم الخلايا الجذعية : رؤية للعلوم والمسائل من الأكاديميات الوطنية
- المعاهد الوطنية للصحة
- مركز أخلاقيات علم الأحياء وكرامة الإنسان
- المعلومات والبدائل لأبحاث الخلايا الجذعية الجنينية
- بوابة علم الأحياء الخلوي والجزيئي
- بوابة علم الأحياء
- بوابة طب