تبلور
التبلور (أو البَلْوَرَة) عبارة عن عملية تشكيل (طبيعية كانت أم اصطناعية) للبلورات الصلبة من المحلول.[1][2][3]


تعد عملية التبلور أيضاً من تقنيات الفصل في الأوساط الصلبة-السائلة، حيث تحدث عملية انتقال لجزيئات للمادة من الحالة السائلة إلى الحالة الصلبة.
تعتمد عملية التبلور على ضبط درجة حرارة الوسط وضبط الضغط وإعطاء النظام الوقت الكافي الذي يسمح بتكون البلورات الكبيرة.
التبلور في الطبيعة


ونشاهد في الطبيعة ظواهر كثيرة تتضمن عملية التبلور، وفي كثير من الأحيان تكون عصورا جيولوجية طويلة قد مضت حتى تتكون، مثل:
- المعادن الخام والصخور مثل الجرانيت متبلورة بطبيعتها، وكذلك الأحجار الكريمة،
- متدليات الكهوف وصواعد الكهوف وهي أعمدة مخروطية متبلورة تحتوي على الماء. وعادة تتواجدا سوياً، حيث تتكون المتدليات أو الهوابط من تتابع تساقط قطرات الماء المحتوية على تركيبات معدنية ذائبة فيتبخر الماء منها وتعلق التركيبات المعدنية وتتبلور في هيئة المتدليات من أسقف الكهوف. عند سقوط قطرات الماء من المتدليات تشكل أيضا علي أرضية الكهف بعد تبخرها مخروطات هرمية من تركيبات المعادن المتبلورة، ومع مرور الزمن تستطيل المتدليات من أعلى إلى أسفل بينما يتزايد ارتفاع الصواعد المخروطية تحتها من أسفل إلى أعلى. بذلك يتكون الشكل المألوف للهوابط والصواعد المتبلورة في الكهوف. تحتاج نشأة تلك الأشكال البلورية إلى أزمنة طويلة من تتابع سقوط قطرات المياه المعدنية واحدة تلو الأخرى وتبلور المعادن التي يحتويها الماء تقاس بعشرات الآلاف أو مئات الآلاف من السنين.
ومن الأشكال المعهودة التي تتبلور خلال وقت قصير :
- أشكال الثليج السداسية الشكل والتي تتكون على الأسطح المستوية الباردة في وجود بخار الماء.
- تبلور عسل النحل، وتميل معظم أنواع عسل النحل على التبلور.
تطبيقات
تستخدم عملية التبلور في نوعين من التطبيقات لإنتاج " التبلور الصناعي" وهما: أنتاج البلورات ولتنقية المعادن والمركبات.
إنتاج البلورات
من وجهة علم المواد والصناعة تدرس وتبتكر طرق لتنمية البلورات :
- لإنتاج بلورات كبيرة الحجم أو إنتاج بلورات على مستوى صناعي كبير ذات نقاوة عالية،
- منها أنتاج بلورات أيونية،
- ومنها أنتاج بلورات روابط تساهمية
- إنتاج بلورات صغيرة :
- إنتاج المساحيق، ومؤخرا مساحيق تقنية النانو،
- إنتاج عل المستوى الصناعي الكبير في الصناعات الكيماوية مثل إنتاج الملح،
- إنتاج العينات : إنتاج عينات دقيقة لدراسة خصائصها في علم المواد، وطرق إعادة التبلور، وتبلور بلورات غريبة تدرس عن طريقها بناء الجزيئات ، وقوي ترابط الذرات في البناء البلوري.
تستخدم طرق تعيين البنية البلورية بواسطة أشعة إكس وكذلك مطيافية الرنين المغناطيسي النووي NMR spectroscopy في الكيمياء المعدنية والكيمياء العضوية لمعرفة الهياكل البلورية لأعداد كبيرة من المركبات المعدنية والمركبات العضوية ، ومن ضمنها دراسة بنية الجزيئات العضوية الكبيرة.
- ترسيب الرقاق الرقيقة.
أمثلة لمنتجات على المستوى الصناعي الكبير:
- إنتاج ملح الطعام
- إنتاج الويفر من السيليكون النقي التي تستخدم في صناعات ميكروبروسيسور
- إنتاج السكروز من قصب السكر والبنجر، حيث يتبلور السكر وينفصل من المحاليل السكرية.
- أنتاج الخلايا الشمسية المستخدمة لإنتاج التيار الكهربائي من الطاقة الشمسية بواسطة التأثير ضوء جهدي.
علاقة التبلور والترموديناميك

تعتمد عملية التبلور على الترموديناميكا وحركة الجزيئات مما يجعل من الصعب التحكم في تلك العملية. وتدخل فيها مسألة نقاوة المادة المتبلورة، وطريقة خلط المكونات، وتصميم بوتقة التبلور، وخطة التبريد، كل تلك العوامل تؤثر على حجم البلورة المتكونة، وعدد البلورات، وشكلها.
ويمكننا تصور عملية التبلور بتخهيل جزيئ في داخل "بلورة مثالية" عندما ترفع درجة حرارتها بواسطة مصدر حراري خارجي. فعند وصول البلورة إلى درجة حرارة معينة (مميزة لمادة البلورة) ، ينق الرباط بين الجزيئ وما حولة فجأة، ولحظيا يحدث ذلك لجميع الجزيئات في البلورة فتنفصل الجزئيات عن بعضها وتفقد هيكلها البلوري مكونة سائلا (يصبح توزيع مجموع الجزيئات عشوائيا لا شكل داخليا له). وتصف الديناميكا الحرارية تلك العملية بأن تحول المادة الصلبة المتبلورة إلى السيولة بسبب زيادة الإنتروبية S حيث تزيد عشوائية توزيع الجزيئات في النظام، وتغلبه على الإنثالبية H ، أي قوي الروابط بين الجزيئات.
G تسمى طاقة جيبس الحرة وهي في السائل أقل من مقدارها في المادة الصلبة أو البلورة.
تلك العملية تحدث دائما عند ارتفاع درجة الحرارة. كذلك بالنسبة إلى عملية التبريد، فعد التبريد ووصول درجة الحرارة المميزة للمادة، فجأة تتشابك الجزيئات وتتخذ شكلها البلوري. بذلك تنخفض الأنتروبية بسبب تبوء الجزيئات أماكن ثابتة منتظمة في البلورة. وهي عندما تترابط فيما بينها فهي تطلق حرارة الارتباط إلى الجو المحيط بها الذي يزيد من عشوائية الذرات والجزيئات في الكون - أي تزيد انتروبية الكون.
ولكن السوائل التي تتصرف بهذه الطريقة عند تبريدها قليلة، فعلى الرغم من القانون الثاني للديناميكا الحرارية يحدث التبلور عادة عند درجة حرارة أقل قليلا عن درجة الحرارة المميزة للمادة - عند حالة للسائل تسمي "تبريد فائق". وهذا يعني من وجهة الترموديناميكا أنه من الأسهل هدم البلورة وتفرقة جزيئاتها عن جمعهم وبناء النظام البلوري.
وإنه من الأسهل إذابة بلورة في مذيب عن تكوين بلورة منتظمة من هثل ذلك المحلول. إن تكوين نواة ابتدائية للتبلور وتنمية البلورة يعتمد على التحكم في حركة الجزيئات أكثر من اعتمادة على التحكم في الحركة الحرارية (الترموديناميك).
طرق
يمكن تقسيم تكوين البلورات إلى نوعين، حيث يتكون النوع الأول من البلورات من كاتيون وأنيون، يُعرف أيضًا بالملح، مثل أسيتات الصوديوم. [3]النوع الثاني من البلورات يتكون من أنواع غير مشحونة، مثل المنثول.
يمكن تحقيق تكوين البلورات بطرق مختلفة، مثل: التبريد، التبخر، إضافة مذيب ثانٍ لتقليل قابلية الذوبان في المذاب (تقنية تعرف باسم مضاد الذوبان أو الغرق) ، طبقات المذيبات، التسامي، تغيير الكاتيون أو الأنيون، بالإضافة إلى طرق أخرى.
لا يضمن تكوين محلول مفرط التشبع تكوين البلورات، وغالبًا ما يلزم بلورة بذرة أو خدش الزجاج لتشكيل مواقع التنوي.
تتمثل التقنية المختبرية النموذجية لتشكيل البلورات في إذابة المادة الصلبة في محلول يكون فيه ذائب جزئيًا، وعادة في درجات حرارة عالية للحصول على تشبع فائق. ثم يتم ترشيح الخليط الساخن لإزالة أي شوائب غير قابلة للذوبان. يسمح للمرشح أن يبرد ببطء. يتم بعد ذلك ترشيح البلورات المتكونة وغسلها بمذيب لا تذوب فيه، ولكنها قابلة للامتزاج مع السائل الأم. ثم يتم تكرار العملية لزيادة النقاء في تقنية تعرف باسم إعادة التبلور.
للجزيئات البيولوجية التي قنوات المذيبات تستمر ليكون حاضرا في الإبقاء على ثلاثة هيكل الأبعاد سليمة، microbatch بلورة إطار النفط وبخار نشر كانت أساليب الطرق الشائعة.[4]
المعدات النموذجية
معدات للعمليات الصناعية الرئيسية للبلورة .
- بلورات الخزان. يعتبر تبلور الخزان طريقة قديمة لا تزال تستخدم في بعض الحالات المتخصصة. يسمح للمحاليل المشبعة، في تبلور الخزان، بالتبريد في خزانات مفتوحة. بعد فترة من الوقت يتم تصريف المحلول الأم وإزالة البلورات. يصعب التحكم في التنوي وحجم البلورات. عادةً ما تكون تكاليف العمالة مرتفعة جدًا.
ديناميات
تتشكل البلورة باتباع نمط أو بنية محددة جيدًا، تمليها قوى تعمل على المستوى الجزيئي. نتيجة لذلك، أثناء عملية تكوينها، تكون البلورة في بيئة يصل فيهاتركيز المادة المذابة إلى قيمة حرجة معينة، قبل تغيير الحالة. الصلبة تشكيل، من المستحيل دون الذوبان العتبة في لحظة معينة في درجة الحرارة وضغط الظروف، قد ثم تجري بتركيز أعلى من مستوى الذوبان النظري. يسمى الفرق بين القيمة الفعلية لتركيز المذاب عند حد التبلور وعتبة الذوبان النظرية (الثابتة) التشبع الفائق وهو عامل أساسي في التبلور.
تنوي
التنوي هو بدء تغيير الطور في منطقة صغيرة، مثل تكوين بلورة صلبة من محلول سائل. إنه نتيجة للتقلبات المحلية السريعة على نطاق جزيئي في مرحلة متجانسة تكون في حالة توازن مستقر. التنوي الكلي هو مجموع تأثير فئتين من التنوي - الابتدائية والثانوية.
التنوي الأولي
التنوي الأولي هو التكوين الأولي للبلورة حيث لا توجد بلورات أخرى أو حيث، إذا كانت هناك بلورات موجودة في النظام، فلن يكون لها أي تأثير على العملية. يمكن أن يحدث هذا في حالتين. الأول هو التنوي المتجانس، وهو تنوي لا يتأثر بأي شكل من الأشكال بالمواد الصلبة. تشمل هذه المواد الصلبة جدران وعاء التبلور وجزيئات أي مادة غريبة. الفئة الثانية، إذن، هي النواة غير المتجانسة. يحدث هذا عندما تتسبب الجسيمات الصلبة للمواد الغريبة في زيادة معدل التنوي الذي لا يمكن رؤيته بدون وجود هذه الجسيمات الغريبة. نادرًا ما يحدث التنوي المتجانس في الممارسة العملية بسبب الطاقة العالية اللازمة لبدء التنوي بدون سطح صلب لتحفيز التنوي.
تم نمذجة النواة الأولية (سواء كانت متجانسة أو غير متجانسة) على النحو التالي:
حيث:
- B هو عدد النوى المتكونة لكل وحدة حجم لكل وحدة زمنية،
- N هو عدد النوى لكل وحدة حجم،
- k n هو معدل ثابت،
- ج هو تركيز المذاب الفوري،
- ج * هو تركيز المذاب عند التشبع،
- (ج - ج *) يُعرف أيضًا باسم التشبع الفائق،
- n هو أس تجريبي يمكن أن يكون كبيرًا مثل 10 ، ولكن بشكل عام يتراوح بين 3 و4.
التنوي الثانوي
التنوي الثانوي هو تكوين نوى يعزى إلى تأثير البلورات المجهرية الموجودة في الصهارة. وببساطة، فإن التنوي الثانوي يحدث عندما يبدأ نمو البلورات بالتلامس مع بلورات أخرى موجودة أو "بذور".[5] يُعزى النوع الأول من التبلور الثانوي المعروف إلى قص المائع، ويعزى الآخر إلى الاصطدامات بين البلورات الموجودة بالفعل إما مع سطح صلب للمبلور أو مع بلورات أخرى نفسها. يحدث نواة القص المائع عندما ينتقل السائل عبر بلورة بسرعة عالية، مما يزيل النوى التي يمكن دمجها في البلورة، مما يتسبب في أن تصبح النوى المنجرفة بلورات جديدة. تم العثور على تنوي الاتصال هو الطريقة الأكثر فعالية وشائعة للتنوي. تشمل الفوائد ما يلي:
- ترتيب حركي منخفض ومعدل يتناسب مع التشبع الفائق، مما يتيح التحكم السهل دون تشغيل غير مستقر.
- يحدث عند فرط التشبع المنخفض، حيث يكون معدل النمو هو الأمثل للحصول على جودة جيدة.
- الطاقة الضرورية المنخفضة التي تصطدم بها البلورات تمنع تكسير البلورات الموجودة إلى بلورات جديدة.
- تم بالفعل عزل الأساسيات الكمية ويتم دمجها في الممارسة.
النموذج التالي، على الرغم من تبسيطه إلى حد ما، غالبًا ما يستخدم لنمذجة التنوي الثانوي:
أين
- ك 1 هو معدل ثابت،
- M T هي كثافة التعليق،
- j هو أس تجريبي يمكن أن يصل إلى 1.5 ، ولكنه بشكل عام 1 ،
- ب هو أس تجريبي يمكن أن يصل إلى 5 ، لكنه بشكل عام 2.
نمو
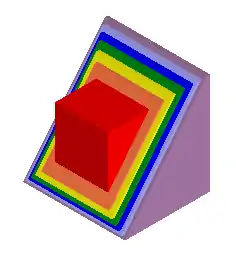
بمجرد تشكيل أول بلورة صغيرة، النواة، تعمل كنقطة التقاء (إذا كانت غير مستقرة بسبب التشبع الفائق) لجزيئات المذاب التي تلامس - أو بجوار - البلورة بحيث تزيد من أبعادها في الطبقات المتتالية. يشبه نمط النمو حلقات البصل، كما هو موضح في الصورة، حيث يشير كل لون إلى نفس كتلة المذاب ؛ تخلق هذه الكتلة طبقات رقيقة بشكل متزايد بسبب زيادة مساحة سطح البلورة المتنامية.تسمى الكتلة المذابة المفرطة التشبع التي قد تلتقطها النواة الأصلية في وحدة زمنية بمعدل النمو المعبر عنه بالكيلو جرام / (م 2 * ساعة) ، وهي ثابتة خاصة بالعملية. يتأثر معدل النمو بعدة عوامل فيزيائية، مثل التوتر السطحيمن الحل، الضغط، درجة الحرارة، وضوح الشمس النسبية سرعة في الحل، رقم رينولدز، وهكذا دواليك.
القيم الرئيسية التي يجب التحكم فيها هي:
- قيمة التشبع الفائق، كمؤشر لكمية المذاب المتاحة لنمو البلورة ؛
- إجمالي السطح البلوري في كتلة سائل الوحدة، كمؤشر لقدرة المذاب على التثبيت على البلورة ؛
- وقت الاستبقاء، كمؤشر لاحتمال تلامس جزيء من المادة المذابة مع بلورة موجودة ؛
- نمط التدفق، مرة أخرى كمؤشر لاحتمال تلامس جزيء من المذاب مع بلورة موجودة (أعلى في التدفق الصفحي، وأقل في التدفق المضطرب، ولكن العكس ينطبق على احتمال التلامس).
القيمة الأولى هي نتيجة للخصائص الفيزيائية للمحلول، بينما تحدد القيم الأخرى الفرق بين بلورة جيدة التصميم وسيئة التصميم.
حجم التوزيع
شكل وحجم المنتج البلوري مهم للغاية في التبلور. إذا كانت هناك حاجة إلى مزيد من المعالجة للبلورات، فإن البلورات الكبيرة ذات الحجم الموحد مهمة للغسيل والتصفية والنقل والتخزين، لأن البلورات الكبيرة أسهل في التصفية من المحلول من البلورات الصغيرة. أيضًا، تحتوي البلورات الأكبر حجمًا على مساحة أصغر من نسبة الحجم، مما يؤدي إلى درجة نقاء أعلى. هذا النقاء العالي يرجع إلى احتباس أقل للخمور الأمالذي يحتوي على شوائب، وخسارة أقل في المحصول عند غسل البلورات لإزالة المحلول الأم. في حالات خاصة، على سبيل المثال أثناء تصنيع الأدوية في صناعة الأدوية، غالبًا ما تكون الأحجام البلورية الصغيرة مرغوبة لتحسين معدل انحلال الدواء والتوافر البيولوجي. يمكن تقدير توزيع الحجم البلوري النظري كدالة لظروف التشغيل مع عملية رياضية معقدة إلى حد ما تسمى نظرية توازن السكان (باستخدام معادلات توازن السكان).
اقرأ أيضا
مراجع
- "Crystallization". www.reciprocalnet.org. مؤرشف من الأصل في 26 ديسمبر 2017. اطلع عليه بتاريخ 03 يناير 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Submerge Circulating Crystallizers - Thermal Kinetics Engineering, PLLC". Thermal Kinetics Engineering, PLLC (باللغة الإنجليزية). مؤرشف من الأصل في 5 أبريل 2020. اطلع عليه بتاريخ 03 يناير 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Lin, Yibin (2008). "An Extensive Study of Protein Phase Diagram Modification:Increasing Macromolecular Crystallizability by Temperature Screening". Crystal Growth & Design. 8 (12): 4277. doi:10.1021/cg800698p. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Benvenuti, Manuela; Mangani, Stefano (2007-07). "Crystallization of soluble proteins in vapor diffusion for x-ray crystallography". Nature Protocols (باللغة الإنجليزية). 2 (7): 1633–1651. doi:10.1038/nprot.2007.198. ISSN 1750-2799. مؤرشف من الأصل في 7 أغسطس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - "Crystallization". www.reciprocalnet.org. مؤرشف من الأصل في 11 سبتمبر 2019. اطلع عليه بتاريخ 30 ديسمبر 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء
