إنتروبيا وسهم الزمن
القصور الحراري أو الإنتروبيا (بالإنجليزية: Entropy) هي الكمية الوحيدة في الفيزياء والكيمياء التي تحتاج إلى تعريف اتجاه الزمن أو ما يسمى سهم الزمن . فبحسب القانون الثاني للديناميكا الحرارية تزداد إنتروبية نظام معزول مع مرور الزمن تلقائيا ، أي يمكن قياس مرور الزمن بمعرفة تغير الإنتروبية . ولكن بالنسبة إلى الأنظمة الترموديناميكية (الحرارية) الغير معزولة يمكن لأنتروبية النظام المفتوح أن تنخفض : وتوجد أنظمة عديدة تتغير فيها الانتروبيا وتقل مع الزمن ، مثل الكائنات الحية ، و عمليات التبلور. في تلك الأنظمة تنخفض قيمة الإنتروبيا على حساب زيادته في الوسط المحيط . ومثال على ذلك تبلور البلورات وعمل الثلاجة و ووجود الحياة ،إذ يوجد تبادل طاقة بين النظام والوسط المحيط في النظام المفتوح.
على عكس ذلك نجد أن قارورة بها غاز لا تتغير مع الزمن ويمكن القول بأن أنتروبيته ثابتة . أما إذا كان لدينا قارورتين واحدة بها غاز والأخرى فارغة وبينهما صمام ، فعند فتح الصمام يبدأ الغاز يتوزع في القارورة الفارغة ويصل إلى حالة استقرار عندما تكون كثافة الغاز في القارورة اليمنى مساوية لكثافته في القارورة اليسرى . عندئذ نستطيع القول أن أنتروبية الغاز زادت مع الزمن حتى الوصول إلى حالة التوازن ، ولكن ليس من المحتمل إطلاقا أن يعود الغاز ويتجمع في إحدى القارورتين مهما طال الزمن .
مقدمة
يسمح القانون الثاني للديناميكا الحرارية بثبات إنتروبية نظام بصرف النظر عن الزمن . فإذا كانت الإنتروبية ثابتة بصرف النظر عن اتجاه الزمن فلا يكون للزمن اتجاها معينا . ولكن إنتروبية نظام تكون ثابتة فقط عندما يكون النظام في أعلى درجة من درجات الهرجلة والعشوائية ، مثل ذرات غاز منتشرة في صندوق ، لا تتغير أنتروبيته. ووجود سهم زمني ترموديناميكي يعني أن النظام يكون على درجة عالية من النظام والترتيب في اتجاه واحد للزمن ، وهو بحسب تعريف القانون "الزمن الماضي" .
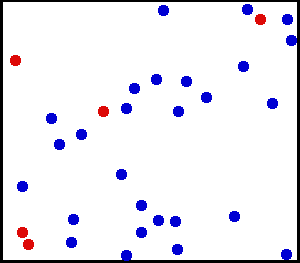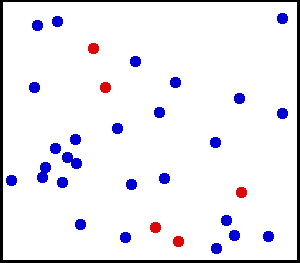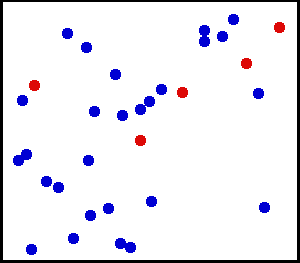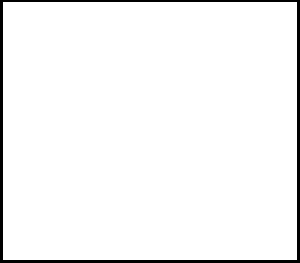
وعلى عكس قوانين الفيزياء ، نجد أن القانون الثاني للديناميكا الحرارية هو قانون لعملية إحصائية في الطبيعة ، ويختص بأنظمة تحتوي على أعداد كبيرة من الجسيمات أو الذرات في نظام عيني كبير . ومن الوجهة الاحتمالية فيمكن القول بأنه يوجد احتمال لكي تتجمع جميع عدد 6 × 1023 من الذرات (وهي ما يحتويه 1 مول من غاز) فجأة في أحد أركان الصندوق ، ولكن هذا الاحتمال ضعيف جدا جدا جدا ، ولذلك لم نر أي مخالفة عمليا لهذا القانون . وتظهر طبيعة الكون لنا أن الأحداث لا تتناظر فيه عند عكس اتجاه الزمن ، وذلك أساسا بسبب القانون الثاني للديناميكا الحرارية .
الإنتروبية والكون
ويرتبط سهم الترمويناميكا غالبا بسهم الزمن الكوني حيث أنه بصفة عامة برتبط بالأحوال الابتدائية عند نشأة الكون . فطبقا لنظرية الانفجار العظيم كان الكون في البدء شديد السخونة وكان توزيع الطاقة فيه متساويا . فإذا نظرنا إلى نظام الكون عند نشأته - وهو نظام تسود فيه قوى الجاذبية - نجد أن أنتروبيته كانت منخفضة (بالمقارنة بحالة عالية من الإنتروبيا إذا تجمعت كل المادة في جسم واحد في صورة ثقب أسود ، وهي حالة قد تحدث مستقبلا ) . ومع تمدد الكون منذ بدايته تنخفض درجة حرارته ، وبالتالي تنخفض كمية الطاقة فيه التي يمكنها أداء شغل مع مرور الزمن . بالإضافة إلى ذلك فطبقا لنظرية الاضطراب يمكن أن يحدث اضطراب في كثافة الطاقة ، مما يؤدي إلى تكون مجرات و نجوم. وعلى ذلك يمكن القول بأن للكون سهما زمنيا ترموديناميكي . و لكن ذلك الفكر لا ينظر إلي مسألة لماذا كانت إنتروبية الكون منخفضة عند نشأته . فإذا تسببت الجاذبية في إيقاف تمدد الكون ، ثم عملت على تجميع المادة في نقة واحدة ثانيا فإن درجة حرارة الكون المنكمش ستتزايد ، ويتزايد أيضا الإنتروبية بسبب تزايد الاضطرابات وربما يتكون ثقب أسود [1] حتى يحدث الانسحاق الشديد عندما تنخفض أنتروبية الكون عما هو عليه الآن.
انظر أيضا
- إنتروبيا
- سهم الزمن
- ثقب أسود
- إنتروبية المعلومات Information entropy
- عفريت ماكسويل Maxwell's demon
- كمون دينامي حراري
مراجع
- Penrose, R. الطريق الى الواقع pp. 686-734
- بوابة كيمياء فيزيائية
- بوابة الكيمياء
- بوابة الفيزياء
