أكسازولين
أكسازولين هو مركب عضوي حلقي غير متجانس وغير مشبع له الصيغة الكيميائية C3H5NO. يتألف المركب بنيوياً من حلقة خماسية حاوية على ذرتين غير متجانستين متجاورتين، ذرة نتروجين وذرة أكسجين؛ بالإضافة إلى وجود رابطة مضاعفة واحدة؛ ويطلق على مشتقاته اسم أكسازولينات.
| أكسازولين | |
|---|---|
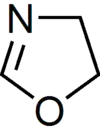 أكسازولين | |
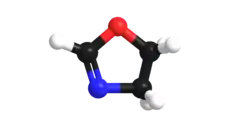 أكسازولين | |
| الاسم النظامي (IUPAC) | |
2-oxazoline | |
| تسمية الاتحاد الدولي للكيمياء | |
4,5-dihydrooxazole | |
| المعرفات | |
| CAS | 504-77-8 |
| بوب كيم (PubChem) | 68157 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | C3H5NO |
| الكتلة المولية | 71.08 غ/مول |
| المظهر | سائل |
| الكثافة | 1.07 غ/سم3 |
| نقطة الغليان | 98 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
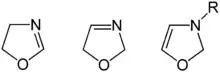
يوجد هناك ثلاثة متصاوغات للمركب، أشهرها هو 2-أكسازولين؛ أما المتصاوغان الآخران 3-أكسازولين و 4-أكسازولين فهما أقل شيوعاً؛ رغم ذلك هناك دراسات حول كيفية تحضيرهما.[2][3][4]
التحضير
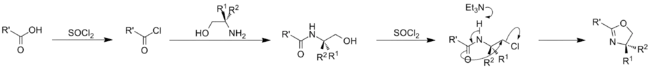
يحضر مركب 2-أكسازولين بعدة طرق تمت مراجعتها في المنشورات العلمية بشكل مكرر.[5][6][7] تتم عملية التحضير إما انطلاقاً من تفاعل الأحماض الكربوكسيلية مع كلوريد الثيونيل:[8]
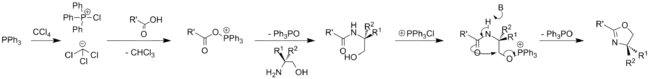
أو بأجراء تفاعل أبل Appel reaction المعدل على الأحماض الكربوكسيلية:[9]
أو بإجراء تفاعل تحلّق بين كحول أميني وألدهيد:[10]
أو انطلاقاً من النتريلات في وسط من كلورو البنزين بوجود حفاز من كلوريد الزنك:[11][12]
الاستخدامات
تستخدم الربيطات الحاوية على 2-أكسازولين في الاصطناع اللامتناظر.[13][14]
كما تستخدم في تحضير البوليميرات:[15]
اقرأ أيضاً
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/68157 — تاريخ الاطلاع: 14 أكتوبر 2016 — العنوان : Oxazoline — الرخصة: محتوى حر
- Vedejs, E.; Grissom, J. W. (1988). "4-Oxazoline route to stabilized azomethine ylides. Controlled reduction of oxazolium salts". Journal of the American Chemical Society. 110 (10): 3238–3246. doi:10.1021/ja00218a038. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Armesto, Diego; Ortiz, Maria J.; Pérez-Ossorio, Rafael; Horspool, William M. (1983). "A novel photochemical 1,2-acyl migration in an enol ester. The synthesis of 3-oxazoline derivatives". Tetrahedron Letters. 24 (11): 1197–1200. doi:10.1016/S0040-4039(00)86403-5. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Sá, Marcus C. M.; Kascheres, Albert (1996). "Electronically Mediated Selectivity in Ring Opening of 1-Azirines. The 3-X Mode: Convenient Route to 3-Oxazolines". The Journal of Organic Chemistry. 61 (11): 3749–3752. doi:10.1021/jo9518866. PMID 11667224. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Wiley, Richard H.; Bennett, Leonard L. (1949). "The Chemistry of the Oxazolines". Chemical Reviews. 44 (3): 447–476. doi:10.1021/cr60139a002. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Frump, John A. (1971). "Oxazolines. Their preparation, reactions, and applications". Chemical Reviews. 71 (5): 483–505. doi:10.1021/cr60273a003. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gant, Thomas G.; Meyers, A.I. (1994). "The chemistry of 2-oxazolines (1985–present)". Tetrahedron. 50 (8): 2297–2360. doi:10.1016/S0040-4020(01)86953-2. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Holerca, Marian N.; Percec, Virgil (2000). "1H NMR Spectroscopic Investigation of the Mechanism of 2-Substituted-2-Oxazoline Ring Formation and of the Hydrolysis of the Corresponding Oxazolinium Salts". European Journal of Organic Chemistry. 2000 (12): 2257–2263. doi:10.1002/1099-0690(200006)2000:12<2257::AID-EJOC2257>3.0.CO;2-2. مؤرشف من الأصل في 03 أكتوبر 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Vorbrüggen, Helmut; Krolikiewicz, Konrad (1993). "A simple synthesis of Δ2-oxazines, Δ2-oxazines, Δ2-thiazolines and 2-substituted benzoxazoles". Tetrahedron. 49 (41): 9353–9372. doi:10.1016/0040-4020(93)80021-K. مؤرشف من الأصل في 24 سبتمبر 2015. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Schwekendiek, Kirsten; Glorius, Frank (2006). "Efficient Oxidative Synthesis of 2-Oxazolines". Synthesis. 2006 (18): 2996–3002. doi:10.1055/s-2006-950198. مؤرشف من الأصل في 02 يونيو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Witte, Helmut; Seeliger, Wolfgang (1972). "Simple Synthesis of 2-Substituted 2-Oxazolines and 5,6-Dihydro-4H-1,3-oxazines". Angewandte Chemie International Edition in English. 11 (4): 287–288. doi:10.1002/anie.197202871. مؤرشف من الأصل في 03 أكتوبر 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Witte, Helmut; Seeliger, Wolfgang (1974). "Cyclische Imidsäureester aus Nitrilen und Aminoalkoholen". Justus Liebigs Annalen der Chemie. 1974 (6): 996–1009. doi:10.1002/jlac.197419740615. مؤرشف من الأصل في 13 نوفمبر 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة) - McManus, Helen A.; Guiry, Patrick J. (2004). "Recent Developments in the Application of Oxazoline-Containing Ligands in Asymmetric Catalysis". Chemical Reviews. 104 (9): 4151–4202. doi:10.1021/cr040642v. PMID 15352789. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Hargaden, Gráinne C.; Guiry, Patrick J. (2009). "Recent Applications of Oxazoline-Containing Ligands in Asymmetric Catalysis". Chemical Reviews. 109 (6): 2505–2550. doi:10.1021/cr800400z. PMID 19378971. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Kobayashi, Shiro; Uyama, Hiroshi (15 January 2002). "Polymerization of cyclic imino ethers: From its discovery to the present state of the art". Journal of Polymer Science Part A: Polymer Chemistry. 40 (2): 192–209. Bibcode:2002JPoSA..40..192K. doi:10.1002/pola.10090. مؤرشف من الأصل في 13 ديسمبر 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء

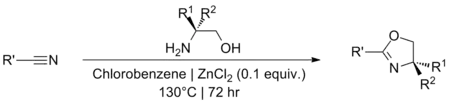
s.png.webp)
