ملوية بوابية
الملوية البوابية (باللاتينية: Helicobacter pylori) أو جرثومة المعدة نوع من البكتيريا من العصيات سلبية الغرام أليفة الهواء القليل التي تستعمر مخاطيات المعدة[1] و الإثنا عشر ، مسببة التهاباً في المخاطية، وترتبط بتطور القرحات الهضمية في المعدة والإثنا عشر وسرطان المعدة. يبقى أكثر من 80% من المصابين بهذا الجرثوم بدون إي أعراض أو مضاعفات.
| ملوية بوابية | |
|---|---|
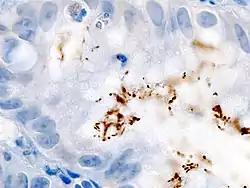 | |
| النطق | /ˌhɛlɪkɵˈbæktər paɪˈlɔəraɪ/ |
| معلومات عامة | |
| الاختصاص | الأمراض المعدية، طب الجهاز الهضمي |
يحمل نحو 50% من سكان المعمورة هذا الجرثوم، مما يجعله العدوى الأكثر انتشاراً في العالم[2]، وانتشاره أكبر في البلدان النامية منه في المتطورة. طريق العدوى غير معروف تماماً.
تاريخ الاكتشاف
تم اكتشاف الملوية البوابية في 1982 على يد العالمان الأستراليين روبن وارن وباري مارشال. أكد العالمان في ورقة بحثهم أن سبب معظم حالات قرحة والتهاب المعدة هو مستعمرات البكتريا وليس التوتر أو الطعام ذي البهارات كما أعتُقِد سابقاً. قوبلت فرضية العلاقة بين الملوية البوابية والقرحة الهضمية بفتور، لذا ولكي يثبت صحة فرضيته، قام باري مارشال بشرب صحن بتري محتويا على مزرعة من العضيات الحية المستخرجة من معدة مريض، وسرعان ما أصيب بالتهاب في المعدة. اختفت أعراض الالتهاب في غضون أسبوعين ولكنه تناول مضادات حيوية للقضاء على ما تبقى من البكتريا تحت إلحاح زوجته، حيث أن رائحة الفم الكريهة هي إحدى أعراض الالتهاب. نشرت هذه الدراسة في عام 1984 في الدورية الطبية الأسترالية وتعتبر إحدى أكثر المقالات التي شيد بها في الدورية. في العام 2005، قام معهد كارولينسكا في ستوكهولم بتقديم جائزة نوبل في الطب والفيزيولوجيا[3] إلى وارن ومارشال لاكتشافهم دور الملوية البوابية في حدوث التهاب المعدة والقرحة الهضمية. استمر الدكتور مارشال في القيام بأبحاث تتعلق بالملوية البوابية ويدير معمل بيولوجيا حيوية بجامعة غرب أستراليا في بيرث.
التشخيص
يتم تشخيص الإصابة بهذه الجرثومة عن طريق أربع فحوصات متداولة:
- الفحص الأول وهو الفحص الأهم المستخدم حاليا من الناحية العملية لتحري الجرثومة وتأكيد الشفاء بعد المعالجة. هذا الفحص يتم عن طريق (الزفير) وهو ما يعرف باسم البولة التنفسية UBT حيث يتم إعطاء المصاب مشروب اليوريا الذي يحتوي على كربون 14 أو 13 ومن ثم البحث عن غاز ثاني أكسيد الكربون CO2 الذي يتم جمعه في هواء الزفير ومعايرته بطريقة فحص الزفير باليوريا [4][5]
- الفحص الثاني بالفحص المباشر على خزعات المعدة المأخوذة بعد إجراء التنظير الهضمي العلوي، يجب أن تأخذ الخزعات من غار وقاع المعدة.
- الفحص الثالث في الدم ويتم فيه البحث عن الاجسام المضادة "جسم مضاد" يفيد هذا الفحص بأن الجسم تعرف على الجرثومة في الماضي ولكنه لا يأكد الإصابة فقد تكون الإصابة حدثت وتم الشفاء منها لكن تبقى الأضداد إيجابية.
- الفحص الرابع في البراز ويتم في البحث عن أضداد الجرثومة مباشرة في البراز وهو يسمى بالبحث عن "مولد الضد"
العلامات والأعراض
رغم أن أكثر من 80% من الأشخاص المصابين بالبكتيريا لا يشكون من أعراض، يمكن أن تكون الأعراض المرتبطة بالملوية البوابية بسيطة أو تختلف مع مرور الزمن.يمكن أن تكون غير محدّدة أو نتيجة لحالات أخرى. إنّ التهاب أو تلف بطانة المعدة الناتج عن الملوية البوابية قد يسبّب ردود فعل معتدلة أو خطيرة في المعدة: ألم في المعدة أو آلام في البطن، حمض الجزر، قلص، تقيّؤ، تشجّؤ، انتفاخ البطن والغثيان.
العلاج
عندما يتم الكشف عن وجود البكتيريا الملوية البوابية عند شخص مصاب بالقرحة الهضمية فإن الإجراء المعتاد هو القضاء على البكتيريا وإعطاء المجال للقرحة بالشفاء، ويوجد عدة خطط علاجية:
- الخطة الأولى: يجمع العلاج الرباعي بالبزموت بين الميترونيدازول والتتراسيكلين ومثبطات مضخة البروتون وأملاح البزموت. كان معدل الشفاءبهذا العلاج يزيد عن 90٪. فإن فعالية العلاج الرباعي بالبزموت تتأثر قليلاً بوجود مقاومة للميترونيدازول من 92٪ إلى 84.2٪. يتم تسويق العلاج الرباعي بالبزموت تحت اسم Pylera ويتطلب تناول أربعة عشر قرصًا يوميًا بالإضافة للعلاج بمضخات البروتون PPI. يمكن اعتبار العلاج الرباعي بالبزموت كعلاج من الدرجة الأولى للمريض الذي نشأ في منطقة جغرافية مع انتشار مقاومة للكلاريثروميسين بنسبة تزيد عن 15 ٪ أو في حالة وجود حساسية من البنسلين. مدة العلاج من 10.[6][7]
- الخطة الثانية: العلاج الرباعي بدون البزموت أو العلاج المصاحب concomitant therapy, و هو إضافة الميترونيدازول إلى العلاج التقليدي (كلاريثروميسين، أموكسيسيلين، مثبطات مضخة البروتون) لمدة 14 يومًا حيث معدل الشفاء أعلى من العلاج التقليدي 90 ٪ . في مناطق جغرافية ذات معدل انتشار مرتفع لمقاومة الكلاريثروميسين (> 15٪) وانتشار مقاومة الميترونيدازول (15-40٪) ، يكون معدل استئصال الملوية البوابية حوالي من 80٪.[8]
- الخطة الثالثة: هي تاريخيا أولى الخطط العلاجية وتتكون من كلاريثروميسين وأموكسيسيلين ومثبطات مضخة البروتون. تراجع استخدام هذه الخطة بعد انتشار المقاومة للكلاريتروميسين. المدة الموصى بها للعلاج في 2020 هي 14 يوم.[9]
- الخطة الرابعة: المعالجة المتسلسلة وتعتمد على اعطاء مثبطات مضخة الروتون PPI و الاموكسيسيللين لمدة 5 إلى 7 أيام، متبوعًا بمثبطات مضخة البروتون PPI مع كلاريثروميسين وميترونيدازول لمدة 5 إلى 7 أيام إضافية. متوسط معدل الشفاءبهذا العلاج هو 84٪ . كان هذا العلاج متفوقًا على العلاج الثلاثي التقليدي كما في الخطة الثالثة آنفا الذي استمر 7 أيام ولكن ليس على العلاج التقليدي الذي استمر14 يومًا . تتمثل عيوب هذه الاستراتيجية في انخفاض الفعالية في حالات مقاومة الكلاريثروميسين والتعقيد النسبي للمرضى.[10]
- الخطة الخامسة: عند فشل الخطة الأولى والثانية يجرى عندها تنظير هضمي علوي مع أخذ خزعات للزرع الجرثومي وتحري الحساسية للصادات الحيوية. و على ضوء حساسية الملوية البوابية للصادات يمكت اللجوء ألى العلاج بالليفوفلوكساسين أو الريفابوتين Rifabutine. مثلا اموكسيسللين مع ليفوفلوكساسين ومثبطات مضخة البروتون لمدة 10 أيام أو أموكسيسيللين مع ريفابوتين ومثبطات مضخة البروتون 10 أيام. [11]
- علاجات مساعدة: بالإضافة إلى التركيبات المختلفة للمضادات الحيوية، فإن إضافة البروبيوتيك قد يكون مفيدا. قد يكون للعصيات اللبنية و bifidobacteria تأثير مثبط على نمو الملوية البوابية، مع تحسين الآثار الجانبية لعلاجات الصادات الحيوية. تشير بعض الدراسات إلى تحسن في معدل الاستئصال وانخفاض في الآثار الجانبية. أظهر استخدام مانع الحموضة لقناة البوتاسيوم H + / K + ATPase ، Vonoprazan ، بالاقتران مع العلاج بالمضادات الحيوية، نتائج واعدة بدلاً من مثبطات مضخة البروتون التقليدية. دراسة واحدة أجريت في اليابان، وبالتالي يجب تكرارها قبل تعميمها.[12][13]
وجدت مقالة في المجلة الأمريكية للتغذية العلاجية أن تناول بكتيريا حمض اللاكتيك يؤثر على التهاب الملوية البوابية على الحيوان والإنسان مع ملاحظة أن التزود بغذاء اللبن المدعم ب ( Lactobacillus—and Bifidobacterium (AB-yogurt) أظهر تحسن في معدلات القضاء على بكتيريا الملوية البوابية عند الإنسان.[14]
لا بد من الإشارة إلى أن التأكد من الشفاء بعد العلاج ضروري ويجرى اختبار تنفس اليوريا بعد شهر من انتهاء الخطة العلاجية بشر ألا يتلقى المريض أي علاج بالصادات الحيوية خلال هذه الفترة وأن يوقف العلاج بمثبطات مضخة البروتون 15 يوما فبل الاختبار لتجنب السلبية الكاذبة.[11]
الوقاية
الملوية البوابية هو السبب الرئيسي لأمراض معينة في الجهاز الهضمي العلوي، حيث يزيد ارتفاع المقاومة للمضادات الحيوية من الحاجة إلى استراتيجية وقائية للبكتيريا[15]، وقد أظهرت دراسات عن اللقاح واسعة النطاق على الفئران نتائج واعدة.[16] هناك العديد من الأطعمة قد تكون مفيدة للوقاية وهي: الشاي الأخضر، النبيذ الأحمر، براعم القرنبيط، قنبيط أخضر، الثوم، البروبايوتيك والفليفونويد.[17]
المراجع
- "كل شئ عن بكتيريا المعدة وأنواعها". فواصل. 2020-04-14. مؤرشف من الأصل في 14 أبريل 2020. اطلع عليه بتاريخ 15 أبريل 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Pounder R.E., Ng D. (1995). "The prevalence of Helicobacter pylori infection in different countries". Aliment. Pharmacol. Ther. 9 Suppl 2: 33–9. PMID 8547526. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "The Nobel Prize in Physiology or Medicine 2005". مؤرشف من الأصل في 3 أبريل 2019. اطلع عليه بتاريخ 30 أغسطس 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Best, Lawrence Mj; Takwoingi, Yemisi; Siddique, Sulman; Selladurai, Abiram; Gandhi, Akash; Low, Benjamin; Yaghoobi, Mohammad; Gurusamy, Kurinchi Selvan (15 March 2018). "Non-invasive diagnostic tests for Helicobacter pylori infection". The Cochrane Database of Systematic Reviews. 3: CD012080. doi:10.1002/14651858.CD012080.pub2. PMID 29543326. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Dr Sulaiman Al Habib awareness brochure "فحص جرثومة المعدة هيليكوباكتر بيلوري"
- Netgen. "Traitement d'éradication d'Helicobacter pylori en 2019". Revue Médicale Suisse (باللغة الفرنسية). مؤرشف من الأصل في 27 يوليو 2020. اطلع عليه بتاريخ 12 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Venerito, Marino; Krieger, Tina; Ecker, Thomas; Leandro, Gioacchino; Malfertheiner, Peter (2013). "Meta-analysis of bismuth quadruple therapy versus clarithromycin triple therapy for empiric primary treatment of Helicobacter pylori infection". Digestion. 88 (1): 33–45. doi:10.1159/000350719. ISSN 1421-9867. PMID 23880479. مؤرشف من الأصل في 12 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gisbert, Javier P.; Calvet, Xavier (2012). "Update on non-bismuth quadruple (concomitant) therapy for eradication of Helicobacter pylori". Clinical and Experimental Gastroenterology. 5: 23–34. doi:10.2147/CEG.S25419. ISSN 1178-7023. PMID 22457599. مؤرشف من الأصل في 12 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Megraud, Francis; Coenen, Samuel; Versporten, Ann; Kist, Manfred; Lopez-Brea, Manuel; Hirschl, Alexander M.; Andersen, Leif P.; Goossens, Herman; Glupczynski, Youri (2013-01). "Helicobacter pylori resistance to antibiotics in Europe and its relationship to antibiotic consumption". Gut. 62 (1): 34–42. doi:10.1136/gutjnl-2012-302254. ISSN 1468-3288. PMID 22580412. مؤرشف من الأصل في 27 مايو 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Gatta, Luigi; Vakil, Nimish; Vaira, Dino; Scarpignato, Carmelo (2013-08-07). "Global eradication rates for Helicobacter pylori infection: systematic review and meta-analysis of sequential therapy". BMJ (باللغة الإنجليزية). 347. doi:10.1136/bmj.f4587. ISSN 1756-1833. PMID 23926315. مؤرشف من الأصل في 9 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة) - "Quel traitement ?". Helicobacter (باللغة الفرنسية). مؤرشف من الأصل في 25 نوفمبر 2020. اطلع عليه بتاريخ 12 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Shi, Xiaoguang; Zhang, Junhong; Mo, Lingshan; Shi, Jialing; Qin, Mengbin; Huang, Xue (2019-04). "Efficacy and safety of probiotics in eradicating Helicobacter pylori: A network meta-analysis". Medicine. 98 (15): e15180. doi:10.1097/MD.0000000000015180. ISSN 1536-5964. PMID 30985706. مؤرشف من الأصل في 12 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Murakami, Kazunari; Sakurai, Yuuichi; Shiino, Madoka; Funao, Nobuo; Nishimura, Akira; Asaka, Masahiro (09 2016). "Vonoprazan, a novel potassium-competitive acid blocker, as a component of first-line and second-line triple therapy for Helicobacter pylori eradication: a phase III, randomised, double-blind study". Gut. 65 (9): 1439–1446. doi:10.1136/gutjnl-2015-311304. ISSN 1468-3288. PMID 26935876. مؤرشف من الأصل في 5 مارس 2021. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Wang KY; Li SN; Liu CS; et al. (2004). "Effects of ingesting Lactobacillus- and Bifidobacterium-containing yogurt in subjects with colonized Helicobacter pylori" (PDF). المجلة الأمريكية للتغذية العلاجية. 80 (3): 737–41. PMID 15321816. مؤرشف من الأصل (PDF) في 18 مارس 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة)CS1 maint: extra punctuation (link) - NCBI - WWW Error Blocked Diagnostic نسخة محفوظة 25 أبريل 2015 على موقع واي باك مشين.
- NCBI - WWW Error Blocked Diagnostic نسخة محفوظة 13 يونيو 2013 على موقع واي باك مشين.
- NCBI - WWW Error Blocked Diagnostic نسخة محفوظة 26 أبريل 2015 على موقع واي باك مشين.
- بوابة طب
- بوابة عقد 1980
- بوابة علم الأحياء الدقيقة
 صور وملفات صوتية من كومنز
صور وملفات صوتية من كومنز أنواع من ويكي أنواع.
أنواع من ويكي أنواع.
