كينوكسالين
كينوكسالين هو مركب عضوي حلقي نتروجيني له الصيغة الكيميائية C8H6N2، ويكون على شكل بلورات صفراء إلى بنية اللون.
| كينوكسالين | |
|---|---|
 كينوكسالين | |
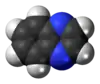 Quinoxaline molecule |
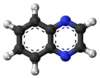 Quinoxaline molecule |
| الاسم النظامي (IUPAC) | |
Quinoxaline | |
| المعرفات | |
| رقم CAS | 91-19-0 |
| بوب كيم (PubChem) | 7045 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | C8H6N2 |
| الكتلة المولية | 130.15 غ/مول |
| المظهر | بلورات صفراء إلى بنية |
| نقطة الانصهار | 29-32 °س |
| نقطة الغليان | 220–223 °س |
| الذوبانية في الماء | ينحل في الماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
يتألف المركب بنيوياً من حلقتين مندمجتين من البنزين والبيرازين؛ وهو ينتمي بذلك إلى مركبات ديازانفثالين (هيكل نفثالين متضمن لذرتي نتروجين في البنية)، بما فيها كينازولين وفثالازين وسينولين.[3]
التحضير
تحضر مركبات الكينوكسالين على العموم من تفاعل تكاثف بين مركب أورثو ثنائي أمين مع ثنائي كيتون. ولتحضير مركب الكينوكسالين يستخدم لذلك التفاعل بين الغليوكسال مع أورثو فينيلديامين (2,1-ثنائي أمينو البنزين).[4]
 اصطناع الكينوكسالين
اصطناع الكينوكسالين
كما يمكن استخدام البنزل عوضاً عن الغليوكسال باستخدام حمض 2-يودوكسي البنزويك (IBX) كحفاز للعملية.[5]
أما المشتقات المستبدلة فتحضر عند استخدام أحماض ألفا كيتو أو ألفا كلورو الكيتونات عوضاً عن ثنائيات الكيتون.[3] كما يمكن تحضير المشتقات من اختزال الأحماض الأمينية المفلورة.[6]
الخواص
يكون الكينوكسالين في الشروط القياسية على شكل بلورات صفراء إلى بنية اللون، وهي تنحل في الماء وفي المذيبات العضوية مثل الإيثانول وثنائي إيثيل الإيثر والبنزين. يبدي المركب خواصاً قاعدية ضعيفة، حيث تبلغ قيمة pKa=0.60[7]
الاستخدامات
يستخدم الكينوكسالين ومشتقاته كربيطة في تصميم الحفازات.[8] كما تستخدم مشتقات الكينوكسالين في تحضير الأصبغة والمستحضرات الصيدلانية.
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/7045 — تاريخ الاطلاع: 6 أكتوبر 2016 — العنوان : QUINOXALINE — الرخصة: محتوى حر
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/7045
-
 واحدة أو أكثر من الجمل السابقة تتضمن نصاً من منشور أصبح الآن في الملكية العامة: هيو تشيشولم, المحرر (1911). "Quinoxalines". موسوعة بريتانيكا. 22 (الطبعة الحادية عشر). مطبعة جامعة كامبريدج. صفحة 760. الوسيط
واحدة أو أكثر من الجمل السابقة تتضمن نصاً من منشور أصبح الآن في الملكية العامة: هيو تشيشولم, المحرر (1911). "Quinoxalines". موسوعة بريتانيكا. 22 (الطبعة الحادية عشر). مطبعة جامعة كامبريدج. صفحة 760. الوسيط |CitationClass=تم تجاهله (مساعدة)CS1 maint: ref=harv (link) - 2,3-Pyrazinedicarboxylic Acid" Reuben G. Jones and Keith C. McLaughlin Org. Synth. 1950, 30, 86. doi:10.15227/orgsyn.030.0086. This paper describes the preparation of quinoxaline as an intermediate.
- Heravi, Majid M. (2006). "Facile synthesis of quinoxaline derivatives using o-iodoxybenzoic acid (IBX) at room temperature". Arkivoc. 2006 (16). doi:10.3998/ark.5550190.0007.g02. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Xiang-Hong Wu; Gang Liu; et al. (2004). "Solution-phase reductive cyclization of 2-quinoxalinol analogs: Systematic study of parallel synthesis". Mol. Diver. 8 (2): 165–147. doi:10.1023/B:MODI.0000025639.89179.60. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Brown, H.C.; et al. (1955). Baude, E.A.; Nachod, F.C. (المحررون). Determination of Organic Structures by Physical Methods. New York: Academic Press. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Xianghong Wu; Anne E. V. Gorden (2007). "Regioselective Synthesis of Asymmetrically Substituted 2-Quinoxalinol Salen Ligands". J. Org. Chem. 72 (23): 8691–8699. doi:10.1021/jo701395w. PMID 17939720. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء