سينولين
سينولين هو مركب عضوي حلقي نتروجيني له الصيغة الكيميائية C8H6N2، ويكون على شكل بلورات عديمة اللون.
| سينولين | |
|---|---|
 سينولين | |
 Cinnoline molecule |
 Cinnoline molecule |
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
Cinnoline | |
| المعرفات | |
| رقم CAS | 253-66-7 |
| بوب كيم (PubChem) | 9208 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | C8H6N2 |
| الكتلة المولية | 130.15 غ/مول |
| المظهر | بلورات عديمة اللون |
| نقطة الانصهار | 40–41 °س |
| نقطة الغليان | 114 °س (عند 0.4 هيكتوباسكال) |
| حموضة (pKa) | 2.64 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
يتألف المركب بنيوياً من حلقتين مندمجتين من البنزين والبيريدازين؛ وهو ينتمي بذلك إلى مركبات ديازانفثالين.
التحضير
حضر المركب لأول مرة من تفاعل تحلق للألكاين o-C6H4(NH2)C≡CCO2H في الماء ليعطي حمض 4-هيدروكسي سينولين-3-كربوكسيليك؛ والتي يمكن إجراء عملية نزع كربوكسيل عليه ثم باختزال مجموعة الهيدروكسيل للحصول على السينولين. يعرف هذا التفاعل باسم اصطناع ريختر للسينولين.[3]
كما يمكن أن تتم عملية التحضير من تفاعل نزع هيدروجين من ثنائي هيدرو السينولين باستخدام أكسيد الزئبق الثنائي المحضر حديثاً، ويعزل السينولين حينئذ على شكل هيدروكلوريد.[4]
أما مشتقات السينولين، والتي تعرف باسم سينولينات، فتحضر بتفاعل يسمى اصطناع فيدمان-شتورمر Widman–Stoermer synthesis؛[5] وهو تفاعل إغلاق للحلقة باستخدام α-فاينيل الأنيلين مع حمض هيدروكلوريك ونتريت الصوديوم.
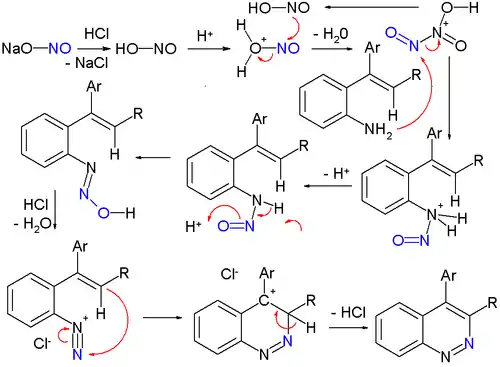
يتحول نتريت الصوديوم في التفاعل إلى حمض النتروز، والذي يشكل حينها مركب وسطي إلكتروفيلي (محب للإلكترون) وهو ثلاثي أكسيد ثنائي النتروجين، والذي يشكل مركب وسطي آخر من نتروزامين، والذي يفقد الماء ليشكل ملح ديازونيوم، والذي يتفاعل مع الفاينيل في تفاعل إغلاق الحلقة. تعد آلية التفاعل هذه قريبة من حيث المبدأ لآلية تفاعل اصطناع بامبيرجر للتريازين.
الخواص
يوجد السينولين في الشروط القياسية على شكل بلورات عديمة اللون؛ وهي تنصهر بين درجتي الحرارة 40 و 41 °س.[6]
اقرأ أيضاً
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/9208 — تاريخ الاطلاع: 6 أكتوبر 2016 — العنوان : CINNOLINE — الرخصة: محتوى حر
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/9208
- Victor von Richter (1883). "Über Cinnolinderivate". Chemische Berichte. 16: 677–683. doi:10.1002/cber.188301601154. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Parrick, J.; Shaw, C. J. G.; Mehta, L. K. (2000). "Pyridazines, cinnolines, benzocinnolines and phthalazines". Rodd's Chemistry of Carbon Compounds. 4 (الطبعة 2nd). صفحات 1–69. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Bradford P. Mundy; Michael G. Ellerd; Frank G. Jr. Favaloro (2005). Name Reactions and Reagents in Organic Synthesis. ISBN 0-471-22854-0. الوسيط
|CitationClass=تم تجاهله (مساعدة) - J. S. Morley: Cinnolines. Part XX VII. The Preparation and Nitration of Cinnoline., J. Chem. Soc., 1951, S. 1971–1975.
- بوابة الكيمياء
