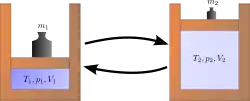
عملية عكوسية
عملية عكوسية في الكيمياء و الفيزياء (بالإنجليزية :reversible process) تسمى عملية أو دورة بأنها عكوسية عندما يمكن عكسها بواسطة تغير طفيف لأحد خصائص النظام بدون فقد للطاقة. [1] ونظرا لأن التغيرات في النظام تكون طفيفة جدا يكون النظام خلال هذا التغير في حالة توازن حراري. وتحتاج عملية عكوسية إلى فترة زمنية لكي تتم ، ولذلك لا تتم عملية أو دورة عكوسية مثاليا في وقت قصير . وتتسم دورة عكوسية بعدم تغير طاقة النظام وما حوله أثناء الدورة ، أي تكون طاقة النظام وما حوله هي نفسها عند بدء العملية وعند نهايتها .[2]
كما يمكن تعريف العملية العكوسية بأنها العملية التي يمكن عكسها بعد انتهائها من غير حدوث أي تغير فيها ولا في الجو المحيط . وبصيغة الحركة الحرارية thermodynamic تعرف العملية أو الدورة بأنها عملية تحول من حالة ترمويناميكية ابتدائية إلى حالة ترموديناميكية أخرى .
غير العكوس
{مقالة رئيسية :عملية غير عكوسية}
تسمى العملية التي لا تكون عكوسية بأنها عملية "غير عكوسية" . وعند أداء عملية غير عكوسية يتغير النظام ولا يكون النظام خلال سريان العملية في حالة توازن حراري. وقد يكون النظام عند نفس النقطة في دورة عكوسية في نفس الحالة ، ولكن الجو المحيط به يكون قد تغير بعد كل دورة .[2]
أمثلة على تغير الحالات غير عكوسية نذكرها مثل انتقال الحرارة من جسم ساخن إلى جسم بارد ، و اختلاط غازين ، أو اختلاط السوائل ، والاحتكاك حيث تتحول طاقة حركة إلى طاقة حرارية ، وعملية تنفيث الضغط (حيث يتغير الضغط الماء أو الغاز إلى حركة) .
الإحتكاك في الآلات
في العملية العكوسية تتغير حالة النظام بطريقة أن نتيجة التغير الكلي لإنتروبية النظام والمحيط تساوي صفرا . وتعرّف الدورة العكوسية كيف تكون كفاءة آلة حرارية في الهندسة الميكانيكية : الدورة العكوسية هي الدورة التي لا يحدث خلالها ضياعا من حرارة النظام في صورة عادم ، عندئذ تكون كفاءة الآلة على أعلى مستواها (اقرأ دورة كارنو).
وعلى سبيل المثال ، عندما يتغير ضغط المكبس في محرك سيارة تغيرا بسيطا يحدث احتكاك بين المكبس والأسطوانة ، ولذلك لا تكون تلك الدورة عكوسية ، إذ تـُفقد بعض الطاقة في الاحتكاك . .[3] ورغم أن النظام قد اعتراه تغير طفيف فقط عند ازاحته من حالة التوازن الحراري ، إلا أن قدرا ولو بسيطا من الحرارة قد ضاع بسبب الاحتكاك ، ولا يمكن استعادته عن طريق تحريك المكبس في الاتجاه العكسي .
المصادر
- Sears, F.W. and Salinger, G.L. (1986), Thermodynamics, Kinetic Theory, and Statistical Thermodynamics, 3rd edition (Addison-Wesley.)
- Zumdahl, Steven S. (2005) "10.2 The Isothermal Expansion and Compression of an Ideal Gas." Chemical Principles. 5th Edition. (Houghton Mifflin Company)
- Giancoli, D.C. (2000), Physics for Scientists and Engineers (with Modern Physics), 3rd edition (Prentice-Hall.)