طرد مركزي تبايني
الطرد المركزي التبايني (بالإنجليزية: Differential centrifugation) الطرد المركزي هو جهاز لفصل الجسيمات من محلول وفقا لحجمها وشكلها، والكثافة، واللزوجة من سرعة متوسطة والدوار في محلول، والجسيمات التي تكون كثافتها أعلى فإنها تكون مصدر المذيبات (الرواسب) ويمكن الزيادة من معدلات الترسيب باستخدام قوة الطرد المركزي، أما الجزيئات التي تكون أخف وزنا فإنها تطفو إلى أعلى. وهذا كلما زاد الفرق في الكثافة وسرعة التحرك. ويستند الفاصل على حجم وكثافة، مع الجسيمات الأكبر حجما وأكثر كثافة التكوير في قوى الطرد المركزي يكون أقل.
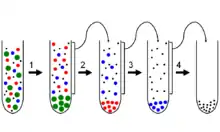
وأبسط شكل من أشكال الفصل المركزي عن طريق الطرد المركزي هو الطرد التفاضلي (ألتبايني)، ويسمى أحياناً التكوير التفاضلي. وهو إجراء شائع في علم الأحياء الدقيقة وعلم الخلايا المستخدمة لفصل بعض العضيات من الخلايا الكاملة لمزيد من التحليل لأجزاء معينة من الخلايا. وفي هذه العملية يتم استدارة عينة حول محور مركزي، الأمر الذي أدى لتجربة ميدانية للطرد المركزي بحيث مكوناته تميل إلى الابتعاد عن محور الدوران. ويتم تنفيذ الطرد المركزي باستخدام أداة جهاز للطرد المركزي.
وعلى الرغم من الاختلاف الكبير في الحجم وسعة وحدة التخزين، والسرعة، وجميع أجهزة الطرد المركزي لديها عنصر الدورية قادرة على إجراء عينات ( عادة في أنابيب). يتم تحديد قوة الطرد المركزي الناتجة عن طريق جهاز للطرد المركزي من سرعة دوران والمسافة من العينة من محور الدوران. وقوة الطرد المركزي وعادة ما يتم مقارنة مع قوة الجاذبية. وأن قوة من 1 غرام تساوي قوة الجاذبية على سطح الأرض باعتبارها قوة الطرد المركزي النسبية.
النظرية
إذا كانت قوة الجاذبية عالية، يكون ترسّب الجزيئات الصغيرة سريع جداً. وعند استخدام جهاز الطرد المركزي يجب أن يتم تعديل قانون ستوكس لحساب التباين في قوة الجذب مع المسافة من مركز الدوران.
حيث أن:
إعداد عينة
[1][3] قبل أن يتم تنفيذ عملية الطرد المركزي التبايني لفصل أجزاء مختلفة من الخلية، يجب أن تكون عينة الأنسجة متجانسة . في هذه العملية الخلاط (blender) المستخدم بالعادة يكون قطعة من الخزف (porcelain) يطابق الوعاء بالشكل والحجم، يكون الوعاء في معظم الحالات من زجاج قابل للغليان.

يتم سحق العينة أولاً وإضافة المحلول المنظم (buffer solution) إليها وبالتالي سوف يتكون محلول سائل معلقة فيه الجزيئات.
المحلول المنظم
المحلول المنظم هو محلول يحافظ على درجة الحموضة عند قيمة ثابتة، يكون على أشكال متعددة منها ( الكثيف " جلي"، أو سائل )، يستخدم لوضع العينة فيه دون التأثير على التفاعلات الكيميائية أو على الضغط الإسموزي . في أغلب الحالات يكون المحلول من السكروز وفي حالات خاصة يكون محلول ملحي.
بعد ذلك نبدأ العمل بواسطة الخلاط (blender) بحيث يكون مرتبط بجهاز دائري عالي السرعة، توضع العينة و يتم دفع مسحوق العينة إلى جدار وعاء العينة مع تشغيل محور الدوران فيتم تأريض العينة عن طريق قطعة الخزف وجدار العينة إلى أجزاء صغيرة، وهذه العملية تسمى عملية شحذ ( طحن )، بحيث تعمل على تكسير الأغشية الخلوية لخلايا العينة، وترك العضيات عالقة في المحلول. وهذا ما يسمى بعملية التجانس. و جزء من الخلايا التي تبقى بعد عملية الطحن تتضرر وهذه الخلايا سيتم معالجتها في مراحل لاحقه بعملية الطرد المركزي.
التوازن المتدرج للطرد المركزي
المعروف أيضاً باسم"isopycnic density gradiant centerfugation" هو نوع من اجراءات الطرد المركزي المستخدمة على نطاق واسع في الكيمياء الحيوية لفصل الجزيئات على اساس'isopycnic' –كثافة الجزيء التي تجعله قابل للطفو ويتحقق ذلك من خلال دوران المكونات البيولوجية بقوة عالية خلال فترات طويلة من الزمن في مخازن أو محاليل التي تحتوي على كميات متفاوتة من الجزيء المتوفر.
الترسيب الذي يعتمد على التوازن
يعتمد مبدأ عمله في حل مثل كلوريد السيزيوم أو السكروز إلى جزيئات منفصلة على اساس من الكثافة الفردية (الكتلة/الحجم) ويستخدم على أنها عملية تنقية للطرد المركزي ويتم اعداد المحلول مع اكثف جزء من التدرج في الاسفل (أي ان الجزيئات الأقل كثافة تكون في الاسفل)، كل عائدات الجسيمات أما صعودا أو هبوطا مختلفة الكثافة فهي قابلة للمقارنة، وهذا التدرج في الكثافة المستمر اعد بطريقة متدرجة. على سبيل المثال، عند استخدام السكروز لاعداد تدرجات الكثافة وبتراكيز مختلفة للسكروز (50% و60%) فانه يتم فصل المكونات بناء على كثافتها فتكون النتيجة بان يطفو السكروز ذو التركيز (50%) على السكروز ذو التركيز (60%).وتتم هذه العملية للخلايا بانه في البداية يتم ازالة خلايا الانسجة عن طريق اعدادها في منطقة منعزلة ووضعها في طرد مركزي لمدة ساعة تقريبا 100,000x، ويمكن ملاحظة أن المكونات الخلوية المختلفة المتساوية في الكثافة أصبحت ضمن الطبقة الواحدة، ومن خلال تعديل كثافة طبقة لتتناسب مع نوع الخلايا، يمكن اثراء مكونات خلوية معينة. ومن فوائد كلوريد السيزيوم في هذه العملية في انه يسمح لمزيد من الدقة في فصل الجسيمات اعتمادا على كثافتها، وعلى سبيل المثال فانه يمكن فصل جزيئات ال DNA دون عن النظائر الثقيلة باستخدام عنصر السيزيوم.
الطرد المركزي الايزوبيكنيكي "Isopycnic centrifugation" والمعروف أيضا باسم "الطرد المركزي المتدرج للكثافة" أو" تواززن الترسيب"، وهو اسلوب يستخدم لفصل الجزيئات على اساس كثافة الطفو، "كلمة الايزوبيكنيكي تعني كثافة الطفو" يتم في العادة توليد ذاتي لكثافة التدرج عبر توازن الترسيب، ومن ثم تحليل الجزيئات التي تطابق كثافة الجزيء. لتوضيح هذه العملية على سبيل المثال لجزيئات الـحمض نووي ريبوزي منقوص الأكسجين، يتم وضع خليط من كلوريد السيزيوم وDNA في أجهزة الطرد المركزي لعدة ساعات في سرعة عالية لتوليد قوة من حوالي 5^10 ج "جاذبية ارضية"، وبعد مرور بعض الوقت يتم تشكيل التدرج من ايونات السيزيوم، والناجمة عن قوتين متعارضتين :نشر وقوة الطرد المركزي، فإن الجزيئات المترسبة (أيونات السيزيوم) الرواسب بعيدا عن الدوار، وتصبح أكثر تركيزا بالقرب من أسفل الأنبوب. تنشأ قوة ناشر بسبب التدرج تركيز كلوريد السيزيوم الإذابة بالإكترونات وموجهة دائما نحو وسط الدوار. التوازن بين هاتين القوتين يولد التدرج الكثافة مستقرة في محلول كلوريد السيزيوم، وهو أكثر كثافة بالقرب من أسفل الأنبوب، وأقل كثافة بالقرب من أعلى.
وبعد ذلك يتم فصل جزيئات DNA على أساس الحصص النسبية من AT (الأدنين وقاعدة الثايمين أزواج) لGC (جوانين وقاعدة السيتوزين أزواج). على زوج قاعدة AT لها وزنها الجزيئي أقل من زوج قاعدة GC، وبالتالي، لاثنين من جزيئات DNA متساوية الطول، واحد مع نسبة أكبر من AT أزواج قاعدة لديهم كثافة أقل، جميع العوامل الأخرى متساوية. كما سيتم فصل أنواع مختلفة من الأحماض النووية في نطاقات، على سبيل المثال RNA هو أكثر كثافة من DNA البلازميد supercoiled، وهو أكثر كثافة من الحمض النووي الكروموسومات الخطية.
.jpg.webp)
الطرد المركزي السكروزي المتدرج
الطرد المركزي السكروزي المتدرج، هو نوع من الطرد المركزي غالباً ما يستخدم لتنقيه الفيروسات المغلفه(enveloped viruses) ذات كثافه (1,1-1,2 غ /سم مكعب)، والرايبوسومات، ولأغشية...ألخ. وهناك طريقتان من هذا النوع من الطرد وهما الطرد المركزي المتوازن، والطرد المركزي الغير متوازن.
عادةً في الطرد المركزي المتوازن، يتم إنشاء مستوى كثافة السكروز عن طريق اضافه تراكيز منخفضة من السكروز بلطف على تراكبز عاليه منه في انبوب الطرد المركزي. على سبيل المثال، قد تتكون المستويات من طبقات تمتد من 70% إلى 20% بحيث تكون كل طبقه 10% (وهذا متغير بدرجة كبيرة اعتماداً على العينة المراد تنقيتها). عوضاً عن ذلك، يمكن استخدام الأجهزة المعروفه مثل الخلاطات أو صانعات التدرج لتكوين المستويات في التدرج. وهذه الأجهزة تتكون من حجرتين، تحتوي على محاليل بتراكبز مختلفه، والتي تمزج تدريجياً لإنشاء الاختلاف في المستويات(التدرج)، إذ تستخدم هذه الأجهزة لإنشاء تدرج خطي أو مقعر أو محدب أو حتى تدرجات أُسيه.
أما طريقة الطرد المركزي الغير متوازن فهي مشابهة للطرد المتوازن، ولكن التجربة هنا تجري إلى نقطة معينة، (هذه التدرجات تسمى تدرجات السرعة). على الرغم من ان الجزيئات الأكثر كثافه ستكون في المستويات السفلي الا انها لا تبعد كثيراً عن المستوى العلوي، حيث ستستقر قبل الوصول إلى التوازن (ليس نفس مستوى الكثافة) فإن الجسيمات المطلوبة ستكون على مسافة معروفة من السطح العلوي، ويتم جمع ما في هذا التدرج ويسمى جزء. وعند توقف عمليه الطرد يتم جمع الأجزاء من خلال عده طرق، ولعل أسهل طريقه لازاله محلول السكروز هي عن طريق ثقب اسفل الأنبوب وإخراج المحلول بلطف كي لا تختلط الطبقات، ومن ثم يتم استخراج الجزء من البروتين أو المواد المطلوبة للاحتفاظ بها. ومن ثم تقسم الجسيمات المستخرجة إلى كسور أو أرقام لتحديد العضيات أو الجزيئات المطلوبة.
الطرد المركزي فائق السرعة
هو الطرد الأمثل للدوران بسرعة عالية جداً، قادر على احداث تسارع يصل إلى 2000000gيتكون من مبرد وحجرة الضغط فيها قليل مع دوار تحركه قوة كهربائية لها سرعة دوران عالية جدا، وهناك نوعان من الطرد المركزي فائق السرعة :الطرد المركزي التحليلي (ويستخدم لتحديد السرعة للجزيئات الكبيرة ومن ثم المساعدة في تحديد وزنها وأشكالها)، الطرد المركزي الإعدادي (يستخدم لفصل الجزيئات الحية مثل عضيات الخلية والبروتينات والأغشية والحمض النووي) وكلاهما له أهمية كبيرة في علم الأحياء الدقيقة والكيمياء الحيوية.
تاريخه
عام 1925 قام العالم ثيودر سفيدبيرج باختراع الطرد المركزي التحليلي وحصل على جائزة نوبل في الكيمياء حيث كان يعمل في أبحاث على البروتينات. عام 1946 قام العالم سبينكو بتمييز أنواع الطرد المركزي فائق السرعة حسب تصميم معين وبعد ذلك اعتبر هذا التصميم معقدا وصعب التعامل به تجاريا فعدل هذا التصميم إلى تصميم أكثر بساطة ومع ذلك بقيت المبيعات قليلة جدا مما أدخله في حالة افلاس ثم تدخل شركة لترفع نسبة المبيعات وتنقذه.
آلية العمل
بعد تحضير العينة يتم وضعها في الطرد المركزي فائق السرعة، وتوضع العينة في أنبوب متصل مع الدوار، حيث تصل سرعة الدوران إلى مئة ألف دورة في الدقيقة أو مئة وخمسون ألف دورة في الدقيقة حسب نوع النظام، وقوة الطرد المركزي تصل إلى مليون درجة هذا ما يسبب ترسب الجزيئات الكبيرة. ولأن كل جزء من الخلية له حجم وكثافة مختلفان عن الأجزاء الأخرى فكل جزء يترسب على قوة طرد معينة ولهذا نحصل على طبقات مختلفة من أجزاء الخلية أو العينة حسب نوعها في كل مرة نعمل على إعادة العملية نفسها بالتخلص من الراسب وإعادة الجزء العلوي(المحلول) إلى الجهاز ثانية حتى نحصل على الجزء المطلوب.
المراجع
- Differential centrifugation - Wikipedia, the free encyclopedia
- (adapted from A. Bregman, Laboratory investigations in cell and molecular biology, 1990)
- Becker's World of the cell
- بوابة الكيمياء الحيوية
