صفات معقدة (وراثة)
الصفات المعقدة (بالإنجليزية: Complex traits)، والمعروفة أيضًا باسم السمات الكمية (بالإنجليزية: quantitative traits)، هي سمات لا تتصرف وفقًا لقوانين الوراثة المندلية البسيطة. وبشكل أكثر تحديدًا، لا يمكن تفسير توارثها بالفصل الجيني لجين واحد، وتُظهر هذه السمات نطاقًا مستمرًا من الاختلاف وتتأثر بالعوامل البيئية والوراثية. وبالمقارنة مع الصفات المندلية الصارمة، فإن الصفات المعقدة أكثر شيوعًا بكثير، ولأنها يمكن أن تكون متعددة الجينات بشكل كبير، يتم دراستها باستخدام تقنيات إحصائية مثل رسم خرائط لموقع الصفة الكمي بدلاً من أساليب الوراثة الكلاسيكية.[1] وتشمل أمثلة السمات المعقدة الطول، والنظم اليومي، وحركية الإنزيمات، والعديد من الأمراض بما فيها داء السكري ومرض باركنسون. وأحد الأهداف الرئيسية للبحث الوراثي اليوم هو فهم أفضل للآليات الجزيئية التي تعمل من خلالها المتغيرات الجينية للتأثير على السمات المعقدة.

تاريخ
 مقالة مفصلة: تاريخ علم الجينات
مقالة مفصلة: تاريخ علم الجينات
عندما أعيد اكتشاف أعمال مندل في الوراثة في عام 1900، ناقش العلماء ما إذا كانت قوانين مندل يمكن أن تفسر الاختلاف المستمر الملحوظ في العديد من السمات. وزعمت إحدى المجموعات المعروفة باسم مختصي الإحصاء الحيوي أن السمات المستمرة، مثل الطول كانت وراثية إلى حد كبير، ولكن لا يمكن تفسيرها من خلال وراثة العوامل الوراثية المندلية الوحيدة. وكان العمل الذي قام به رونالد فيشر عام 1918 قد حسم في الغالب الجدل من خلال إظهار أن التباين في السمات المستمرة يمكن حسابه إذا كان هناك العديد من العوامل قد ساهمت بشكل إضافي في كل سمة.[2] ومع ذلك، فإن عدد الجينات المشاركة في مثل هذه السمات بقي غير محدد. وحتى وقت قريب، كان من المتوقع أن يكون للمواقع الجينية أحجام تأثير معتدلة وكل منها يفسر نسبة من الوراثة.[3] وبعد الانتهاء من مشروع الجينوم البشري في عام 2001، بدا أن التسلسل ورسم الخرائط للعديد من الأفراد سيسمح قريبا بفهم كامل البنية الوراثية للصفات. ومع ذلك، فإن الاختلافات الوراثية التي تم اكتشافها من خلال دراسات الارتباط على مستوى الجينوم لم تمثل سوى نسبة صغيرة من التوريث المتوقع؛ على سبيل المثال، في حين يقدر أن الطول قابل للتوريث بنسبة 80-90٪، فإن الدراسات الأولية حددت فقط المتغيرات التي تمثل 5٪ من هذا التوريث.[4] وأظهرت الأبحاث اللاحقة أن معظم التوارث الناقص يمكن حسابه من خلال المتغيرات المشتركة التي أخطأتها دراسات الارتباط على مستوى الجينوم؛ لأن أحجام تأثيرها انخفضت إلى أقل من عتبات الدلالة، وتم احتساب نسبة أصغر من المتغيرات النادرة ذات أحجام تأثير أكبر، على الرغم من أن بعض الصفات النادرة مثل التوحد تلعب دورًا مهيمنًا أكثر.[5][6][7] وفي حين أنه تم تحديد العديد من العوامل الوراثية المشاركة في الصفات المعقدة، فإن تحديد مساهماتها المحددة في أنماط المظهر الظاهري - وتحديدًا الآليات الجزيئية التي تعمل من خلالها - لا يزال يمثل تحديًا كبيرًا.[8]
الأساليب
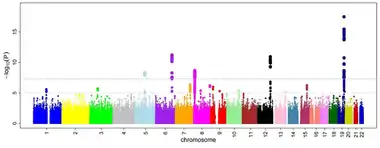
تخطيط المواقع الجينية للصفات المعقدة
موقع السمة الكمية هو جزء من الجينوم المرتبط بالتغير في سمة كمية أو معقدة. ولتحديد ذلك الموقع، يتم إجراء رسم الخرائط له على أفراد ذوي أنماط جينية مختلفة. وفي كثير من الأحيان، ينحدر هؤلاء الأفراد من نفس السلف. وتشمل الخرائط إما تسلسل الجينوم الكامل أو التنميط الجيني للعديد من المواقع المحددة في جميع أنحاء الجينوم، ثم يتم قياس الظواهر ذات الأهمية. وعلى سبيل المثال، مستويات التعبير لكل جين في الجينوم هي نمط ظاهري واحد يتم قياسه بشكل شائع (تسمى المواقع المصاحبة بمواقع السمات الكمية التعبيرية (eQTLs)). وفي كل موقع، يتم تجميع الأفراد حسب نمطهم الوراثي، ويتم إجراء اختبارات إحصائية لتحديد ما إذا كانت قيم الصفات المقيسة لمجموعة واحدة تختلف بشكل كبير عن المتوسط الكلي لجميع المجموعات. وقد لا تكون المواقع المحددة عبارة عن مواقع السمات الكمية نفسها، ولكن من المحتمل أن تكون تلك المواقع بها اختلال في الارتباط مع الموقع الذي يؤثر فعليًا على السمات.
دراسة الارتباط على مستوى الجينوم
إن دراسة الارتباط على مستوى الجينوم هي طريقة شبيهة بتخطيط مواقع السمات الكمية المستخدم لتحديد المتغيرات المرتبطة بالصفات المركبة. ويختلف تخطيط الارتباط عن رسم خرائط المواقع بشكل أساسي في أن تخطيط الارتباط يتم فقط مع مجموعات التزاوج العشوائي؛ لأنه يتم اختبار جميع الأليلات في السكان في نفس الوقت، ويمكن مقارنة الأليلات المتعددة في كل موقع.[1]
البنية الجينية للصفات المعقدة
في الآونة الأخيرة، مع الزيادات السريعة في البيانات الجينية المتاحة، بدأ الباحثون بتوصيف أفضل للهيكل الجيني للصفات المركبة. ومن المفاجآت ملاحظة أن معظم المواقع التي تم تحديدها في دراسة الارتباط على مستوى الجينوم موجودة في المناطق غير المشفرة من الجينوم. ولذلك، بدلاً من تغيير تسلسل البروتين مباشرة، من المحتمل أن تؤثر هذه الاختلافات الوراثية على تنظيم الجينات.[9] ولفهم الآثار الدقيقة لهذه الاختلافات، تم استخدام رسم خرائط مواقع السمات الكمية لفحص البيانات من كل خطوة من خطوات تنظيم الجينات. وعلى سبيل المثال، يمكن أن يساعد رسم خرائط بيانات تسلسل الحمض النووي الريبوزي في تحديد تأثيرات الاختلافات على مستويات تعبير الحمض النووي الريبوزي الرسول، والتي من المفترض أن تؤثر بعد ذلك على أعداد البروتينات المترجمة. وأظهر التحليل الشامل لمواقع السمات الكمية المتضمَن في خطوات تنظيمية مختلفة، مثل نشاط المحفز، ومعدلات النسخ، ومستويات التعبير للحمض النووي الريبوزي الرسول، ومستويات الترجمة، ومستويات التعبير البروتين أن نسب عالية من مواقع السمات الكمية مشتركة، مما يشير إلى أن التنظيم يتصرف بمثابة "سلسلة منظمة متسلسلة" مع الاختلافات الوراثية التي تؤثر على جميع مستويات التنظيم.[10] وتعمل العديد من هذه الاختلافات بالتأثير على ربط عامل النسخ والعمليات الأخرى التي تغير وظيفة الكروماتين، وهي الخطوات التي تحدث قبل وأثناء نسخ الحمض النووي الريبوزي.[10]
ولتحديد النتائج الوظيفية لهذه الاختلافات، ركز الباحثون بشكل كبير على تحديد الجينات الرئيسية، والمسارات، والعمليات التي تقود سلوك السمات المعقدة، وكان الافتراض المتأصل هو أن معظم الاختلافات ذات الدلالة الإحصائية لها أكبر الأثر على السمات؛ لأنها تعمل من خلال التأثير على هذه المحركات الرئيسية.[8][11] وعلى سبيل المثال، افترضت إحدى الدراسات أن هناك جينات محورية لوظيفة الشبكات الجينية التنظيمية تحد من معدل الإصابة،[12] وحددت دراسات أخرى التأثيرات الوظيفية للجينات الرئيسية والطفرات على الاضطرابات، بما في ذلك التوحد وانفصام الشخصية.[7][13] ومع ذلك، فإن تحليل عام 2017 لبويل وآخرين يناقش أنه في حين أن الجينات التي تؤثر مباشرة على السمات المعقدة موجودة، فإن الشبكات التنظيمية مترابطة للغاية بحيث يؤثر أي جين مُعبَّر عنه في وظائف هذه الجينات "الأساسية"، وفي حين أن كل هذه الجينات "الطرفية" لها تأثيرات صغيرة، فإن تأثيرها المشترك يفوق بكثير مساهمات الجينات الأساسية نفسها. ولدعم الفرضية القائلة بأن الجينات الأساسية تلعب دورًا أصغر من المتوقع، يصف المؤلفان ثلاثة ملاحظات رئيسية هي: انتشار الوراثة للصفات المعقدة على نطاق واسع بشكل متكرر عبر الجينوم، وأنه لا يبدو أن التأثيرات الجينية تتوسطها وظيفة محددة من النوع الخلوي، ومساهمة الجينات في الفئات الوظيفية ذات الصلة بشكل متواضع أكثر في التوريث من الجينات الأخرى.[8] وأحد البدائل لتلك الفرضية هو فكرة أن الجينات المحيطية لا تعمل عن طريق تغيير الجينات الأساسية ولكن عن طريق تغيير الحالات الخلوية، مثل سرعة انقسام الخلايا أو استجابة الهرمون.[14][15]
المراجع
- Griffiths AJ, Wessler SR, Carroll SB, Doebley JF. Introduction to genetic analysis (الطبعة Eleventh). New York, NY. ISBN 978-1-4641-0948-5. OCLC 900650999. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Fisher RA (1919). "XV.—The Correlation between Relatives on the Supposition of Mendelian Inheritance". Earth and Environmental Science Transactions of the Royal Society of Edinburgh. 52 (2): 399–433. doi:10.1017/S0080456800012163. مؤرشف من الأصل في 31 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gibson G (January 2012). "Rare and common variants: twenty arguments". Nature Reviews. Genetics. 13 (2): 135–45. doi:10.1038/nrg3118. PMC 4408201. PMID 22251874. مؤرشف من الأصل في 25 أغسطس 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Manolio TA, Collins FS, Cox NJ, Goldstein DB, Hindorff LA, Hunter DJ, et al. (October 2009). "Finding the missing heritability of complex diseases". Nature. 461 (7265): 747–53. doi:10.1038/nature08494. PMC 2831613. PMID 19812666. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Shi H, Kichaev G, Pasaniuc B (July 2016). "Contrasting the Genetic Architecture of 30 Complex Traits from Summary Association Data". American Journal of Human Genetics. 99 (1): 139–53. doi:10.1016/j.ajhg.2016.05.013. PMC 5005444. PMID 27346688. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Marouli E, Graff M, Medina-Gomez C, Lo KS, Wood AR, Kjaer TR, et al. (February 2017). "Rare and low-frequency coding variants alter human adult height". Nature. 542 (7640): 186–190. doi:10.1038/nature21039. PMC 5302847. PMID 28146470. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Krumm N, Turner TN, Baker C, Vives L, Mohajeri K, Witherspoon K, Raja A, Coe BP, Stessman HA, He ZX, Leal SM, Bernier R, Eichler EE (June 2015). "Excess of rare, inherited truncating mutations in autism". Nature Genetics. 47 (6): 582–8. doi:10.1038/ng.3303. PMC 4449286. PMID 25961944. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Boyle EA, Li YI, Pritchard JK (June 2017). "An Expanded View of Complex Traits: From Polygenic to Omnigenic". Cell. 169 (7): 1177–1186. doi:10.1016/j.cell.2017.05.038. PMC 5536862. PMID 28622505. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Frazer KA, Murray SS, Schork NJ, Topol EJ (April 2009). "Human genetic variation and its contribution to complex traits". Nature Reviews. Genetics. 10 (4): 241–51. doi:10.1038/nrg2554. PMID 19293820. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Li YI, van de Geijn B, Raj A, Knowles DA, Petti AA, Golan D, Gilad Y, Pritchard JK (April 2016). "RNA splicing is a primary link between genetic variation and disease". Science. 352 (6285): 600–4. doi:10.1126/science.aad9417. PMC 5182069. PMID 27126046. مؤرشف من الأصل في 31 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Callaway E (2017-06-15). "New concerns raised over value of genome-wide disease studies". Nature. 546 (7659): 463–463. doi:10.1038/nature.2017.22152. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Chakravarti A, Turner TN (June 2016). "Revealing rate-limiting steps in complex disease biology: The crucial importance of studying rare, extreme-phenotype families". BioEssays. 38 (6): 578–86. doi:10.1002/bies.201500203. PMID 27062178. مؤرشف من الأصل في 09 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Sekar A, Bialas AR, de Rivera H, Davis A, Hammond TR, Kamitaki N, Tooley K, Presumey J, Baum M, Van Doren V, Genovese G, Rose SA, Handsaker RE, Daly MJ, Carroll MC, Stevens B, McCarroll SA (February 2016). "Schizophrenia risk from complex variation of complement component 4" (PDF). Nature. 530 (7589): 177–83. doi:10.1038/nature16549. PMC 4752392. PMID 26814963. مؤرشف من الأصل (PDF) في 25 يوليو 2018. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Preininger M, Arafat D, Kim J, Nath AP, Idaghdour Y, Brigham KL, Gibson G (2013-03-14). "Blood-informative transcripts define nine common axes of peripheral blood gene expression". PLoS Genetics. 9 (3): e1003362. doi:10.1371/journal.pgen.1003362. PMC 3597511. PMID 23516379. الوسيط
|CitationClass=تم تجاهله (مساعدة) - He X (October 2017). "Comment on: An Expanded View of Complex Traits: From Polygenic to Omnigenic". Journal of Psychiatry and Brain Science. doi:10.20900/jpbs.20170014s2. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة تاريخ العلوم
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي
