سترات الكالسيوم
سترات الكالسيوم مركب كيميائي له الصيغة Ca3(C6H5O7)2 ، ويكون على شكل بلورات بيضاء، وهو ملح الكالسيوم لحمض الليمون (حمض الستريك).
| سترات الكالسيوم | |
|---|---|
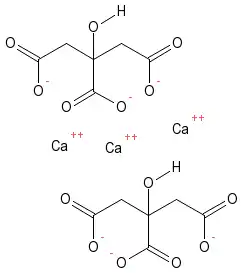 سترات الكالسيوم | |
| المعرفات | |
| رقم CAS | 813-94-5 5785-44-4 (رباعي هيدرات) |
| بوب كيم | 13136 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | Ca3(C6H5O7)2 |
| الكتلة المولية | 498.46 غ/مول |
| المظهر | بلورات بيضاء |
| الكثافة | 1.63 غ/سم3 |
| نقطة الانصهار | 120 °س |
| الذوبانية في الماء | 0.095 غ/100 مل ماء عند 25 °س |
| الذوبانية | غير منحل في الإيثانول |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- لمركب سترات الكالسيوم انحلالية ضعيفة في الماء، فقط 0.95 غ/ل عند 25°س. يختلف سترات الكالسيوم عن باقي أغلب الأملاح بأن انحلاليته تزداد بانخفاض درجة الحرارة (انحلالية عكسية). تزداد الانحلالية أيضاً بارتفاع pH الوسط. بالمقابل فإن لا ينحل في الكحول مثل الإيثانول.
- يبلغ محتوى الكالسيوم في هذا المركب 21% من الشكل الخالي من الماء، حيث أن سترات الكالسيوم يوجد أيضاً على شكل هيدرات (رباعي هيدرات)، ويبدأ بفقدان ماء التبلور عند التسخين فوق 120°س.
التحضير
يحضر سترات الكالسيوم (رباعي هيدرات) من تفاعل تعديل حمض الليمون (حمض الستريك) بهيدروكسيد الكالسيوم، وهو تفاعل ناشر للحرارة:
3Ca(OH)2 + 2C6H8O7 → Ca3(C6H5O7)2 + 6H2O
يحصل على سترات الكالسيوم طبيعياً كمركب وسيط أثناء عزل حمض الستريك من عمليات التخمير في عمليات تحضير حمض الستريك صناعياً.[2]
الاستخدامات
- يستعمل سترات الكالسيوم في الصناعات الغذائية كمضاف غذائي، حيث يستعمل كمادة حافظة. للمركب رقم الإي E 333.
- له تطبيقات في مجال إزالة قساوة المياه.
- يستخدم لتحضير أملاح السترات الأخرى، ويدخل في تركيب بعض المستحضرات الطبية المستخدمة لإغناء محتوى الكالسيوم، على سبيل المثال معاجين الأسنان.
المصادر
- موسوعة رومب الكيميائية Römpp Lexikon Chemie, Georg Thieme Verlag
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/13136 — تاريخ الاطلاع: 14 أكتوبر 2016 — العنوان : Acicontral — الرخصة: محتوى حر
- "Use of Lime in the Chemical Industry". National Lime Association. مؤرشف من الأصل في 21 فبراير 2009. اطلع عليه بتاريخ 25 نوفمبر 2006. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
