حمض الأسبارتيك
حمض الأسبارتيك (يختصر ب Asp أو D ) هو حمض ألفا-أميني قطبي ثنائي الكربوكسيل، وهو من الأحماض الأمينية غير الأساسية و رمزه الوراثي هو GAU و GAC·[2]
| حمض الأسبارتيك | |
|---|---|
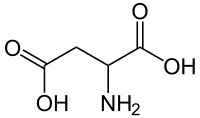 حمض الأسبارتيك | |
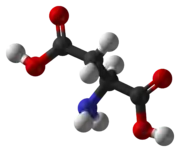 حمض الأسبارتيك | |
| الاسم النظامي (IUPAC) | |
Trivial: Aspartic acid | |
| المعرفات | |
| رقم CAS | 617-45-8 56-84-8 (L-isomer) 1783-96-6 (D-isomer) |
| بوب كيم (PubChem) | 424 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | C4H7NO4 |
| كتلة مولية | 133.1 غ.مول−1 |
| المظهر | colourless crystals |
| الكثافة | 1.7 g/cm3 |
| نقطة الانصهار | 270 °C |
| نقطة الغليان | 324 °C (decomposes) |
| الذوبانية في الماء | 4.5 g/L [1] |
| حموضة (pKa) | 3.9 |
| المخاطر | |
| فهرس المفوضية الأوروبية | not listed |
| NFPA 704 |
1
1
0
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الأسبارتات هو أنيون حمض الأسبارتيك·
عند الثدييات هو غير أساسي، يدخل في دورة اليوريا، يشارك في دورة تخليق الجلوكوز و يلعب دور في تركيب البيريميدين·هو ناقل عصبي محفز للمخ في شكله الميثيلي، حيث يفعل مستقبلات N-méthyl-D-aspartate) NMDA) التي هي مستقبلات للجلوتامات، لكن بحدة أقل من هذا الأخير·[3]
تاريخ
تم إكتشاف حمض الأسبارتيك بواسطة Plisson ،سنة 1827، وهو مشتق من الأسباراجين الذي تم إكتشافه سنة 1806 إنطلاقا من عصير الهليون·[4]
الأشكال و التسمية
هناك شكلين أو متقابلين ضوئين لحمض الأسبارتيك،إسم "حمض الأسبارتيك" يدل على كلى الشكلين أو على خليطهما الراسمي،[2]
فقط واحد من الشكلين يدخل في تركيب البروتينات وهو الشكل "L-aspartic acid"، الأدوار البيولوجية للشكل الأخر "D-aspartic acid" تبقى جد محدودة، تستطيع الأنزيمات المتخصصة إنتاج شكل واحد من الشكلين بينما التصنيع الكيميائي ينتج خليط راسمي·
مصادر حمض الأسبارتيك
المصادر الغذائية
حمض الأسبارتيك ليس من الأحماض الأمينية الأساسية، وهو ما يعني أنه يمكن gللجسم البشري تركيبه بواسطة عمليات الإستقلاب .
يتواجد حمض الأسبارتيك في:
- مصادر حيوانية:اللانشون، النقانق واللحوم
- مصادر نباتية : رقائق الشوفان ، الأفوكادو، الهليون ، وقصب السكر الفتي، ودبس السكر من الشمندر السكري.
- مكملات غذائية:حمض الأسبارتيك كمكمل غذائي أو على شكل ملح (مغنزيوم الأسبراتات)·
- المُحَلي الصناعي: أسبارتام
التصنيع الكيميائي
يمكن تصنيع خليط راسمي لحمض الأسبارتيك إنطلاقا من Diethyl Sodium Phthalimidomalonate ذو الصيغة الكيميائية (C6H4(CO)2NC(CO2Et)2·[5]
العيب الرئيسي للتقنية أعلاه هو إنتاجها لكميات متساوية المولية للمتقابلات الضوئية لحمض الأسبارتيك·
حاليا، وبفضل البيوتكنولوجيا، يمكن يمكن استخدام أنزيمات ثابتة من أجل إنتاج نوع واحد من المتقابلات الضوئية لحمض الأسبارتيك،يتم إنتاجه بواسطة أنزيم الأسبارتاز Aspartase [6] الخاص ببكتيريا إشريكية قولونية E.coli بالتفاعل مع فومارات الأمونيوم (Ammonium Fumarate)· في الأصل يقوم أنزيم الأسبارتاز بتفكيك حمض الأسبارتيك لكي تستخدمه البكتيريا كمصدر للأزوت لكن بإستعمال كميات كبيرة من فومارات الأمونيوم يؤدي هذا الأنزيم وظيفة عكسية تتجلى في تكوين حمض الأسبارتيك بكميات مهمة·
مراجع
- International Programme on Chemical Safety نسخة محفوظة 13 نوفمبر 2016 على موقع واي باك مشين.
- "Nomenclature and symbolism for amino acids and peptides (IUPAC-IUB Recommendations 1983)", Pure Appl. Chem. 56 (5), 1984: 595–624 http://iupac.org/publications/pac/56/5/0595/ نسخة محفوظة 14 يناير 2018 على موقع واي باك مشين.
- Chen, Philip E.; Geballe, Matthew T.; Stansfeld, Phillip J.; Johnston, Alexander R.; Yuan, Hongjie; Jacob, Amanda L.; Snyder, James P.; Traynelis, Stephen F.; Wyllie, David J. A. (2005). "Structural Features of the Glutamate Binding Site in Recombinant NR1/NR2A N-Methyl-D-aspartate Receptors Determined by Site-Directed Mutagenesis and Molecular Modeling". Mol. Pharmacol. 67 (5): 1470–84. doi:10.1124/mol.104.008185. PMID 15703381. مؤرشف من الأصل في 03 مايو 2009. الوسيط
|CitationClass=تم تجاهله (مساعدة) - R.H.A. Plimmer (1912) [1908]. R.H.A. Plimmer & F.G. Hopkins (المحرر). The chemical composition of the proteins. Part I. Analysis (الطبعة 2nd). London: Longmans, Green and Co. صفحة 112. مؤرشف من الأصل في 12 مارس 2020. اطلع عليه بتاريخ 18 يناير 2010. الوسيط
|CitationClass=تم تجاهله (مساعدة) - (1950)"DL-Aspartic Acid". Org. Synth.30: 7; Coll. Vol. 4: 55. .
- Aspartase Bioinformatics Resource Portal, ENZYME entry: EC 4.3.1.1 نسخة محفوظة 06 سبتمبر 2016 على موقع واي باك مشين.
- بوابة الكيمياء
- بوابة الكيمياء الحيوية
- بوابة صيدلة
- بوابة طب
- بوابة علم الأحياء

