بضع الكرة الشاحبة
بضع الكرة الشاحبة (بالإنجليزية: Pallidotomy) كان يستخدم لعقود لعلاج التصلب الحركي المصاحب لمرض باركنسون، الا أنه عند بدئ استخدام دواء ليفودوبا عام 1960 م، تم الحد من اجراء هذه العملية.[1] لكن على الرغم من التقدم الدوائي الملحوظ، الا أن من المرضى من يعاني من خلل الحركة (بالإنجليزية: Dyskinesia) المصاحب لاستعمال الأدوية أو أعراض حركية متقدمة مصاحبة لمرض باركنسون مما أدى إلى اعادة استخدام هذه العملية على نطاق أوسع.[2]
بضع الكرة الشاحبة يعزى بالوقت الحالي لكي الكرة الشاحبة الداخلية (بالانجليزية: Globus Pallidus internus GPi) حيث توجد كرة شاحبة داخلية وخارجية بكل نصف كرة مخية أو دماغية، الا أنه منذ عام 1987 م تحول الكي بشكل ملحوظ إلى التحفيز العميق للدماغ للكرة الشاحبة الداخلية (بالانجليزية: Deep Brain Stimulation (DBS) of GPi) عوضاً عن الكي كون التحفيز العميق لا يؤدي إلى تلف النسيج الداخلي المصاحب للكي، الا أن الكي لازال يستخدم في عدد من الحالات يتم تحديدها ودراستها من قبل أطباء جراحة الأعصاب. [3]
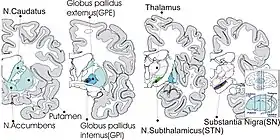
أغلب من يعاني من مرض باركنسون متقدم تظهرعليه الأعراض بكلا الجهتين من الجسم (اليمنى واليسرى) مصاحب لخلل في الاتزان وبطئ في الحركة، بالتالي لا يكفي اجراء عملية لجهة واحدة من نصف الكرة المخية مما يضطر أحياناً إلى تحفيز أو كي الكرة الشاحبة الداخلية للجهتين، الا أن كي الجهتين نادراً ما يتم اختياره كونه قد يؤدي إلى خلل في النطق أو الإدراك[4] لذلك يعد التحفيز أفضل من الكي عند القيام بعمليتين لكلا الجهتين من الدماغ، مع العلم أن الكي لكلا الجهتين قد يتم اختياره لبعض المرضى بفاصل زمني بين العمليتين 6 شهور أو أقل أو أكثر للتخفيف من الأعراض الجانبية التي قد تحدث عند اجراء العمليتين بنفس الوقت.[5]
دواعي العملية الجراحية
ان اختيار المريض المناسب يعتمد على توافق البيانات المستمدة من التاريخ المرضي والفحص السريري الدقيق والصور الطبية:
- أعراض حركية متقدمة مصاحبة لمرض باركنسون.
- خلل الحركة (بالإنجليزية: Dyskinesia) المصاحب لاستعمال أدوية مرض باركنسون.
- خلل التوتر أو ديستونيا (بالإنجليزية: Dystonia) لا يستجيب للعلاج الدوائي. قد يتم اجراء الكي لبعض المرضى لكلا الجهتين من الدماغ.
- الجهة الأخرى المقابلة من التحفيز العميق للدماغ. حيث يمكن اجراء تحفيزعميق للدماغ لكرة شاحبة داخلية وكي للكرة المقابلة عند الحاجة للدواعي المرضية السابقة.
- عند حدوث مضاعفات من التحفيز العميق للدماغ كالتهاب بكتيري حاد أو مزمن أدى إلى ازالته، عند هذه الحالة يتم اجراء الكي كبديل علاجي جراحي.
الحالات التي تمنع اجراء العملية الجراحية
- الحالات الطبية غير المستقرة التي تمنع المريض أن يكون مستيقظاً عند الاجراء الجراحي. وذلك لأن الاجراء يحتاج إلى تقييم عصبي سريري مستمر طوال العملية. (في حالات نادرة جداً يتم استخدام التخدير العام).
- الاضطرابات النفسية عند المريض: كاكتئاب نفسي متقدم غير معالج أو أعراض ذهانية (الا أن تكون الأعراض الذهانية ناتجة عن العلاج الدوائي كالدوبامين) أو خرف.
- ضمور نظم متعددة بمرضى الباركنسونية.
- حالات مرض باركنسون التي لا تستجيب لعلاج ليفودوبا (بالإنجليزية: Levodopa) من الأساس.
- المرضى الذين لديهم قابلية للنزف: كاعتلال تخثر الدم، أو مريض يأخذ مميعات الدم بانتظام.
العملية الجراحية
يتم وضع وتثبيت اطار التوضيع التجسيمي (بالانجليزية: stereotactic frame) على رأس المريض تحت التخدير الموضعي، وقد يستخدم المنوم أو المخدر العام للتركيب إذا كانت ارتعاشات المريض شديدة تمنع من القدرة على تركيب الإطار. يتم تصوير رأس المريض بالرنين المغناطيسي لتكوين صورة مجسمة ثلاثية الأبعاد لتحديد موقع الهدف (الكرة الشاحبة الداخلية)، في حال وجود مانع لاستخدام الرنين المغناطيسي يتم اجراء صورة مقطعية للرأس.
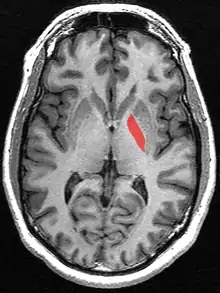
يتم اجراء حسابات رياضية اعتماداً على نقاط معينة يتم تحديدها داخل الدماغ، حيث أن هذه النقاط يتم اعطاؤها موقع احداثي رياضي باتخاذ الإطار المحيط بالرأس كمرجع. يتم تحديد الجهة الخلفية البطنية من الكرة الشاحبة الداخلية بشكل غير مباشر (بالانجليزية: posteroventral GPi) كالتالي:
- تحديد موقع المقرن أمامي (بالانجليزية: anterior commissure) وتحديد موقع المقرن الخلفي (بالانجليزية: posterior commissure)
- حساب وتحديد نصف المسافة بينهما. عند نصف المسافة يحسب 2 مليمتر باتجاه المقرن الأمامي، 20 مليمتر للجانب المراد، 4 مليمتر للأسفل.
- أحياناً يتم تعديل الموقع النهائي بشكل طفيف اعتماداً على التحديد التشريحي المباشر للكرة الشاحبة الداخلية عند معاينة صور الرنين المغناطيسي.
عند الانتهاء من الحسابات الرياضية يتم تجهيز المريض بحيث يكون نائماً على ظهره منحن للأمام 45 درجة تقريباً لاجراء العملية الجراحية، وبعد التعقيم المناسب يتم تركيب قوس للإطار المحيط بالرأس حيث أن هذا القوس يحمل الإبرة مزودة بقطب كهربائي للوصول للنقطة المرادة.

عند تجهيز المريض يتم عمل جرح صغير (3-5 سم) تحت التخدير الموضعي على الجهة المرادة من الرأس قبل الدرز الإكليلي باتجاه الجبهة فوق خط تخيلي يمتد من منتصف محجر العين للخلف. ثم تثقب الجمجمة ثم الأم الجافية حيث يتم ادخال الإبرة.
عند وصول الإبرة للنقطة المرادة يتم إرسال ترددات راديوية للتأكد من موقع الإبرة وأنها ليست بمكان خاطئ كالسبيل البصري، حيث يتم سؤال المريض وفحصه خلال هذه الترددات.
عند التأكد من وجود الإبرة بالمكان الصحيح يتم كي الجهة الخلفية البطنية من الكرة الشاحبة الداخلية بابرة قطرها 1.1 مليمتر وطرف عار 3 مليمتر. يتم عمل كي مؤقت بدرجة حرارة 42 درجة مئوية، وإذا لم يكن هنالك أي مضاعفات جانبية يتم الكي بشكل دائم بدرجة حرارة بين 75 إلى 80 درجة مئوية لمدة 60 ثانية. يتم سحب الإبرة للأعلى 2الى3 مليميتر مع كي لمدة 60 ثانية. في بعض الأحيان يتم تحريك الإبرة للكي أيضاً إلى الامام 2 مليمتر وأيضاً باتجاه منتصف الرأس 2 مليميتر، وهذا يعتمد على حجم الكرة الشاحبة الداخلية. عند الانتهاء يتم سحب الإبرة بعد أن تبرد لدرجة حرارة 42 درجة مئوية أو أقل، ومن ثم خياطة جرح جلدة الرأس.
مراجع
- Alfredo Quiñones-Hinojosa, MD (2012). Schmidek and Sweet: Operative Neurosurgical Techniques (باللغة الانجليزية) (الطبعة 6). Saunders, an imprint of Elsevier Inc. صفحة 1315. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: لغة غير مدعومة (link) - Laitinen LV, Bergenheim AT, Hariz MI (1992), Leksell’s posteroventral pallidotomy in the treatment of Parkinson’s disease, J Neurosurg. 1992;76:53-61 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) CS1 maint: ref=harv (link) - Limousin P, Pollack P, Benazzouz A (1995), Bilateral Subthalamic Nucleus Stimulation for Severe Parkinson's Disease, Mov Disord. 1995; 10:672–674 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) CS1 maint: ref=harv (link) - Favre J, Burchiel KJ, Taha JM (2000), Bilateral Outcome of unilateral and bilateral pallidotomy for the treatment of Parkinson’s disease: patient assessment., Neurosurgery. 2000;46:344-353 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) CS1 maint: ref=harv (link) - Siegfried J, Lippitz B. (1994), Bilateral chronic electrostimulation of ventroposterolateral pallidum: a new therapeutic approach for alleviating all parkinsonian symptoms., Neurosurgery. 1994;35:1126-1129 الوسيط
|CitationClass=تم تجاهله (مساعدة); الوسيط|separator=تم تجاهله (مساعدة); line feed character في|title=على وضع 114 (مساعدة)CS1 maint: ref=harv (link) - Rahul Jandial, Paul McCormick, Peter Black (April 25, 2011). Core Techniques in Operative Neurosurgery (باللغة الانجليزية) (الطبعة 1). Saunders. صفحة 290. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) صيانة CS1: لغة غير مدعومة (link)
- بوابة طب
 صور وملفات صوتية من كومنز
صور وملفات صوتية من كومنز