نظام أصهري
النظام الأصهري[1] أو النظام سهل الانصهار[2] أو نظام يوتكتي[3] (وذلك من eutectic والمشتقة من اللفظ الإغريقي "ευ" (يو) بمعنى سهل، ومن Τήξις (تكسيس) بمعنى انصهار) . هو حالة من حالات التوازن الطوري لنظام مكون من عنصرين (على الأقل) في سبيكة متجانسة.

رسم بياني للأطوار
الرسم البياني يبين الآتي: إلى اليمين العنصر B بنسبة 100% (بالتالي تكون نسبة العنصر A مساوية 0 % )؛ ويمثل المحور إلى اليسار وجود العنصر A بنسبة 100% (وعدم وجود العنصر B). ويبين الشكل أن العنصر B النقي ينصهر عند درجة حرارة عالية عند L+B ؛ واما العنصر النقي A فله درجة انصهار عالية أخرى عند L+ A . إذا بدأنا بالعنصر B وأضفنا إليه 10% مثلا من العنصر A (يصبح B في المخلوط بنسبة 90%) نجد أن نقطة انصهار المخلوط تقل تبعا للخط العلوي L+B . (الخط العلوي L+B هو الحد الفاصل بين السائل (أعلى) والصلب (أسفل)). وإذا أزدنا نسبة A في المخلوط ليصبح 20% A إلى 80 % B نجد أن نقطة الانصهار تنخفض تبعا للخط العلوي L+B ، ولا نزال نغير نسبة المادتين حتى يصل المخلوط إلى أقل درجة حرارة ينصهر فيها وهي النقطة L ، وهي تسمى نقطة اليوتيكي . وليس بالضرورة أن تكون نقطة اليوتيكي عند 50% A و50% B للمخلوط، فعادة تكون نقطة اليوتيكي L منزاحة نحو اليمين أو اليسار بحسب خواص مواد المخلوط.
بالمثل إذا بدأنا من أقصى اليسار حيث يكون العنصر A نقيا. فعدما نخلطه بالعنصر B بنسب مختلفة نجد أن درجة انصهاره تنخفض حتى النقطة L .
عند نقطة اليوتيكي يسمى المخلوط المزيج الأصهري أو التركيب الأصهري، والذي يتميز بأن له أخفض نقطة انصهار بالمقارنة مع النسب الأخرى للمخلوط. وتدعى درجة الحرارة تلك بالنقطة الأصهرية.
يكون للمزيج الأصهري (أو المزيج اليوتيكي) بنية بلورية خاصة تدعى باسم الشبكة الفائقة superlattice ؛ ويكون فيها ترتيب الذرات منتظما ليس على المستوى القريب فقط وإنما على المستوى البعيد أيضا في المادة (أي يشمل مئات أو آلاف الذرات). عندئذ ينصهر المزيج ككل عند النقطة الأصهرية، ويسيل النظام البلوري للذرات في نفس الوقت ويتحول إلى مزيج سائل (الصهارة). بالتالي، فإن النقطة الأصهرية هي أخفض درجة انصهار ممكنة من مزيج عناصر، وهي تحدث عند المزيج اليوتيكي.
عادةً ما يمثل النظام الأصهري في مخطط أطوار كما هو مبين في الشكل أعلاه. تعرّف النقطة الأصهرية (نقطة اليوتيكي) على أنها النقطة التي توافق درجة الحرارة الأصهرية ونسبة المزيج الأصهري.
تفاصيل أخرى في أطوار مزيج
طبقا للرسم البياني نجد ان العنصر B يتبلور مثلا في نظام بلوري مكعب (β) ، في حين أن العنصر A يتبلور في نظام بلوري آخر (نظام بلوري سداسي مثلا α) . نجد أن النظام البلوري المكعب β يغلب في وجود نسب قليلة من A . وهذا ما يشير إليه الرسم البياني إلى اليمين حيث يوجد خط فاصل بين المتبلور β والمتبلور L+ β . أما أسفل نقطة اليوتيكي فنجد أيضا حدا فاصلا بين الطور β والطور α + β . في الوسط يغلب نظام التبلور α + β (انظر الشكل).
بالمثل نجد أن النظام البلوري السداسي α يغلب إلى اليسار حيث نسبة العنصر A في المزيج كبيرة.
كل مزيج من تلك الخلطات يسمى طورا للمادة، وكل طور يتميز بخواص بلورية مختلفة وبالتالي بخواص فيزيائية وكيميائية مختلفة، وهي جميعها تعتمد على نوعي العنصرين المشكلين للمزيج وكذلك على درجة حرارة المزيج. تلك الخصائص نستعين بها في تحضير الفولاذ وتحضير الأنواع المختلفة من الحديد (انظر أسفله ومخطط الحديد والكربون) .
التفاعل اليوتيكي
يعرّف التفاعل اليوتيكي كما يلي:
هذا التفاعل يبين حالة توازن بين الطور السائل والمحلول الصلب α والمحلول الصلب β . حالة التوازن هذه تشبه حالة انصهار الحديد حيث تظل درجة الحرارة "ثابتة" حتى يتحول كل الحديد إلى الطور السائل. من الوجهة الترموديناميكة يتصف هذا التوازن بأن الطاقة الحرة للنظام تكون مساوية للصفر. وهذا يعني أن السائل واثنين من المحاليل الصلبة α وβ تتواجد في الوقت نفسه، ويكونوا في حالة توازن كيميائي. أي معدل تغير المواد من اليمين إلى اليسار في التفاعل تكون مساويا لمعدل تحول السائل من اليسار إلى اليمين.
بعد تبريد النظام يتخذ المزيج بنية من التفاعل اليوتيكي تعتمد على عدة عوامل. أهم تلك العوامل هو كيفية تبلور السائلين الجامدين ونمو بلوراتهما. عمليا تنتج في الأغلب بنية رقائقية، ولكن بنيات أخرى محتملة تشمل البنية الكروية أو القضيبية أو الإبرية. [4] باختلاف تلك البنيات الداخلية للسبيكة الناتجة تختلف خواصها الفيزيائية، كالصلابة والمرونة والهشاشة ومقاومة الصدأ وغيرها.
الأنواع
سبائك
سبائك سهلة الانصهار ولديهم اثنين أو أكثر من المواد، ويكون لها تركيب سهل الانصهار وبها خليط غير سهل الانصهار (غير أصهري) يتصلب، ومكوناته يتصلب عند درجات حرارة مختلفة، وإظهار مدى ذوبان البلاستيك. خليط سهل الانصهار يتصلب في درجة حرارة واحدة حادة. وعلى العكس، عندما تمتزج جيدا، وسبائك سهلة الانصهار يذوب وهو يفعل ذلك في درجة حرارة ثابتة. ويمكن فهم التحولات التي تحدث أثناء مرحلة ترسيخ خليط تعطى عن طريق رسم خط عمودي من المرحلة السائلة إلى المرحلة الصلبة في مرحلة الرسم. بعض الاستخدامات تشمل ما يلي:
- سبائك لحام أصهرية، ويتكون من القصدير (SN)، الرصاص (Pb) والفضة في بعض الأحيان (حج) أو الذهب (Au).
- صب السبائك، مثل الألومنيوم والسليكون والحديد الزهر (في تكوين لسهل الانصهار الأوستينيت-cementite في نظام الحديد والكربون).
- أسلوب واحد التي يستخدمها في صناعة أشباه الموصلات على رقائق السيليكون السندات لمطلية بالذهب ركائز هي للحث على سهل الانصهار السيليكون الذهب من خلال تطبيق الطاقة بالموجات فوق الصوتية إلى الرقاقة. انظر الرابطة سهلة الانصهار.
- مختلط، حيث نشر يمكن إزالة عناصر من صناعة السبائك المشتركة، بحيث انصهار سهل الانصهار غير ممكن إلا في مرحلة مبكرة من عملية مختلط.
- استجابة درجة الحرارة، والمعادن مثل الخشب والمعدن الميدانية لرشاشات الحريق.
- بدائل الزئبق غير السامة، مثل Galinstan
- زجاجي المعادن التجريبية، مع قوة عالية للغاية والمقاومة للتآكل.
- 8. سهل الانصهار سبائك من الصوديوم والبوتاسيوم (سائل التبريد NaK) التي تكون سائلة في درجة حرارة الغرفة وتستخدم في تبريد مفاعلات الأبحاث لخفض سرعة النيوترونات السريعة.
أخرى
كلوريد الصوديوم والماء تشكل مزيجا سهل الانصهار. لديه نقطة سهلة الانصهار -21.2 C [5] و 23.3٪ حسب الكتلة. يستغل طبيعة سهلة الانصهار من الملح والماء عندما يتم نشر الملح على الطرق للمساعدة على ازالة الثلوج، أومختلطة مع الجليد لإنتاج درجات حرارة منخفضة (على سبيل المثال، في صنع الآيس كريم التقليدية). 60٪ و 40٪ NaNO3 KNO3 يشكل خليط سهل الانصهار والتي تستخدم في تكنولوجيا الطاقة الشمسية ملح مصهور. لتقليل درجة انصهار سهل الانصهار في الأملاح المنصهرة الشمسية يتم استخدام نترات الكالسيوم في هذه النسبة، في كاليفورنيا 42٪ (NO3) 2 ، 43٪ و 15٪ KNO3 NaNO ليدوكائين وبريلوكائين، على حد سواء المواد الصلبة في درجة حرارة الغرفة، تشكيل سهل الانصهار الذي هو النفط مع 16 درجة مئوية (61 درجة فهرنهايت) درجة انصهار، وتستخدم في خليط سهل الانصهار من التحضيرات المحلية (EMLA)مخدر. المعادن قد أخلاطا سهل الانصهار في الصخور النارية. بعض الأحبار هي مزيج سهل الانصهار، مما يسمح للطابعات النافثة للحبر على العمل في درجات حرارة منخفضة.
النقاط الحرجة الأخرى
Eutectoid
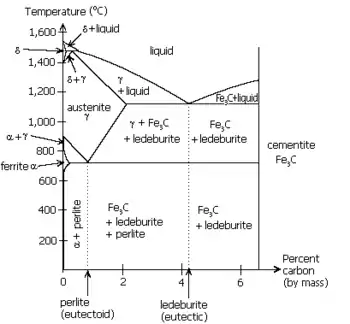
الحديد والكربون مرحلة الرسم، والتي تبين تحول eutectoid بين الأوستينيت (γ) والبرليت. عندما حل فوق نقطة تحول صلبة، بدلا من السائل، يمكن أن تحول eutectoid مماثل يحدث. على سبيل المثال، في نظامالحديد والكربون، ويمكن للمرحلة الأوستينيت يخضع لعملية تحول eutectoid لإنتاج الفريت وcementite، في كثير من الأحيان في هياكل رقائقية مثل البرليت وbainite. هذه نقطة eutectoid يحدث في 723 درجة مئوية (1333 درجة فهرنهايت) والكربون حوالي 0.83٪.
Peritectic
التحولات Peritectic هي أيضا مشابهة لردود الفعل سهل الانصهار. هنا، في مرحلة السائلة والصلبة ذات أبعاد ثابتة تتفاعل عند درجة حرارة ثابتة لتسفر عن مرحلة واحدة صلبة. منذ أشكال المنتج صلبة في مجال التفاعل بين المواد المتفاعلة 2، ويمكن أن تشكل حاجزا نشر ويسبب عموما ردود الفعل هذه على المضي قدما ببطء أكثر بكثير من التحولات سهل الانصهار أو eutectoid. لهذا السبب، عندما تكوين peritectic يتصلب فإنه لا تظهر بنية رقائقية التي يتم العثور عليها مع التصلب سهل الانصهار. مثل هذا التحول موجود في نظام الحديد والكربون، وكما رأينا بالقرب من الزاوية اليسرى العليا من هذا الرقم. انه يشبه سهل الانصهار مقلوب، مع المرحلة δ مع الجمع بين السائل لإنتاج نقي الأوستينيت في 1495 درجة مئوية (2723 درجة فهرنهايت) والكربون 0.17٪. Peritectic التحلل. وقد تم تناول ما يصل إلى هذه النقطة في مناقشة التحولات من وجهة نظر من التبريد. أنها يمكن أيضا أن تناقش مشيرا إلى أن التغيرات التي تحدث لبعض المركبات الكيميائية الصلبة ويتم تسخينها هم. بدلا من الذوبان، فيدرجة حرارة التحلل peritectic، مجمع تتحلل إلى مركب آخر الصلبة والسائلة أ. يتم تحديد نسبة كل من حكم رافعة.المفردات يغير قليلا. تماما كما يطلق عليه في تبريد المياه، الأمر الذي يؤدي إلى جليد وتجميد وارتفاع حرارة الجليد يؤدي إلى ذوبان. في مرحلة الرسم شركة الاتحاد الأفريقي، على سبيل المثال، يمكن أن ينظر إلى أن اثنين فقط من المراحل تذوب بشكل متطابق، AuAl2 وAu2Al. بقية تتحلل peritectically
انظر أيضاً
مراجع
- ترجمة Eutectic في قاموس المورد، البعلبكي، بيروت، لبنان.، الكلمة مشتقة على وزن اسم التفضيل من الفعل صَهَرَ، على وزن أصهر، بمعنى الأكثر قابلية للانصهار.
- ترجمة Eutectic في المعجم الطبي الموحد
- ترجمة Eutectic في قاموس المورد، البعلبكي، بيروت، لبنان.
- Smith & Hashemi 2006، صفحات 332–333.
- بوابة كيمياء فيزيائية
- بوابة تعدين
- بوابة الكيمياء
- بوابة الفيزياء
