ليمونين
الليمونين سائل هيدروكربوني صافٍ وشفا، ويصنّف ضمن التربينات الأحادية الحلقية، وهو المكوّن الأساس في زيت قشور الحمضيات.[1] المتماكب-D هو المتماكب الأكثر شيوعًا في الطبيعة ويستخدم عطر البرتقال كمادة منكهة في صناعة الأغذية.[1][2] ويستخدم الليمونين كذلك في التخليق الكيميائي كمادة بادئة لصناعة الكارفون وكمذيب في منتجات التنظيف.[1] أما المتماكب-L وهو المتماكب الأقل شيوعًا، فينتشر في زيت النعناع وله رائحة شبيهة برائحة الصنوبر أو التربنتين.[1]
| ليمونين | |
|---|---|
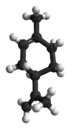 ليمونين |
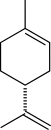 ليمونين |
 ليمونين | |
| الاسم النظامي (IUPAC) | |
1-Methyl-4-(1-methylethenyl)-cyclohexene | |
| المعرفات | |
| رقم CAS | 138-86-3 (R/S) 5989-27-5 (R) 5989-54-8 (S) |
| بوب كيم (PubChem) | 22311 439250 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | C10H16 |
| كتلة مولية | 136.23 غ.مول−1 |
| المظهر | colorless to pale-yellow liquid |
| الرائحة | برتقال |
| الكثافة | 0.8411 g/cm3 |
| نقطة الانصهار | -74.35 °س، 199 °ك، -102 °ف |
| نقطة الغليان | 176 °س، 449 °ك، 349 °ف |
| الذوبانية في الماء | insoluble |
| الذوبانية | miscible in كحول, بنزين (مركب كيميائي), كلوروفورم, إيثر, ثنائي كبريتيد الكربون, and oils soluble in رباعي كلوريد الكربون |
دوران محدد ([α]D) |
87° - 102° |
| معامل الانكسار (nD) | 1.4727 |
| كيمياء حرارية | |
| تغير الإنتالبي القياسي للاحتراق ΔcH |
−6.128 MJ mol−1 |
| المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| NFPA 704 |
2
1
0
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التفاعلات الكيميائية
يعدّ الليمونين تربينًا مستقراً نسبياً ويمكن تقطيره دون أن يتفكك، ولكنّه قد يتكسّر في درجات الحرارة المرتفعة ليتحول إلى الآيزوبرين.[3] يتأكسد الليمونين بسهولة في الهواء الرطب منتجًا الكارفيول والكارفون وأكسيد الليمونين.[4] وبوجود الكبريت، يفقد الليمونين الهيدروجين ليتحول إلى باراسيامين.[5]
التأثير على الصحة
قد يؤدي دهن الجلد بالليمونين إلى حدوث تهيّج، ولكنّه يبدو آمنًا للاستخدامات البشرية. [6] الليمونين مادة قابلة للاشتعال عندما يكون سائلًا أو بخارًا، ويعد مادة سامة للحياة المائية.[1]
مراجع
- D-limonene. PubChem Compound Database; CID=440917, National Center for Biotechnology Information, US National Library of Medicine. 2017. Retrieved 22 December 2017. نسخة محفوظة 13 أبريل 2018 على موقع واي باك مشين.
- Fahlbusch, Karl-Georg; Hammerschmidt, Franz-Josef; Panten, Johannes; Pickenhagen, Wilhelm; Schatkowski, Dietmar; Bauer, Kurt; Garbe, Dorothea; Surburg, Horst (2003). "Flavors and Fragrances". Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1111/j.1600-0536.1992.tb00129.x. PMID 1395597. نسخة محفوظة 06 مارس 2016 على موقع واي باك مشين.
- Pakdel, Hooshang; Pantea, Dana Magdalena; Roy, Christian (2001-01). "Production of dl-limonene by vacuum pyrolysis of used tires". Journal of Analytical and Applied Pyrolysis. 57 (1): 91–107. doi:10.1016/s0165-2370(00)00136-4. ISSN 0165-2370. مؤرشف من الأصل في 14 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Karlberg, Ann-Therése; Magnusson, Kerstin; Nilsson, Ulrika (1992-05). "Air oxidation ofd-limonene (the citrus solvent) creates potent allergens". Contact Dermatitis (باللغة الإنجليزية). 26 (5): 332–340. doi:10.1111/j.1600-0536.1992.tb00129.x. ISSN 0105-1873. مؤرشف من الأصل في 14 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Weitkamp, A. W. (1959-07). "I. The Action of Sulfur on Terpenes. The Limonene Sulfides". Journal of the American Chemical Society (باللغة الإنجليزية). 81 (13): 3430–3434. doi:10.1021/ja01522a069. ISSN 0002-7863. مؤرشف من الأصل في 14 ديسمبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة); تحقق من التاريخ في:|تاريخ=(مساعدة) - Kim, Young Woo; Kim, Min Ji; Chung, Bu Young; Bang, Du Yeon; Lim, Seong Kwang; Choi, Seul Min; Lim, Duck Soo; Cho, Myung Chan; Yoon, Kyungsil (2013). "Safety evaluation and risk assessment of d-Limonene". Journal of Toxicology and Environmental Health. Part B, Critical Reviews. 16 (1): 17–38. doi:10.1080/10937404.2013.769418. ISSN 1521-6950. PMID 23573938. مؤرشف من الأصل في 31 أكتوبر 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة)

