خلية كهربائية
الخلية الكهربائية هي أحد مصادر التيار الكهربائي الذي ينتج من تفاعل كيميائي تتحول فيه الطاقة الكيميائية إلى طاقة كهربائية. تتكون الخلية من قطبين من مادتين مختلفتين ومادة ثالثة تفصل بينهما وتسمي كهرل . أبسط أنواعها يتكون من وعاء زجاجي يحوي محلولاً مخففاً من حمض الكبريتيك وهو يمثل الكهرل ينغمس فيه قطبان من النحاس والزنك. إذا اتصل القطبان من الخارج بسلك معدني، يسري تيار كهربائي بينهما نتيجة تفاعل الحمض مع الزنك ، فتتجمع على لوح الزنك إلكترونات وتسري خارجه إلى قطب النحاس. (هذا عكس اتجاه التيار الكهربائي الذي اصطـُلح على سريانه من قطب النحاس الموجب إلى قطب الزنك السالب). تنتج هذه الخلية جهدا كهربائيا مقداره نحو 5و1 فولت ويمكن زيادة الجهد عن طريق توصيل عدة من تلك الخلايا . فإذا وصلنا ثلاثة منها أنتجت لنا قوة دافعة كهربائية مقداره 5و4 فولت.
- هناك عدة أنواع من هذه الخلايا الكهربائية تختلف نوع قطبيها ونوع المادة الكيميائية كهرل بينهما، تتوقف القوة الدافعة الكهربائية (أو ما يسمى بفرق الجهد بين القطبين عندما توصل الخلية من الخارج بمقاومة كبيرة) على مقدار نشاط مادتي القطبين الكيميائية. من امثلة الخلايا الكهربائية: خلية دانيال ، وخلية لكلانشيه.
- تتكون البطارية الجافة من وعاء صغير من الزنك (القطب السالب) بداخلها قضيب من الكربون (القطب الموجب)، بينهما عجينة من الكربون وثاني أكسيد المنجنيز مشبعة بمحلول كلوريد الأمونيوم .
- وتوجد بطارية الرصاص وهي بطارية السيارة يمكن إعادة شحنها عندما تفرغ بتمرير تيار كهربائي فيها وإعادتها إلى حالتها الأصلية ، وبذلك يمكن شحنها بعد تفريغها وتسمى المجموعة من تلك الخلايا "بالمركم". وتعمل البطارية الرصاصية بلوحين أحدهما رصاص واللوح الآخر أكسيد الرصاص . وعند غمسهما في محلول حامض الكبريتيك ككهرل ينتج فرق جهد قوة دافعة كهربية تعمل على مرور تيار عند توصيل اللوحين من الخارج بسلك موصل.
- في أي خلية كهربية تنشا بين اللوحين قوة دافعة كهربائية مميزة بحسب نوع اللوحين والكهرل . فإذا وصلنا اللوحين بسلك أو لمبة مثلا تنخفض القوة الدافعة الكهربية إلى ما نسميه فرق الجهد بين اللوحين وذلك بسبب الاستهلاك ومرور التيار. والقوة الدافعة الكهربية هي فارق الجهد عندما تكون المقاومة الخارجية كبيرة أو لا نهائية .
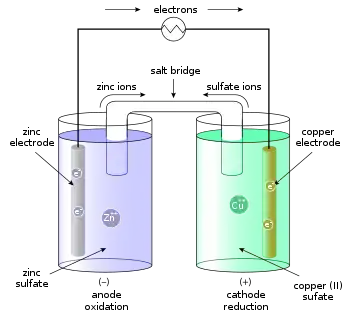
الخلية الجلفانية (خلية دانيال) ويلاحظ تجمع أكثر للإلكترونات على لوح الخارصين Zn عن لوح النحاس Cu
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
