تسمم بالأكسجين
التسمم بالأكسجين هو حالة مرضيّة ناجمة عن الآثار الضارة لتنفس الأكسجين الجزيئى (O2) في مستويات ضغوط جزئية مرتفعة. وتُعرف هذه الحالة أيضًا باسم متلازمة سمية الأكسجين، والتسميم عن طريق الأكسجين. تاريخيًا، سُميت إصابة الجهاز العصبى المركزى بهذه الحالة المرضية تأثير باول بيرت، وسُميت إصابة الرئة بتأثير لورين سميث، وذلك نسبةً للباحثين الروّاد الذين اكتشفوها ووصفوها في أواخر القرن التاسع عشر. ويُمكن أن تؤدي الإصابات الجسيمية بهذا المرض إلى حدوث تلف في الخلايا أو الموت، وتظهر آثار المرض في معظم الأحيان على الجهاز العصبى المركزى والرئتين والعينين. وتعد سمية الأكسجين مصدر قلق للغواصين تحت الماء، وهؤلاء الذين يتعرضون لتركيزات عالية من الأكسجين الأضافى وخاصة الأطفال الخدج وهؤلاء الذين يخضعون لمُعالَجَةٌ بالأُكسجين العالِي الضَّغْط.
| سمية الأكسجين | |
|---|---|
 في عام 1942 و1943 أخضعت حكومة المملكة المتحدة الغواصين لاختبارات مكثفة بشأن سمية الأكسجين، وفيها وصل ضغط الهواء في حجرة الاختبارات إلى 3.7 بار وتنفس الخاضع للاختبار الموجود في وسط الصورة أكسجين نقي بنسبة 100% عن طريق قناع.[1] في عام 1942 و1943 أخضعت حكومة المملكة المتحدة الغواصين لاختبارات مكثفة بشأن سمية الأكسجين، وفيها وصل ضغط الهواء في حجرة الاختبارات إلى 3.7 بار وتنفس الخاضع للاختبار الموجود في وسط الصورة أكسجين نقي بنسبة 100% عن طريق قناع.[1] | |
| معلومات عامة | |
| الاختصاص | طب الطوارئ |
| من أنواع | تسمم |
| التاريخ | |
| سُمي باسم | بول بيرت |
وينتج عن التنفس في مستويات ضغوط جزئية مرتفعة من الأكسجين فرط التأكسج؛ وهو وجود فائض من الأكسجين في أنسجة الدم. يتأثر الجسم بطرق مختلفة ويعتمد ذلك على نوع التعرض؛ فينجم تسمم الجهاز العصبى المركزى عن التعرض قصير الأجل لمستويات ضغوط جزئية من الأكسجين أعلى مما هي عليه في الضغط الجوي، وينتج تسمم الرئة والعين من التعرض طويل الأجل لمستويات مرتفعة من الأكسجين في الضغط العادى. ومن الممكن أن تشمل الأعراض كل من الارتباك ومشاكل في التنفس وتغيرات في الرؤية مثل قصر النظر. ومن الممكن أن يؤدى التعرض المطول لمستويات الضغوط الجزئية من الأكسجين التي تكون فوق معدلاتها الطبيعية أو التعرض لفترة قصيرة للضغوط الجزئية العالية للغاية إلى ضرر تأكسدي لأغشية الخلايا وتهدم الحويصلات الهوائية في الرئتين وانفصال الشبكية والإصابة بالنوبات. وتواجه سمية الأكسجين عن طريق الحد من التعرض لمستويات الأكسجين المرتفعة. وتشير الدراسات أنه، وعلى المدى الطويل، من الممكن التعافي من التسمم بالأكسجين بشكل كامل.
توجد بروتوكولات لتجنب فرط التأكسج في المجالات التي يُتنفس فيها الأكسجين في مستويات ضغط جزئية أعلى من المعدلات الطبيعية، بما في ذلك الغوص تحت الماء باستخدام غازات التنفس المضغوطة، والتطبيب بالضغط العالى، وورعاية الأطفال الحديثي الولادة، ورحلات الفضاء البشرية. وأدت هذه البروتوكولات إلى ارتفاع ندرة النوبات الناتجة عن التسمم بالأكسجين واقتصار الأضرار التي تلحق بالرئة والعين بشكل رئيسى على مشاكل إدارة الأطفال الخدج.
في السنوات الأخيرة، أصبح الأكسجين متاحًا للاستخدام الترفيهي في حانات الأكسجين. وحذرت إدارة الغذاء والدواء الأمريكية أولئك الذين يعانون من مشاكل مثل أمراض القلب أو الرئة من استخدام الأكسجين الذي يُباع في حانات الأكسجين. يستخدم غواصوا السكوباغازات للتنفس تحتوى على مايصل إلى 100% أكسجين، وينبغي أن يخضعوا لتدريبات خاصة لاستخدام هذه الغازات.
التصنيف
ويمكن تصنيف آثار سمية الأكسجين من قبل الأجهزة المتضررة، منتجة ثلاثة أشكال رئيسية:[2][3][4]
الجهاز العصبي المركزي، والذي يصاب بتشنجات تليها فقدان للوعى، وهذا يحدث عند التعرض للضغط المفرط. الجهاز الرئوي (الرئتين)، وما يحدث من صعوبة في التنفس وألم في الصدر، وذلك يحدث عند التنفس لفترات طويلة في ضغوط مرتفعة من الأكسجين؛ الجهاز البصري (شروط ريتينوباثيك)، والتغييرات التي تخضع لها العيون، والتي تحدث عند التنفس لفترات طويلة في ضغوط مرتفعة من الأكسجين. سمية الأكسجين تضر الجهاز العصبى المركزى، وبالتالى ممن الممكن الإصابة بنوبات، وفترات قليلة من الصمل، تلهيا تشنجات وفقدان الوعى، وذلك يعد مصدر قلق للغواصين الذين يتعرضون لضغط أكبر من ضغط الغلاف الجوى. ينتج أضرار عديدة بسبب الإصابة بسمية الأكسجين للجهاز الرئوى حيث تصاب الرئتين بأضرار جسيمة، مما يسبب الألم وصعوبة في التنفس. وقد يؤدى الضرر التأكسدى على العين إلى قصر النظر أو انفصال جزئى لشبكية العين.ويعد الضرر الذي يصيب الجهاز الرئوى والعين هم الأكثر احتمالا في الحدوث وذلك عندما يتم اعطاء أكسجين اضافى كجزء من العلاج، وخاصة للأطفال الرضع حديثى الولادة، ويمثل أيضا مصدر قلق عند العلاج بالتعرض للأكسجين العالى الضغط.
قد يحدث الضرر التأكسدي في أي خلية من خلايا الجسم ولكن آثار الضرر على الأعضاءالثلاثة سيكون الشاغل الرئيسى. كما قد تكون مقحمة في تدمير خلايا الدم الحمراء (انحلال الدم)،[5][6] الأضرار التي لحقت بالكبد (كبدى)،[7] القلب ( متعلق بعضلة القلب)،[8] الغدد الصماء (الغدة الكظرية، الغدد التناسلية، والغدة الدرقية)،[9][10][11] أو الكلى (كلوى)،[12] والضرر العام للخلايا.[2][13]
في ظروف غير عادية، من الممكن ملاحظة الآثار على الأنسجة الأخرى: وفي خلال رحلات الفضاء يشتبه في أن تركيزات الأكسجين العالية يمكن أن تسهم في تلف العظام.[14] فرط التأكسج يمكن أيضا بطريقة غير مباشرة أن يسبب تَخَدُّرٌ بأُحاديِّ أُكْسيدِ الكَرْبون للمرضى الذين يعانون من أمراض الرئة مثل مرض الدَّاءُ الرِّئَوِيُّ المُسِدُّ المُزْمِن، أوالذين يعانون من الاكتئاب التنفسي المركزي.[14]
فرط التهوية من الهواء الجوي في الضغوط الجوي لا يسبب سمية الأكسجين، لأن هواء مستوى سطح البحر يحتوي على الضغط الجزئي للأكسجين (PPO 2) من 0.21 بار (21 كيلو باسكال) والحد الأدنى للسمية هو أكثر من 0.3 بار (30 كيلو باسكال). [15]
العلامات والأعراض
الجهاز العصبي المركزي
| التعرض (بالدقائق) | عدد أفراد العينة | الأعراض |
|---|---|---|
| 96 | 1 | انبهار مطول، وقىء تصاحبه تشنجات شديدة |
| 60-69 | 3 | نفضان للشفة شديد، وشمق، وغثيان ودوار، وارتعاش الذراع |
| 50-55 | 4 | نفضان للشفة شديد، وانبهار، وانتحاب الشفاه، وغلبة النعاس، ودوار |
| 31-35 | 4 | الغثيان، والدوار، ونفضان للشفة، والتشنج |
| 21-30 | 6 | التشنج، والشعور بالنعاس، ونفضان للشفة شديد، والأَورَةٌ الشُرْسوفِيَّة، وتشنجات الذراع، وفقدان الذاكرة |
| 16-20 | 8 | التشنج، والدوار، ونفضان للشفة شديد، والأَورَةٌ الشُرْسوفِيَّة، والتنفس المتشنج |
| 11-15 | 4 | سيطرةالشهيق، ونفضان شديد للشفة، والإغماء، والغثيان، والارتباك |
| 6-10 | 6 | الدوار، ونفضان للشفة، والمذل، والدوخة، والتشنج الحجابى، والغثيان الشديد |
عندما تصيب سمية الأكسجين الجهاز العصبى المركزى فهناك أعراض تظهر وتغيرات أيضا مثل التغيرات البصرية (وخاصة الرؤية النفقية)، رنين في الأذنين (الطنين)، والغثيان، والوخز (وخاصة في الوجه)، والتهيج (تغيرات في الشخصية، والقلق، والارتباك، إلخ)، و الدوخة. هذا قد يعقبه نَوبَةٌ تَوَتُّرِيَّةٌ-رَمَعِيَّة مكونة من مرحلتين : يحدث انقباض شديد للعضلات لعدة ثوان (منشط) تليها تشنجات سريعة لاسترخاء العضلات المتناوبة وتقلص منتجا رجيج اختلاجى (رمعي). وتنتهى النوبة مع فترة من فقدان الوعي ( حالة تالٍ للنَّشْبَة ).[16] بدء النوبة يعتمد على الضغط الجزئى للأكسجين (PPO2) في مدة تنفس الغاز والتعرض له. ومع ذلك مدة التعريض قبل بدء الأعراض لايمكن التنبؤ بها، كما أظهرت الاختبارات تباين واسع، سواء فيما بين الأفراد، وفي نفس الفرد من يوم إلى يوم.[16] وبالإضافة إلى ذلك، فإن العديد من العوامل الخارجية، مثل الغمر تحت الماء، والتعرض للبرد، وممارسة التمارين الرياضية تقلل من نسبة الوقت لبدء ظهور الأعراض على الجهاز العصبي المركزي.[1] ويرتبط احتباس ثانى أكسيد الكربون بانخفاض درجة التحمل.[17] هناك عوامل أخرى مثل الظلام، والكافيين تزيد من درجة التحمل وذلك في حيوانات التجارب، ولكن هذه الآثار لم يتم اثباتها على البشر.[18]
الجهاز الرئوى
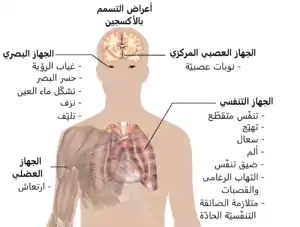
أعراض التسمم الرئوي تنتج عن التهاب والذي يبدأ في الشعب الهوائية متجها إلى الرئتين ومن ثم ينتشر في الرئتين (الشَّجَرَةُ الرُّغامِيَّةُ القَصَبِيَّة ). تظهر الأعراض في منطقة أعلى الصدر (مناطق تَحْتَ القَصّ والغضروفية).[20] ويبدأ هذا بمثابة دغدغة خفيفة قيما يتعلق بالاستنشاق وتتطور بعد ذلك إلى السعال المتكرر.[20] واذا لم يتم التوقف عن التنفس في حالة ارتفاع الضغوط الجزئية للأكسجين، يتعرض المرضى ويشعروا بحرقان خفيف عند الاستنشاق جنبا إلى جنب مع السعال الذي لا يمكن السيطرة عليه والضيق أحيانا في التنفس (بحة الصوت ).[20] شملت نتائج الفحص البدنى المتعلقة بسمية الجهاز الرئوى أصوات فقعية، تسمع من خلال سماعة الطبيب (خَرْخَرَةٌ فُقَّاعِيَّة ), والحمى، وزيادة تدفق الدم إلى بطانة الأنف (تبيغ من الغشاء المخاطي للأنف).[21] وتظهر نتائج إشعاع من داخل الرئتين الالتهاب والتورم من الرئتين يظهر الالتهاب والتورم (الوذمة الرئوية).[20] قلت قياسات وظائف الرئة، حيث ملاحظة انخفاض كمية تخزين الهواء وابقاءه في الرئتين التي تقوم بوظيفة حمل الهواء (السَّعَةُ الحَيَوِيَّة)، وتغيرات في عملية الزفير ومرانة الرئة.[22] وأوضحت الاختبارات على الحيوانات الاختلاف في التحمل مماثلة لتلك التي وجدت في سمية الجهاز العصبي المركزي، فضلا عن وجود تباينات واضحة بين الأنواع. عندما يكون التعرض للأكسجين أعلى من 0.5 بار (50 كيلو باسكال) متقطع، فإن هذا يسمح للرئتين التعافى وتأخر ظهور السمية.[23]
العين
في الأطفال الخدج، يلاحظ علامات تلف العين (اعتلال الشبكية للخداج، أو ROP) عبر منظار العين باعتبارها تحديد بين المناطق الوعائية و الغير وعائية لشبكية عين الرضيع. يتم استخدام درجة هذا التحديد لتعيين أربع مراحل: (أولا) يعد التحديد خط، (ثانيا) يصبح التحديد حرف. (ثالثا) نمو أوعية دموية جديدة وتنتشر حول الحرف. (رابعا) تبدأ شبكية العين في الانفصال من الجدار الداخلي للعين (المشيمية).[24]
الأسباب
تنجم سمية الأكسجين عن طريق التعرض للأكسجين في الضغوط الجزئية الأكبر من تلك التي يتعرض لها الجسم بمعدل وشكل طبيعي. يحدث هذا عن طريق ثلاثة مواضع رئيسة: الغوص تحت الماء، والعلاج من خلال ضغط الأكسجين المرتفع، وتوفير الأكسجين الإضافي، وخصوصا للأطفال الخدج. في كل حالة من هذه الحالات، تكون عوامل الخطر مختلفة بشكل ملحوظ.
تسمم الجهاز العصبي المركزي
انظر أيضا: انغماس تقني
التعرض، من دقائق إلى بضع ساعات، لضغوط جزئية من الأكسجين أعلى من 1.6 البارات (160 كيلو باسكال)- حوالى ثمانية أضعاف مستوى الغلاف الجوي الجزئي- ترتبط عادة بسمية الأكسجين للجهاز العصبى المركزى، وهى الأكثر احتمالية في الحدوث بين المرضى الذين يخضعون نظام المركزية وهي الأكثر احتمالا في الحدوث بين المرضى الذين يخضعون للعلاج عن طريق ضغط الأكسجين المرتفع والغواصون. نظراً لكون الضغط الجوي على مستوى سطح البحر حوالي 1 بار (100 كيلو باسكال)، يمكن أن تحدث سمية الجهاز العصبي المركزي فقط تحت ظروف الضغط العالي، حيث أن الضغط المحيط أعلى من المعدل الطبيعي.[25] يتنفس الغواصون الهواء في أعماق أكبر من 60 متر (200 قدم) مواجهون مخاطر متزايدة لسمية الأكسجين "اصابة" (نوبة). الغواصون الذين يتنفسوا المزيج من الغازات الغنية بالأكسجين، مثل النيتروكس، يمكن أن تعانى بالمثل من بعض النوبات في عمق أكثر ضحالة، الذين ينبغي عليهم النزول إلى العمق الأقصى ويتعدوا الحد المسموح للمزيج.[26]
تسمم الرئة
الرئتين، فضلا عن ما تبقى من الجهاز التنفسي، يتعرضوا لأعلى تركيز للأكسجين في جسم الإنسان، ولذلك فهى من الأعضاء الأولى والأساسية التي تصاب بالتسمم. يحدث تسمم الرئة عند التعرض للضغوط الجزئية للأكسجين عندما تكون أعلى من 0.5 بار (50 كيلو باسكال)، وهو ما يمثل نسبة الأوكسجين 50٪ عند الضغط الجوي الطبيعى. تبدأ علامات التسمم الرئوى في الظهور عن طريق الْتِهابُ الرُّغامَى و القَصَبات والتهاب في الشعب الهوائية العليا، وذلك بعد فترة غير مصحوبة بأعراض تمتد بين 4و22 ساعة في أكثر من 95٪ أكسجين،[27] تشير بعض الدراسات إلى أن عادة ما تبدأ الأعراض بعد حوالي 14 ساعة على هذا المستوى من الأكسجين.[28]
عند الضغوط الجزئية للأكسجين من 2 إلى 3 بار (200 و 300 كيلو باسكال) -100٪ الأكسجين يكون ضعف الضغط الجوى من 2 إلى 3، هذه الأعراض قد تبدأ في أقرب وقت حيث من الممكن بعد ثلاث ساعات من التعرض للأكسجين.[29] وعندما جريت تجارب على الفئران حيث تتنفس الأكسجين عند ضغوط تتراوح بين 1 و 3 بارات (100 و 300 كيلو باسكال) تبين أن مظهر الرئة المصابة بسمية الأكسجين يختلف عن مظهرها في نظام الضغط وذلك لتعرضها لحالة من الضغط الزائد.[30] دليل على انخفاض في وظيفة الرئة يمكن التأكد منه عن طريق اختبار لأداء الرئتين ويمكن الاختبار في أسرع وقت في خلال 24 ساعة من التعرض المستمر إلى 100٪ أكسجين،[31] مع أدلة على وجود ضرر سنخي منتشر وبداية متلازمة الضائقة التنفسية الحادة التي تحدث عادة بعد 48 ساعة من التعرض للأكسجين 100%.[29] تنفس الأكسجين 100٪ يؤدى في نهاية المطاف إلى انهيار الحويصلات الهوائية (انخماص)، في حين، في نفس الضغط الجزئي للأكسجين- وجود ضغوط جزئية كبيرة من الغازات الخاملة، وعادة النيتروجين، سيمنع هذا الأثر.[32]
ومن المعروف أن الأطفال حديثى الولادة قبل الأوان يتعرضوا لمخاطرة كبيرة وذلك لامكانية اصابتهم بالدَّاءُالرِّئَوِيُّ المُسِدُّ المُزْمِن مع التعرض الطويل لتركيزات عالية من الأكسجين.[33] هناك مجموعات أخرى عرضة لسمية الأكسجين حيث المرضى الذين يتعرضوا للتهوية الميكانيكية مع التعرض لمستويات أكسجين أعلى من 50٪، والمرضى المعرضين للمواد الكيميائية التي تزيد من خطر سمية الأكسجين مثل هذا البليوميسين (مضاد للأورام)عامل علاج كيميائى .[34] ولذلك، توصى المبادئ التوجيهية الحالية للمرضى المعرضين للتهوية الميكانيكية في العناية المركزة بالحفاظ على أن يكون تركيز الأكسجين أقل من 60٪.[29] وبالمثل، الغواصون الذين خضعوا لداءُ الغُوَّاص معرضون لخطر متزايد لامكانية الإصابة بسمية الأكسجين حيث يتطلب العلاج التعرض لفترات طويلة من الأكسجين والتنفس في وجود الضغط الزائد، بالإضافة إلى أي تعرض للأكسجين أثناء الغوص.[35]
تسمم العين
انظر أيضا: اعتلال الشبكية للأطفال حديثى الولادة قبل الأوان.
يسبب التعرض الطويل للجزيئات العالية والمؤثرة من الأكسجين إلى تلف شبكية العين.[36] الأضرار التي تلحق بالعين النامية للرضع المعرضة لجزيئات الأكسجين في الضغط العادى لديها لذات نسبة الأكسجين في الضغط العادي لديها آلية وتأثير مختلف عن عين الغواصين البالغين التي يحدث لها ضرر عند التعرض للضغط الزائد.[37] وقد يكون فرط التأكسج عاملا مساعدا للاضطراب يسمى التَّنَسُّجُ اللِّيْفِيُّ خَلْفَ العَدَسَة أو اعتلال الشبكية للخداج (ROP) في الأطفال الرضع.[38] في الخدج، غالبا ما تكون شبكية العين غالبا ما تكون غير وعائية غير كاملة. يحدث اعتلال الشبكية عند الخدج عندما يبدأ نمو الأوعية الدموية في شبكية العين ثم يتوقف أو ينتقل بشكل غير طبيعي. يرتبط مع نمو هذه الأوعية الجديدة نسيج ليفي (نَسيجٌ نَدْبِيّ) التي قد يتقلص ويسبب انفصال الشبكية. التعرض للأكسجين الإضافي، في حين أنه أحد عوامل الخطر، لكنه ليس هو عامل الخطر الرئيسي لنمو هذا المرض. تقييد استخدام الأكسجين الإضافي لا يقلل بالضرورة من معدل اعتلال الشبكية للخداج، ويمكن أن يزيد من مخاطر حدوث نقص التأكسج المرتبط بمضاعفات للنظام.[39]
حدث قصر النظر مفرط التأكسج في دائرة مغلقة يتم فيها تنفس الأكسجين واعادة التنفس من قبل الغواصين والتعرض لذلك لفترات طويلة.[37] ويحدث كثيرا للذين يخضعون للعلاج المتكرر عن طريق التعرض للضعط العالى من الأكسجين.[40] يعود ذلك إلى زيادة في انكسار قوة العدسة، منذ أن الطول محوري وقراءات قياس القرنية لا يكشفوا عن وجود أساس القرنية أو طول لتحول قصر النظر.[41] وعادة ما يكون العكس مع مرور الوقت.[42]
آلية العمل
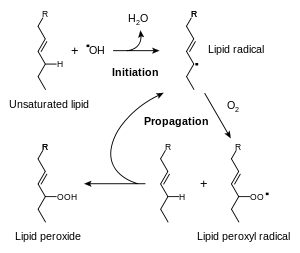
المقالات الرئيسة:أنواع الأكسجين التفاعلية و الضغط التأكسدى
أساس البيوكيميائية لسمية الأكسجين هو الحد الجزئي للأكسجين بواحد أو اثنين من الإلكترونات لتشكيل أنواع الأكسجين التفاعلية,[43] التي تعد منتجات طبيعية من الأيض الغذائى للأكسجين وتلعب دور هام في إشارة الخلية.[44] أحد الأنواع النى ينتجها الجسم وهو أنيون فوق الأكسيد(O-2),[45] ومن الممكن أنه يقوم بدور في اكتساب الحديد.[46] تؤدى التركيزات العالية الأكثر من الطبيعى للأكسجين إلى زيادة أنواع مستويات الأكسجين التفاعلية.[47] يعد الأكسجين ضرورى لاستقلاب الخلايا ولامداد جميع أجزاء الجسم بالدم الذي يحتاجه. عند تنفس الأكسجين عند ضغوط جزئية عالية، ستنتشر حالة فرط التأكسج مع أنسجة وعائية سريعة التأثر. خلال الأوقات التي يكون هناك فيهاجهاد بيئي، يمكن لمستويات من أنواع الاكسجين التفاعلية أن تزيد بشكل كبير، والتي يمكن أن تلحق الضرر بهياكل الخلية وانتاج الضغط التأكسدى.[48]
في حين أن جميع اليات تفاعل هذه الأنواع داخل الجسم تزال غير مفهومة تماما,[49] الا ان مجموعة الهيدروكسيل (OH) تعد أحد أهم العناصر التفاعلية للضغط التأكسدى، والتي من الممكن أن تبدأسلسة من التفاعلات الضارة لانزيمات الدهون في الدهون الغير مشبعة في أغشية الخلايا. تزيد التركيزات العالية من الأكسجين أيضا تشكيل الجذور الحرة الأخرى مثل أكسيد النيتريك، النيتريك البيروكسى، وثلاثى أكسيد ثانى الهيدروجين والذي يضر الDNA والجزيئات الحيوية الأخرى.[50] على الرغم من أن الجسم لديه العديد من الأنظمة المضادة للأكسدة مثل الجلوتاثيون التي تتجنب الضغط التأكسدى، هزمت هذه النظم في نهاية المطاف على مستوى عالى جدا من الأكسجين الحر، ويتجاوز معدل تلف الخلايا قدرة الأنظمة التي تمنعه أو تقوم على إصلاحه.[51] ومن ثم ينتج تلف الخلايا وموتها.[52]
التشخيص
يصعب تشخيص سمية الأكسجين للجهاز العصبى المركزى للغواصين قبل حدوث النوبة، كما أن الأعراض مثل اضطراب البصر، ومشاكل الأذن، والدوخة، والارتباك والغثيان يمكن أن تكون بسبب العديد من العوامل الشائعة إلى توجد في البيئة المائية مثل الخدر و الاحتقان والبرودة. ومع ذلك، قد تكون هذه الأعراض نافعة في تشخيص المراحل الأولى من سمية الأكسجين للمرضى الذين يخضعون للعلاج بالأكسجين العالى الضغط. في كلتا الحالتين، ما لم يكن هناك تاريخ سابق لمرض الصرع أو اختبارات تشير إلى نقص سكر الدم، فان النوبة تحدث في المواضعالتي يتنفس فيها الأكسجين عند ضغوط جزئية أعلى من 1.4 بار (140 كيلو باسكال) وتشير إلى القيام بالتشخيص وعلامات لوجود سمية الأكسجين.[53]
يصعب تشخيص خلل التنسج القصبي الرئوي في الأطفال حديثي الولادة الذين يعانون من صعوبات في التنفس في الأسابيع القليلة الأولى. ومع ذلك، إذالم يتم تحسن تنفس الرضيع خلال هذا الوقت، يمكن أن تستخدم اختبارات الدم والأشعة السينية لتأكيد وجود خلل التنسج القصبي الرئوي. وبالإضافة إلى ذلك، يمكن أن يساعد مخطط صدى القلب على القضاء على أية أسباب أخرى محتملة مثل عيوب القلب الخلقية أو ارتفاع ضغط الدم الشرياني الرئوي.[54]
اقترح تشخيص اعتلال الشبكية في الأطفال الرضع من قبل الاعدادات الاكلينيكية. الخداج، حيث انخفاض وزنهم عند الولادة وتاريخ من التعرض لللأكسجين هي المؤشرات الرئيسية، في حين أنه لم يتم اثبات وجود عوامل وراثية لتسفر هذا النموذج.[55]
الوقاية

الوقاية من سمية الأكسجين تعتمد اعتمادا كليا على الاستعدادات. تقضى الاحتياطات المناسبة تحت الماء وفي الفضاء، على الآثار الأكثر خبثاو ضررا. عادة ما يتطلب الأطفال الخدج الأكسجين الإضافي لعلاج مضاعفات الولادة المبكرة. في هذه الحالة يجب أن تتم الوقاية من خلل التنسج القصبي الرئوي واعتلال الشبكية للخداج دون أن يتم المساس بإمدادات الأكسجين الكافى للحفاظ على حياة الرضيع.
المراجع
- Donald, Part I 1947.
- Clark & Thom 2003, pp. 358–360.
- Acott, Chris (1999). "Oxygen toxicity: A brief history of oxygen in diving". South Pacific Underwater Medicine Society Journal 29 (3): 150–5. ISSN 0813-1988. OCLC 16986801. Retrieved 29 April 2008.
- Beehler, CC (1964). "Oxygen and the eye". Survey of Ophthalmology 45: 549–60. ببمد 14232720.
- Goldstein, JR; Mengel, CE (1969). "Hemolysis in mice exposed to varying levels of hyperoxia". Aerospace Medicine 40 (1): 12–13. ببمد 5782651.
- Larkin, EC; Adams, JD; Williams, WT; Duncan, DM (1972). "Hematologic responses to hypobaric hyperoxia". American Journal of Physiology 223 (2): 431–7. ببمد 4403030.
- Schaffner, Fenton; Felig, Philip (1965). "CHANGES IN HEPATIC STRUCTURE IN RATS PRODUCED BY BREATHING PURE OXYGEN" (PDF). Journal of Cell Biology 27 (3): 505–17. doi:10.1083/jcb.27.3.505. PMC 2106769. ببمد 5885427.
- Caulfield, JB; Shelton, RW; Burke, JF (1972). "Cytotoxic effects of oxygen on striated muscle". Archives of Pathology 94 (2): 127–32. ببمد 5046798.
- Bean, JW; Johnson, PC (1954). "Adrenocortical response to single and repeated exposure to oxygen at high pressure". American Journal of Physiology 179 (3): 410–4. ببمد 13228600.
- Edstrom, JE; Rockert, H (1962). "The effect of oxygen at high pressure on the histology of the central nervous system and sympathetic and endocrine cells". Acta Physiologica Scandinavica 55 (2–3): 255–63. doi:10.1111/j.1748-1716.1962.tb02438.x. ببمد 13889254.
- Gersh, I; Wagner, CE (1945). "Metabolic factors in oxygen poisoning". American Journal of Physiology 144 (2): 270–7.
- Hess, RT; Menzel, DB (1971). "Effect of dietary antioxidant level and oxygen exposure on the fine structure of the proximal convoluted tubules". Aerospace Medicine 42 (6): 646–9. ببمد 5155150.
- Clark, John M (1974). "The toxicity of oxygen". American Review of Respiratory Disease 110 (6 Pt 2): 40–50. ببمد 4613232.
- Patel, Dharmeshkumar N; Goel, Ashish; Agarwal, SB; Garg, Praveenkumar; Lakhani, Krishna K (2003). "Oxygen toxicity" (PDF). Journal, Indian Academy of Clinical Medicine 4 (3): 234–237. Retrieved 28 September 2008.
- Clark & Lambertsen 1970.
- Clark & Thom 2003, p. 376.
- Lang 2001, p. 82.
- Bitterman, N.; Melamed, Y.; Perlman, I. (1986). "CNS oxygen toxicity in the rat: role of ambient illumination". Undersea Biomedical Research 13 (1): 19–25. ببمد 3705247. Retrieved 20 September 2008.
- Dharmeshkumar N Patel; Ashish Goel; SB Agarwal; Praveenkumar Garg; et al. (2003). "Oxygen Toxicity" (PDF). Indian Academy of Clinical Medicine. 4 (3): 234. مؤرشف من الأصل (PDF) في 27 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Clark & Thom 2003, p. 383.
- Clark, John M.; Lambertsen, Christian J. (1971). "Rate of development of pulmonary O2 toxicity in man during O2 breathing at 2.0 Ata". Journal of Applied Physiology 30 (5): 739–52. ببمد 4929472
- Clark, John M.; Lambertsen, Christian J. (1971). "Rate of development of pulmonary O2 toxicity in man during O2 breathing at 2.0 Ata". Journal of Applied Physiology 30 (5): 739–52. ببمد 4929472.
- Smith, J.Lorrain (1899). "The pathological effects due to increase of oxygen tension in the air breathed" (PDF). Journal of Physiology (London: The Physiological Society and Blackwell Publishing) 24 (1): 19–35. PMC 1516623. ببمد 16992479. Note: 1 atmosphere (atm) is 1.013 bars.
- Fielder, Alistair R. (1993). Fielder, Alistair R.; Best, Anthony; Bax, Martin C. O, ed. The Management of Visual Impairment in Childhood. London: Mac Keith Press : Distributed by Cambridge University Press. p. 33. ISBN 0-521-45150-7.
- Smerz, R.W. (2004). "Incidence of oxygen toxicity during the treatment of dysbarism". Undersea and Hyperbaric Medicine 31 (2): 199–202. ببمد 15485081. Retrieved 30 April 2008.
- Lang 2001, p. 7.
- Bitterman, H. (2009). "Bench-to-bedside review: Oxygen as a drug". Critical Care 13 (1): 205. doi:10.1186/cc7151. PMC 2688103. ببمد 19291278. ^ Jump up to: a b c
- Jackson, R.M. (1985). "Pulmonary oxygen toxicity". Chest 88 (6): 900–905. doi:10.1378/chest.88.6.900. ببمد 3905287. Jump up ^
- Bitterman, H. (2009). "Bench-to-bedside review: Oxygen as a drug". Critical Care 13 (1): 205. doi:10.1186/cc7151. PMC 2688103. ببمد 19291278
- Demchenko, Ivan T.; Welty-Wolf, Karen E.; Allen, Barry W.; Piantadosi, Claude A. (2007). "Similar but not the same: normobaric and hyperbaric pulmonary oxygen toxicity, the role of nitric oxide". American Journal of Physiology – Lung Cellular and Molecular Physiology 293 (1): L229–38. doi:10.1152/ajplung.00450.2006. ببمد 17416738
- Jackson, R.M. (1985). "Pulmonary oxygen toxicity" (PDF). Chest 88 (6): 900–905. doi:10.1378/chest.88.6.900. ببمد 3905287.
- Wittner, M.; Rosenbaum, R.M. (1966). Pathophysiology of pulmonary oxygen toxicity. Proceedings of the Third International Conference on Hyperbaric Medicine (NAS/NRC, 1404, Washington DC): 179–88. – and others as discussed by Clark & Lambertsen 1970, pp. 256–60.
- Bancalari, Eduardo; Claure, Nelson; Sosenko, Ilene R.S. (2003). "Bronchopulmonary dysplasia: changes in pathogenesis, epidemiology and definition". Seminars in Neonatology (London: Elsevier Science) 8 (1): 63–71. doi:10.1016/S1084-2756(02)00192-6. ببمد 12667831
- Jackson, R.M. (1985). "Pulmonary oxygen toxicity". Chest 88 (6): 900–905. doi:10.1378/chest.88.6.900. ببمد 3905287
- Smerz, R.W. (2004). "Incidence of oxygen toxicity during the treatment of dysbarism". Undersea and Hyperbaric Medicine 31 (2): 199–202. ببمد 15485081. Retrieved 30 April 2008
- Yarbrough, O.D.; Welham, W.; Brinton, E.S.; Behnke, Alfred R. (1947). "Symptoms of Oxygen Poisoning and Limits of Tolerance at Rest and at Work". Nedu-47-01 (United States Navy Experimental Diving Unit Technical Report). Retrieved 29 April 2008.
- Butler, Frank K.; White, E.; Twa, M. (1999). "Hyperoxic myopia in a closed-circuit mixed-gas scuba diver". Undersea and Hyperbaric Medicine 26 (1): 41–5. ببمد 10353183. Retrieved 29 April 2009.
- Nichols, C.W.; Lambertsen Christian (1969). "Effects of high oxygen pressures on the eye". New England Journal of Medicine 281 (1): 25–30. doi:10.1056/NEJM196907032810106. ببمد 4891642
- Drack, A.V. (1998). "Preventing blindness in premature infants". New England Journal of Medicine 338 (22): 1620–1. doi:10.1056/NEJM199805283382210. ببمد 9603802.
- Anderson Jr., B.; Shelton, D.L. (1987). "Axial length in hyperoxic myopia". In: Bove, Alfred A.; Bachrach, Arthur J.; Greenbaum, Leon (eds.) Ninth International Symposium of the UHMS (Undersea and Hyperbaric Medical Society): 607–11
- Anderson Jr., B.; Shelton, D.L. (1987). "Axial length in hyperoxic myopia". In: Bove, Alfred A.; Bachrach, Arthur J.; Greenbaum, Leon (eds.) Ninth International Symposium of the UHMS (Undersea and Hyperbaric Medical Society): 607–11.
- Anderson, B.; Farmer, Joseph C. (1978). "Hyperoxic myopia". Transactions of the American Ophthalmological Society 76: 116–24. PMC 1311617. ببمد 754368
- Clark & Thom 2003, p. 360.
- Rhee S.G. (2006). "Cell signaling. H2O2, a necessary evil for cell signaling". Science 312 (5782): 1882–1883. doi:10.1126/science.1130481. ببمد 16809515.
- Thom, Steven R. (1992). "Inert gas enhancement of superoxide radical production". Archives of Biochemistry and Biophysics 295 (2): 391–6. doi:10.1016/0003-9861(92)90532-2. ببمد 1316738.
- Ghio, Andrew J.; Nozik-Grayck, Eva; Turi, Jennifer; Jaspers, Ilona; Mercatante, Danielle R.; Kole, Ryszard; Piantadosi, Claude A. (2003). "Superoxide-dependent iron uptake: a new role for anion exchange protein 2". American Journal of Respiratory Cell and Molecular Biology 29 (6): 653–60. doi:10.1165/rcmb.2003-0070OC. ببمد 12791678.
- Fridovich, I. (1998). "Oxygen toxicity: a radical explanation" (PDF). Journal of Experimental Biology 201 (8): 1203–9. ببمد 9510531.
- Bitterman, N. (2004). "CNS oxygen toxicity". Undersea and Hyperbaric Medicine 31 (1): 63–72. ببمد 15233161. Retrieved 29 April 2008.
- Imlay, J.A. (2003). "Pathways of oxidative damage". Annual Review of Microbiology 57: 395–418. doi:10.1146/annurev.micro.57.030502.090938. ببمد 14527285.
- Bowen, R. "Free Radicals and Reactive Oxygen". Colorado State University. Retrieved 26 September 2008.
- Thom, Steven R.; Marquis, R.E. (1987). "Free radical reactions and the inhibitory and lethal actions of high-pressure gases". Undersea Biomedical Research 14 (6): 485–501. ببمد 2825395. Retrieved 26 September 2008.
- Kim, Y.S.; Kim, S.U. (1991). "Oligodendroglial cell death induced by oxygen radicals and its protection by catalase". Journal of Neuroscience Research 29 (1): 100–6. doi:10.1002/jnr.490290111. ببمد 1886163.
- NBDHMT (4 February 2009). "Recommended Guidelines for Clinical Internship in Hyperbaric Technology (V: C.D)". Harvey, LA: National Board of Diving and Hyperbaric Medical Technology. Archived from the original on 20 September 2007. Retrieved 26 March 2009.
- "How is bronchopulmonary dysplasia diagnosed?". U.S. Department of Health & Human Services. Retrieved 28 September 2008
- Regillo, Brown & Flynn 1998, p. 178.
- بوابة غوص
- بوابة طب
