أميد الليثيوم
أميد الليثيوم مركب كيميائي لا عضوي له الصيغة LiNH2، ويكون على شكل بلورات بيضاء.
| أميد الليثيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
أميد الليثيوم | |
| المعرفات | |
| رقم CAS | 7782-89-0 |
| بوب كيم (PubChem) | 16211536 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | LiNH2 |
| الكتلة المولية | 22.96 غ/مول |
| المظهر | بلورات بيضاء |
| نقطة الانصهار | 390 °س |
| نقطة الغليان | 430 °س |
| الذوبانية في الماء | يتفكك |
| المخاطر | |
| ترميز المخاطر |  F F
 C C |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- تكون الرابطة بين أيون الليثيوم والأميد رابطة أيونية، ويعبر عنها بالشكل -Li+NH2 .
- يتفكك أميد الليثيوم عند التماس مع الماء.
أميدات الليثيوم
يطلق اسم أميدات الليثيوم في الكيمياء العضوية على أملاح الليثيوم للأمينات أي لها الصيغة العامة -Li+NR2 ، مثل مركب ثنائي إيزوبروبيل أميد الليثيوم (LDA) الذي لديه استخدامات عديدة.
تحضر هذه الأميدات من تفاعل الليثيوم مع الأمين الموافق، ويرافق ذلك انطلاق غاز الهيدروجين حسب المعادلة:
تمتاز مركبات أميدات الليثيوم بنشاطها الكيميائي وتعد من القواعد القوية. وفي حال عدم إعاقة ذرة النيتروجين فراغياً فإن هذه المركبات لها صفة أليفة النواة (نكليوفيلية).
أمثلة
لقد تم التمكن من بلورة ملح الليثيوم لمركب 6،6،2،2-رباعي ميثيل بيبيريدين على شكل رباعي وحدات (تترامير).
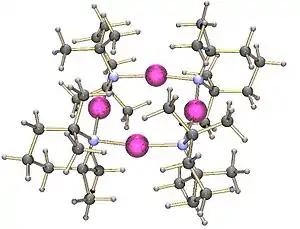
بالمقابل فإن مشتق الليثيوم لمركب ثنائي-(1-فينيل إيثيل)أمين يتبلور على شكل ثلاثي وحدات (تريمير).
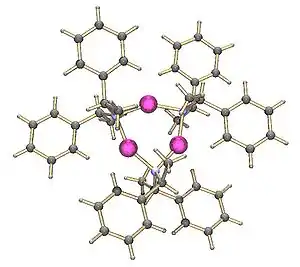
كما أنه من الممكن تشكيل وحدات قليلة مختلطة من ألكوكسيدات الفلز والأميدات.[5] ولهذه المركبات الناشئة صلة بالقواعد الفائقة والتي هي مزيج من ألكوكسيدات الفلزات والألكيلات. من الممكن أيضاً أن يتشكل قليل وحدات حلقي وذلك عندما يشكل نيتروجين الأميد رابطة سيغما مع الليثيوم، في حين يشارك الزوج الوحيد الإلكتروني مع ذرة فلز أخرى.
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/24532 — تاريخ الاطلاع: 14 أكتوبر 2016 — العنوان : LITHIUM AMIDE — الرخصة: محتوى حر
- Lithium amide hydrogen-storage grade | Sigma-Aldrich نسخة محفوظة 29 أبريل 2009 على موقع واي باك مشين.
- M.F. Lappert, M.J. Slade, A. Singh, J.L. Atwood, R.D. Rogers and R. Shakir (1983). "Structure and reactivity of sterically hindered lithium amides and their diethyl etherates: crystal and molecular structures of [Li{N(SiMe3)2}(OEt2)]2 and tetrakis(2,2,6,6-tetramethylpiperidinatolithium)". Journal of the American Chemical Society. 105 (2): 302–304. doi:10.1021/ja00340a031. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - D.R. Armstrong, K.W. Henderson, A.R. Kennedy, W.J. Kerr, F.S. Mair, J.H. Moir, P.H. Moran and R. Snaith, Dalton Transactions, 1999, 4063.
- K.W. Henderson, D.S. Walther and P.G. Williard (1995). "Identification of a Unimetal Complex of Bases by 6Li NMR Spectroscopy and Single-Crystal Analysis". Journal of the American Chemical Society. 117 (33): 8680–8681. doi:10.1021/ja00138a030. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء