نترات السترونشيوم
نترات السترونشيوم مركب كيميائي له الصيغة Sr(NO3)2 ، ويكون على شكل بلورات بيضاء .
| نترات السترونشيوم | |
|---|---|
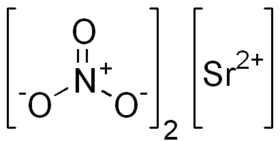 نترات السترونشيوم | |
| الاسم النظامي (IUPAC) | |
نترات السترونشيوم | |
| المعرفات | |
| رقم CAS | 10042-76-9 |
| بوب كيم | 24848 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | Sr(NO3)2 |
| الكتلة المولية | 211.63 غ/مول |
| المظهر | بلورات بيضاء |
| الكثافة | 2.986 غ/سم3 |
| نقطة الانصهار | 570 °س |
| نقطة الغليان | 645 °س |
| الذوبانية في الماء | 71 غ/100 مل ماء عند 18 °س |
| الذوبانية | غير منحل في الإيثانول والأسيتون |
| المخاطر | |
| ترميز المخاطر |  O O
 Xi Xi |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- ينحل مركب نترات السترونشيوم بشكل جيد جداً في الماء حيث يشكل محلول معتدلاً، أي أن الأس الهيدروجيني pH ≈ 7.
- لا ينحل مركب نترات السترونشيوم لا في الإيثانول ولا في الأسيتون.
التحضير
يحضر مركب نترات السترونشيوم من تفاعل كربونات السترونشيوم مع حمض النتريك ذي تركيز 60% حسب المعادلة:
- SrCO3 + 2HNO3 → Sr(NO3)2 + H2O + CO2
بتبخير المحلول الناتج نحصل على ملح نترات السترونشيوم الخالي من الماء. في حال ترك المحلول يتبرد ببطء دون تبخير نحصل على شكل رباعي الهيدرات (يتبلور مع أربع جزيئات ماء). يتميز رباعي الهيدرات من نترات السترونشيوم بأنه يتفتت بالتماس مع الهواء.
نحصل على الشكل الخالي من الماء مرة أخرى بالتسخين فوق 100°س.
الاستخدامات
يستخدم مركب نترات السترونشيوم في الألعاب النارية حيث يعطي لهباً أحمر.
المصادر
- Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4
المراجع
- معرف بوب كيم: https://pubchem.ncbi.nlm.nih.gov/compound/24848 — تاريخ الاطلاع: 19 نوفمبر 2016 — العنوان : 10042-76-9 — الرخصة: محتوى حر
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.