عامل 12
عامل تجلط الدم الثاني عشر، المعروف أيضا باسم عامل هاجمان، هو بروتين البلازما. وهو إنزيم (EC 3.4.21.38) من الطبقة البروتينية سيرين (أو سيبيريد endopeptidase). في البشر، يتم ترميز العامل الثاني عشر بواسطة جين F12.[1]
بناء
العامل البشري الثاني عشر هو 596 من الأحماض الأمينية الطويلة ويتكون من سلسلتين، السلسلة الثقيلة (353 بقايا) وسلسلة خفيفة (243 بقايا) يربطهما سند ثنائي الكبريتيد. ومن 80,000 دالتونز . تحتوي سلسلته الثقيلة على نطاقين من فبرونيكتين (النوع الأول والثاني) ، ونطاقا شبيهان بمثيل نمو البشرة، ونطاق كرينجل، ومنطقة غنية بالبرولين، وسلسلة خفيفة تحتوي على مجال البروتياز. في الآونة الأخيرة، تم حل بنية المجال الترادفي FnI-EGF الشبيه بعامل التجلط 12 عن طريق البلورات بالأشعة السينية[2][3]
.
الوظيفة
العامل الثاني عشر هو جزء من سلسلة تجلط الدم وينشط العامل 12 في المختبر. يتم تنشيط العامل 12 نفسه لعامل 12أ بواسطة الأسطح المشحونة سالبًا، مثل الزجاج. هذه هي نقطة البداية للمسار الجوهري. يمكن استخدام العامل الثاني عشر أيضًا لبدء مجموعات تجلط الدم في الدراسات المختبرية.[4]
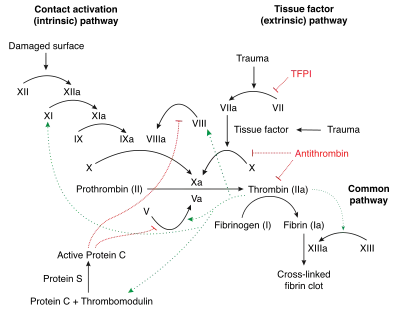
الدور في المرض
عامل XII هو اضطراب نادر موروث .[5] على عكس أوجه القصور الأخرى لعامل التخثر، يكون عوز العامل الثاني عشر عديم الأعراض تمامًا ولا يسبب نزيفًا زائدًا.[5] ومع ذلك، فإن الفئران التي تفتقر إلى جين العامل الثاني عشر تكون أقل عرضة للتخثر. يبدو أن البروتين مرتبط في المراحل المتأخرة من تكوين الجلطة بدلاً من الانسداد الأول للأضرار في جدار الأوعية الدموية.[6] يؤدي العامل الثاني عشر دورًا مهمًا في تكوين الجلطة أثناء إجراء قياسات في المختبر لوقت الثرومبوبلاستين الجزئي، مما يتسبب في إطالة هذه القياسات بشكل ملحوظ لدى المرضى الذين يعانون من نقص العامل الثاني عشر، وعادة ما يتجاوز ذلك أيضًا ما يُرى في الهيموفيليا A ، أو الناعور B ونتيجة لذلك، فإن القلق الرئيسي المتعلق بعجز العامل الثاني عشر هو الاختبار غير الضروري، والتأخير في الرعاية، والقلق، وما إلى ذلك التي يمكن أن تدفعها نتيجة المختبر غير الطبيعية. كل هذا، بما في ذلك آلية الوراثة، ينطبق أيضا على عوامل الاتصال الأخرى، والكينينوجين عالي الوزن الجزيئي.[5]
المستويات الزائدة من العامل 12 يمكن أن تؤهب الأفراد نحو خطر أكبر من الخثار الوريدي بسبب دور العامل الثاني عشر كأحد العوامل الحافزة لتحويل البلازمينوجين إلى شكل البلازمين الفعال للبلازمين.[7]
يتم تنشيط عامل الثاني عشر أيضا من قبل السموم الداخلية، وخاصة الدهون A.
التاريخ
تم اكتشاف عامل هاجمان لأول مرة في عام 1955 عندما تم العثور على عينة دم قبل الجراحة روتينية لرجل يبلغ من العمر 37 عاما، وهو براكماي السكك الحديدية جون هاجمان (1918) كان لديه نسبة التخثر في أنابيب الاختبار عالية جدا، على الرغم من عدم وجود أعراض نزفية له. ثم تم فحص هاجمان من قبل اختصاصي أمراض الدم أوسكار راتنوف، الذي وجد أن هاجمان كان يفتقر إلى عامل تخثر غير معروف من قبل.[8] وجد راتنوف فيما بعد أن عوز هاجمان عامل هو اضطراب وراثي جسمي متنحي، بعد فحص العديد من الأشخاص ذوي الصلة الذين لديهم نقص. من المفارقات أن الانسداد الرئوي ساهم في وفاة هاجمان بعد حادث مهني. ومنذ ذلك الحين، حددت دراسات الحالة والدراسات السريرية وجود ارتباط بين الخُثار ونقص العامل الثاني عشر.[9]
مراجع
- Cool DE, MacGillivray RT (Oct 1987). "Characterization of the human blood coagulation factor XII gene. Intron/exon gene organization and analysis of the 5'-flanking region". The Journal of Biological Chemistry. 262 (28): 13662–73. PMID 2888762. مؤرشف من الأصل في 11 مايو 2020. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Stavrou E, Schmaier AH (Mar 2010). "Factor XII: what does it contribute to our understanding of the physiology and pathophysiology of hemostasis & thrombosis". Thrombosis Research. 125 (3): 210–5. doi:10.1016/j.thromres.2009.11.028. PMC 2851158. PMID 20022081. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Beringer DX, Kroon-Batenburg LM (Feb 2013). "The structure of the FnI-EGF-like tandem domain of coagulation factor XII solved using SIRAS". Acta Crystallographica Section F. 69 (Pt 2): 94–102. doi:10.1107/S1744309113000286. PMC 3564606. PMID 23385745. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Renné T, Schmaier AH, Nickel KF, Blombäck M, Maas C (Nov 2012). "In vivo roles of factor XII". Blood. 120 (22): 4296–303. doi:10.1182/blood-2012-07-292094. PMC 3507141. PMID 22993391. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Wagenman BL, Townsend KT, Mathew P, Crookston KP (Jun 2009). "The laboratory approach to inherited and acquired coagulation factor deficiencies". Clinics in Laboratory Medicine. 29 (2): 229–52. doi:10.1016/j.cll.2009.04.002. PMID 19665676. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Renné T, Pozgajová M, Grüner S, Schuh K, Pauer HU, Burfeind P, Gailani D, Nieswandt B (Jul 2005). "Defective thrombus formation in mice lacking coagulation factor XII". The Journal of Experimental Medicine. 202 (2): 271–81. doi:10.1084/jem.20050664. PMC 2213000. PMID 16009717. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Kroll, Michael H. (2001). Manual of Coagulation Disorders. Blackwell Science. صفحات 3–4, 206–207. ISBN 0-86542-446-2. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ratnoff OD, Margolius A (1955). "Hageman trait: an asymptomatic disorder of blood coagulation". Transactions of the Association of American Physicians. 68: 149–54. PMID 13299324. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Gordon EM, Gallagher CA, Johnson TR, Blossey BK, Ilan J (Apr 1990). "Hepatocytes express blood coagulation factor XII (Hageman factor)". The Journal of Laboratory and Clinical Medicine. 115 (4): 463–9. PMID 2324612. الوسيط
|CitationClass=تم تجاهله (مساعدة)
- بوابة الكيمياء الحيوية
- بوابة طب