البروتين المرتبط بكريسبر 9
البروتين المرتبط بكريسبر 9 (CRISPR associated protein 9؛ Cas9 كاس ناين[1]) بروتين مضاد لفيروسات الحمض النووي. يواجه العلماء قرارات صعبة عندما لا تتطابق أحدث نتائج تحرير الجينات مع نتائج التقنيات الأخرى. كان جيسون شيلتزر، عالم الأحياء السرطانية في مختبر كولد سبرينغ هاربور في نيويورك، يبحث عن الجينات المرتبطة بنمو الورم. خطط هو وزملاؤه لتعطيل الجينات باستخدام أداة تحرير الجينات الشائعة كريسبر-cas9) cas9 هو انزيم نووي داخلي يحفز تقسيم موقع محدد في الحمض النووي منقوص الأكسجين الثنائي)، بعد ذلك بحث عن التغيرات التي خفضت معدل تضاعف الخلايا السرطانية. لكنهم كانوا بحاجة إلى جين تحكم من شأنه أن يسفر عن نفس التأثير .
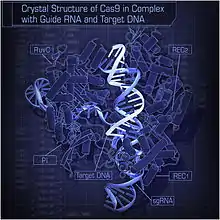 | |
| Crystal structure of S pyogenes Cas9 in complex with guide RNA and its target DNA at 2.5 A ˚ resolution.(Nishimasu, et al. 2014) | |
| معرفات | |
| الكائن | |
| الرمز | cas9 |
| Alt. symbols | SPy_1046 |
| المركز الوطني لمعلومات التقانة الحيوية | NP_269215.1 |
| يونيبروت | Q99ZW2 |
| معلومات أخرى | |
| رقم التصنيف الإنزيمي | 3.1.-.- |
| كروموسوم | genomic: 0.85 - 0.86 Mb |
يشير الإنتاج الفكري إلى أن جين MELK ميلك كان مثاليا: كانت هناك أدلة وافرة على أهمية ذلك في تكاثر الخلايا السرطانية، والتجارب السريرية قيد التنفيذ لاختبار الأدوية التي تثبط بروتين ميلك. ولكن تعطيل الجين باستخدام كريسبر-Cas9 لم ينتج أي تأثير. يقول شلتزر: "لقد ألقى كريسبر-Cas9 مفتاحا في تجاربنا. واضاف "ان كل شيء توقف".
وبهذه النتيجة، انضم شيلتزر وفريقه إلى ناد متزايد من المختبرات التي دفعت على إعادة تقييم وتكرار التجارب، حيث أن انتشار كريسبر-Cas9 يكشف الأخطاء المحتملة في البيانات التي تم جمعها باستخدام التقنيات القديمة. وفي 3 نيسان / أبريل، قدم فريق شلتزر النتائج في الاجتماع السنوي للرابطة الأمريكية لابحاث السرطان في واشنطن العاصمة. وقد نشرت النتائج أيضا في مجلة eLife1
يقول مايكل باسيك، عالم الأحياء الجزيئي في جامعة ستانفورد في كاليفورنيا: "هناك الكثير من العمل الذي يتعين القيام به، فقط تكرار نفس التحريات التي قام بها الناس" مع طرق أخرى. "وأعتقد أنه من الإنصاف القول، للحصول على بيانات أفضل بكثير"
مقياس المشكلة
كان ناثان لوسون، عالم البيولوجيا الجزيئية في كلية الطب بجامعة ماساتشوستس في ورسستر، واحدا من أول من وصف المشكلة بشكل منهجي. في عام 2015، قرر هو وزملاؤه جهودهم لمقارنة النتائج من طريقتين في سمكة الزرد: تعطيل الجينات باستخدام تقنية التحرير الجيني تسمى انزيمات الحمض النووي إصبع زنك، والتقليل من التعبير الجيني باستخدام ادوات جزيئية تسمى مورفولينوس . ووجد الباحثون أن نصف العشرين جين التي اختبروها أسفرت عن نتائج مختلفة 2. وكشفت شبكة إضافية من خلال قواعد البيانات الوراثية والأنتاج الفكري للمورفولينو أن 80٪ من نتائج تجارب مورفولينو التي نشرت غير قابلة للتكرار في الطفرات الوراثية 2
وقال بعض الباحثين في سمكة الزرد انهم رحبوا بالتقرير الذي وصف نتائج البحث لأنها دفعت المجتمع لمواجهة مشكلة لوحظت انها نادرة. البعض الآخر لم يكن سعيدا جدا. يقول لوسون: "حصلت على بعض الأشخاص الذين قالوا لي إنني أفسدت المجال"
وقد تفاقمت تناقضات مماثلة في كائنات أخرى. في نموذج نبات أرابيدوبسيس ثاليانا (نبات الرشاد)، أظهر استخدام كريسبر-Cas9 أن بروتين يعتقد سابقا أنه يتوسط آثار الهرمون النباتي أوكسين ليس لديه هذه الوظيفة 3. في ذباب الفاكهة والخلايا البشرية، اظهرت دراسات الفحص الكبيرة قد تحولت على نطاق واسع التناقضات بين النتائج التي تم الحصول عليها باستخدام تداخل الحمض النووي الريبوزي (رناي) - وهي تقنية تقلل من التعبير الجيني - وتلك الناتجة عن الطفرات الوراثية 4 .
كلا الطريقتين لهاقيودها، يلاحظ لوسون. تداخل الحمض النووي الريبوزي أحيانا يغير تعبير جينات غير الهدف المطلوب . والتدخل مع آلية معالجة الحمض النووي الريبوزي الداخلية للخلية يمكن أن تؤثر احيانا على الأنظمة الخلوية الأخرى التي تشمل الحمض النووي الريبوزي. يتطلب التحرير الجيني كريسبر-Cas9، في الوقت نفسه، كسر خيوط الحمض النووي الريبوزي منقوص الاكسجين - والتي يمكن أن تحفز استجابات أخرى في الخلية، بما في ذلك انتحار الخلية. ويمكن لهذه التقنية أيضا أن تقطع الحمض النووي في بعض الأحيان في مواقع غير مقصودة.
الرجوع إلى الأساسيات
النتائج المتعارضة من تداخل الحمض النووي الريبوزي والمسوحات الوراثية لا تعني دائما أن نهجا واحدا كان صحيحا والآخر كان خاطئا، ينبه باسيك. بعض الخلايا قد تستجيب بشكل مختلف للتغير الجيني الذي يمحو التعبير الجيني للجين، كما هو غالبا الهدف لدى كريسبر-Cas9، مقارنة ب كيف أنها تستجيب لتقليل التعبير إلى مستويات منخفضة جدا بتداخل الحمض النووي الرايبوزي .
ولكن في كثير من الأحيان، ويضيف، السبب وراء هذا التناقض يمكن تعقبها مرة أخرى إلى إمكانات تداخل الحمض النووي الرايبوزي لآثار خارج الهدف. وكانت الاهتمامات بشأن ذلك تجمع الباحثون لإعادة إنتاج النتائج القديمة.
في حالة ميلك، نتائج كريسبر-Cas9 هي ذات أهمية خاصة لأنها يمكن أن تقوض الأساس العلمي لإجراء التجارب السريرية. لكن فريق شيلتزر أظهر فقط أن ميلك لا يبدو له دورا في انقسام الخلايا السرطانية، كما يلاحظ كارلوس مورينو، باحث السرطان في جامعة إيموري في أتلانتا، جورجيا. من الممكن أن جوانب أخرى من ميلك، مثل دوره المزعوم في جعل الخلايا السرطانية أكثر مقاومة للإشعاع، لا تزال صالحة، كما يقول
وأضاف أن العديد من الأدوية الناجحة قد وضعت على خلفية فرضية علمية خاطئة. مثبطات ميلك في التجارب السريرية قد تعمل من خلال بعض الآليات الأخرى، على سبيل المثال. وقال "هذا لن يكون سببا لوقف التجربة إذا كانت تظهر اثارا ايجابية". "من المهم عدم رمي الطفل بالمياه الحمامية"
المصادر
- Team, Forvo. "CRISPR-Cas9 pronunciation: How to pronounce CRISPR-Cas9 in English". Forvo.com (باللغة الإنجليزية). مؤرشف من الأصل في 30 أبريل 2019. اطلع عليه بتاريخ 30 أبريل 2019. الوسيط
|CitationClass=تم تجاهله (مساعدة)
قراءة إضافية
- Kennedy EM, Cullen BR (2015). "Bacterial CRISPR/Cas DNA endonucleases: A revolutionary technology that could dramatically impact viral research and treatment". Virology. 479–480: 213–20. doi:10.1016/j.virol.2015.02.024. PMC 4424069. PMID 25759096. الوسيط
|CitationClass=تم تجاهله (مساعدة) - Ian M. Slaymaker; Linyi Gao; Bernd Zetsche; David A. Scott; Winston X. Yan; Feng Zhang (2015). "Rationally engineered Cas9 nucleases with improved specificity". Science. 351. doi:10.1126/science.aad5227. PMC 4714946. PMID 26628643. الوسيط
|CitationClass=تم تجاهله (مساعدة) - CRISPR-Cas: A Laboratory Manual Edited by Jennifer Doudna, University of California, Berkeley; Prashant Mali, University of California, San Diego
- : Novel CRISPR/Cas9 Monoclonal Antibody Diagenode launches the industry’s first monoclonal antibody targeting CRISPR/Cas9
- بوابة تقانة
- بوابة تقانة حيوية
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي