استخدام أسيتات الكايتين لالتقاط غاز ثاني أكسيد الكربون والحد من التلوث
استخدام الكايتين لالتقاط غاز ثاني أكسيد الكربون والتقليل من التلوث: يعتبر غاز ثاني أكسيد الكربون من الغازات الدفيئة المسببة لظاهرة الاحتباس الحراري التي تتسبب بالعديد من الكوارث الطبيعية كالفيضانات والجفاف والأعاصير وارتفاع مستوى سطح البحر وذوبان الجليد في القطبين وما ينتج عنها من آثار مدمرة لكوكب الأرض. ينتج غاز ثاني أكسيد الكربون بشكل رئيسي من احتراق الوقود الأحفوري وغيرها من النشاطات الإنسانية التي يتم فيها حرق الوقود الأحفوري لتوليد الكهرباء وفي الصناعات المختلفة، وقد ظهرت في السنوات الأخيرة العديد من الدراسات والأبحاث لإيجاد مواد صديقة للبيئة قادرة على التقاط غاز ثاني أكسيد الكربون وتخزينه بعد عملية احتراق الوقود الأحفوري فيما عرف باسم (CO2 capture and storage CCS).
| استخدام أسيتات الكايتين لالتقاط غاز ثاني أكسيد الكربون والحد من التلوث | |
|---|---|
 استخدام أسيتات الكايتين لالتقاط غاز ثاني أكسيد الكربون والحد من التلوث | |
 استخدام أسيتات الكايتين لالتقاط غاز ثاني أكسيد الكربون والحد من التلوث |
 استخدام أسيتات الكايتين لالتقاط غاز ثاني أكسيد الكربون والحد من التلوث |
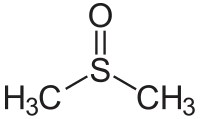
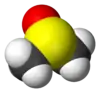
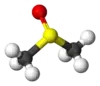
 A sample of dimethyl sulfoxide A sample of dimethyl sulfoxide | |
| الاسم النظامي (IUPAC) | |
Dimethyl sulfoxide | |
| تسمية الاتحاد الدولي للكيمياء | |
Methanesulfinylmethane (substitutive) | |
| المعرفات | |
| الاختصارات | DMSO, Me2SO |
| رقم CAS | 67-68-5 |
| بوب كيم (PubChem) | 679 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | C2H6OS |
| كتلة مولية | 78.13 غ.مول−1 |
| المظهر | Colourless liquid |
| الكثافة | 1.1004 g cm−3 |
| نقطة الانصهار | 19 °س، 292 °ك، 66 °ف |
| نقطة الغليان | 189 °س، 462 °ك، 372 °ف |
| الذوبانية في الماء | Miscible |
| الذوبانية في ثنائي إيثيل الإيثر | very soluble |
| حموضة (pKa) | 35[1] |
| معامل الانكسار (nD) | 1.479 εr = 48 |
| اللزوجة | 1.996 cP at 20 °C |
| البنية | |
| البنية الجزيئية | trigonal pyramidal |
| عزم جزيئي ثنائي القطب | 3.96 D |
| كود ATC | G04 |
| المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| مخاطر | Irritant and flammable |
| NFPA 704 |
2
1
0
|
| نقطة الوميض | 89 °C |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
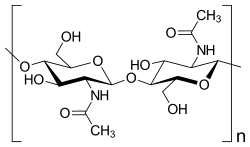
من الأمثلة على هذه المواد استخدام الكايتين وهو مبلمر يتكون من أحد مشتقات سكر الغلوكوز كوحدات بنائية لالتقاط ثاني أكسيد الكربون بعد عمليات الاحتراق، الكايتين مادة طبيعية توجد بشكل رئيسي في الجدار الخلوي لبعض الفطريات والهيكل الخارجي لمفصليات الأرجل. وقد تم اختبار فعالية الكايتين لالتقاط غاز ثاني أكسيد الكربون، بإذابته في ثنائي ميثيل سلفوكسيد (الموضح في الشكل بالأعلى) الذي يعتبر من المذيبات الصديقة للبيئة، ومن ثم تدفق غاز ثاني أكسيد الكربون في المحلول لمدة عشرين دقيقة، وبإجراء العديد من القياسات مثل الرنين المغناطيسي النووي وتحليل الأشعة الحمراء والموصلية الكهربائية للمحلول الناتج بعد تدفق غاز ثاني أكسيد الكربون، أُثبت تكون رابطة تساهمية بين غاز ثاني أكسيد الكربون وذرة الأكسجين في الكايتين. لقد طورت هذه الدراسة استخدام مواد غير ملوثة للبيئة للتخلص من أهم الغازات الدفيئة بكفاءة عالية وصلت إلى امتصاص 3.36 ملي مول من ثاني أكسيد الكربون لكل غرام من الكايتين، وتتميز بالقدرة على استرجاع الكايتين من جديد لإعادة استخدامه بطرق قليلة التكلفة كزيادة درجة الحرارة أو تمرير تيار كهربائي في المحلول.
مراجع
- Matthews, W.S., Bares, J.E., Bartmess, J.E., Bordwell, F.G., Cornforth, F.J., Drucker, G.E., Margolin, Z., McCallum, R.J., McCollum, G.J., Vanier, N.R.; Bares; Bartmess; Bordwell; Cornforth; Drucker; Margolin; McCallum; McCollum; Vanier (1975). "Equilibrium acidities of carbon acids. VI. Establishment of an absolute scale of acidities in dimethyl sulfoxide solution". J. Am. Chem. Soc. 97 (24): 7006–7014. doi:10.1021/ja00857a010. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link)
