أكسيد السيريوم الرباعي
أكسيد السيريوم الرباعي (أو ثنائي أكسيد السيريوم) مركب كيميائي له الصيغة CeO2، ويكون على شكل بلورات بيضاء إلى صفراء شاحبة. وهو أحد أكاسيد للعنصر الأرضي النادر السيريوم، إذ يوجد أيضاً أكسيد السيريوم الثلاثي Ce2O3، وأكسيد السيريوم الثلاثي والرباعي Ce3O4. يمكن أن يوجد بشكل لامائي أو على شكل أحادي هيدرات.
| أكسيد السيريوم الرباعي[1] | |
|---|---|
_oxide.jpg.webp) أكسيد السيريوم الرباعي | |
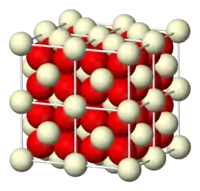 أكسيد السيريوم الرباعي | |
| الاسم النظامي (IUPAC) | |
أكسيد السيريوم الرباعي | |
| المعرفات | |
| رقم CAS | 1306-38-3 12014-56-1 (أحادي هيدرات) |
| بوب كيم | 73963 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | CeO2 |
| الكتلة المولية | 172.12 غ/مول |
| المظهر | بلورات بيضاء إلى صفراء شاحبة |
| نقطة الانصهار | 2000 °س |
| الذوبانية في الماء | غير منحل |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- إن مركب أكسيد السيريوم الرباعي غير منحل في الماء، لكنه ينحل في حمض الكبريتيك المركز الساخن حيث يشكل كبريتات السيريوم كما في المعادلة:
CeO2 + H2SO4 → Ce(SO4)2 + 2H2O
التحضير
يحضر أكسيد السيريوم الرباعي من التفكك الحراري لمركبات مثل نترات السيريوم الثلاثي Ce(NO3)3 أو أكسالات السيريوم الثلاثي Ce2(C2O4)3 بوجود الهواء.[5]
الاستخدامات
التحفيز
يستخدم أكسيد السيريوم الرباعي كحفاز في آليات النقل، حيث أنه عند نقص الأكسجين يؤكسد غاز أحادي أكسيد الكربون إلى ثنائي أكسيد الكربون حسب المعادلة:
4CeO2 + 2CO → 2Ce2O3 + 2CO2
وعند توفر الأكسجين في غاز العادم تحدث عملية إعادة تنشيط للحفاز كما يلي:
2Ce2O3 + O2 → 4CeO2
قميص الغاز
استعمل أكسيد السيريوم الرباعي فيما مضى في تركيب قمصان الغاز Gas mantle، حيث أن المزيج المثالي للتركيب والذي يعطي أفضل إضاءة كان يتألف من حوالي 99% أكسيد الثوريوم الرباعي (ThO2) و1% أكسيد السيريوم الرباعي (CeO2).
تشبّع ألياف من الحرير الصناعي أو الرايون بمحاليل نترات فلزي السيريوم والثوريوم، وعند اشتعال اللهب وتماسه مع النترات تتشكل الأكاسيد والتي تكون مسؤولة عن إصدار الضوء في الطيف المرئي عند التهابها.
استخدامات أخرى
- يستخدم أكسيد السيريوم الرباعي كوسيلة لصقل الأدوات الزجاجية في مجال البصريات، حيث يسمى باسم أوبالين Opaline. يشكل عادة مستعلق من أكسيد السيريوم الرباعي وذلك بمزجه مع ماء خال من الأيونات بنسبة 60 غ لكل لتر واحد من الماء.[6]
- أدت الأبحاث إلى تطوير طريقة لتوليد الهيدروجين من أشعة الشمس وذلك باستخدام دورة أكسيد السيريوم الرباعي-أكسيد السيريوم الثلاثي Cerium(IV) oxide-cerium(III) oxide cycle وذلك كوسيلة لإيجاد حلول لأزمة الطاقة المستقبلية.[7]
المراجع
- صفحة بيانات السلامة الكيميائية من Merck نسخة محفوظة 28 مايو 2020 على موقع واي باك مشين.
- وصلة : معرف بوب كيم — الرخصة: محتوى حر
- وصلة : معرف بوب كيم
- Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- Easwar S. Ranganathan, Shyamal K. Bej, Levi T. Thompson (2005). "Methanol steam reforming over Pd/ZnO and Pd/CeO2 catalysts". Applied Catalysis A: General. 289 (2): 153–162. doi:10.1016/j.apcata.2005.04.022. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Optimierung der chemischen Einflüsse bei der mechanischen Politur von Glas نسخة محفوظة 26 مايو 2020 على موقع واي باك مشين.
- Hydrogen production from solar thermochemical water splitting cycles نسخة محفوظة 30 أغسطس 2009 على موقع واي باك مشين. "نسخة مؤرشفة". Archived from the original on 16 يونيو 2013. اطلع عليه بتاريخ 15 يوليو 2017. الوسيط
|CitationClass=تم تجاهله (مساعدة)صيانة CS1: BOT: original-url status unknown (link)
- بوابة الكيمياء